
科目: 来源: 题型:
【题目】下表为元素周期表的一部分:

请参照元素①一⑨在周期表表中的位置,用化学用语回答下列问题:
(1)写出元素⑥在周期表中的位置是____________。
(2)元素⑤、⑧、⑨的离子半径由大到小的顺序为______________。
(3)元素①④⑨形成原子个数比1:1:1化合物的电子式为_________;写出元素⑤和⑧形成原子个数比2:1化合物的形成过程:_________________。
(4)元素⑤和⑥最高价氧化物水化物反应的离子方程式为_______________。
(5)②的单质与⑧的最高价氧化物水化物浓溶液反应的化学方程式为______________________,若反应中有6.02×1023个电子发生转移,则生成的气体标准状况下的体积为______L。
(6)写出一个方程式,证明元素⑧的非金属性比元素⑨弱:____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)现有如下A、B两反应:
A: 2NaOH+H2SO4=Na2SO4+2H2O;B:Zn+H2SO4=ZnSO4+H2↑
则A、B反应能设计成为原电池的是____(填“A”或“B”)。
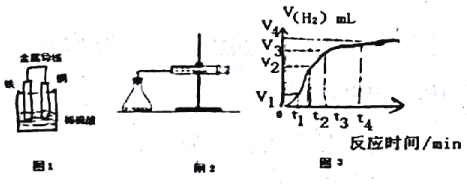
(2)某原电池示意图如图1,则该电池负极电极的反应方程式为_______________。
(3)若该电池反应过程中共有0.3mol电子发生转移,则生成的气体体积在标准状况下的体积是_____L。
(4)为了研究Fe与稀H2SO4反应的速率,某同学通过如图2实验装置测定反应中生成的H2体积,绘制了如图3所示的曲线,在该实验过程中发现锥形瓶温度升高。请回答以下问题。
在0~tl、tl~t2、t2~t3各个时间段里,反应速率最大的时间段是____,产生这种情况可能的原因是_____;该实验过程中收集到气体最多的是在______时间内。
(5)为了减缓该反应的速率,你认为可行的方法是________。
A.向H2SO4溶液中加蒸馏水 B.将Fe片改成Fe粉
C.向H2SO4溶液中加Na2SO4溶液 D.向H2SO4溶液中滴入几滴Cu(NO3)2溶液.
查看答案和解析>>
科目: 来源: 题型:
【题目】饮食是保证我们身体健康的基本需求,下列关于饮食的说法正确的是
A. 鸡蛋含有丰富的蛋白质,人类需要的蛋白质都可以由鸡蛋提供,多吃有益
B. 水果、蔬菜含有丰富的维生素,有人为了减肥,每天只吃水果蔬菜即可
C. 米饭含有大量的淀粉,成人每天食用量不能超过200g。
D. 要促进身体健康,各种食物必须合理搭配
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活密切相关,下列叙述错误的是( )·
A.用热的的纯碱溶液清除灶具上的油污
B.用硫酸清洗锅炉中的水垢
C.用明矾[KAl(SO4)2 ·12H2O]作净水剂,除去水中悬浮的杂质
D.用Na2S作沉淀剂,除去废水中的Cu2+和Hg2+
查看答案和解析>>
科目: 来源: 题型:
【题目】四氢硼锂(LiBH4)是一种重要的化学试剂,低温下可与 HCl 气体发生如下反应:
2LiBH4 + 2 HCl![]() 2 LiCl + B2H6 + 2 H2
2 LiCl + B2H6 + 2 H2
该反应中,LiBH4和B2H6 中的氢元素均显-1价。 请回答下列问题。
(1)LiBH4 中硼元素的化合价为________。
(2)该反应的还原剂为________;4 mol LiBH4 完全反应后共失去________mol 电子。
查看答案和解析>>
科目: 来源: 题型:
【题目】图是元素周期表的一部分,请回答下列问题。
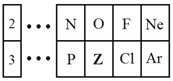
(1)Z元素在元素周期表中位于第________族。
(2)Z的原子半径__________(填“大于”、“小于”或“等于”)Si的原子半径。
(3)Cl元素的非金属性比Z元素的__________(填“强”或“弱”)。
(4)Z元素的气态氢化物的化学式为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。回答下列问题:
(1) NaClO2的化学名称为_______。
(2)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×103 mol·L1 。反应一段时间后溶液中离子浓度的分析结果如下表。
离子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式__________。增加压强,NO的转化率______(填“提高”、“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐______ (填“增大”“不变”或“减小”)。
③由实验结果可知,脱硫反应速率______脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________。
(3)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压pe如图所示。
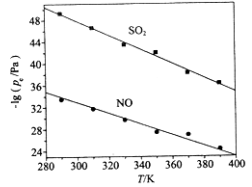
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均______________(填“增大”、“不变”或“减小”)。
②反应ClO2+2SO32===2SO42+Cl的平衡常数K表达式为___________。
(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。
①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是_______。
②已知下列反应:
SO2(g)+2OH (aq) ===SO32 (aq)+H2O(l) ΔH1
ClO (aq)+SO32 (aq) ===SO42 (aq)+Cl (aq) ΔH2
CaSO4(s) ===Ca2+(aq)+SO42(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO (aq) +2OH (aq) === CaSO4(s) +H2O(l) +Cl (aq)的ΔH=______。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)可用作分析试剂、鞣革还原剂、脱氯剂等。它受热、遇酸易分解。它有多种制备方法,其中硫化碱法为:向热的硫化钠和亚硫酸钠混合液中通入二氧化硫,经吸硫、蒸发、结晶,制得硫代硫酸钠晶体。制备过程中发生的主要反应如下:
Na2S + H2O + SO2 → Na2SO3 + H2S ………… (i)
2H2S + SO2 → 3S + 2H2O …………………… (ii)
S + Na2SO3 —△→ Na2S2O3 …………………(iii)
(1)已知Na2S2O3分解反应是吸热反应,由此可得出:该分解反应中,反应物断裂化学键所吸收的总能量_________(填“大于”、“小于”或“等于”)生成物形成化学键所放出的总能量。
(2)Na2S2O3具有还原性,判断依据是_________、_________(至少写出两条)。
(3)上述反应i ~ iii总反应的化学方程式为_________。制备过程中,即使将反应物的用量按化学方程式的计量数进行配比,反应后各反应物仍有剩余,这说明该过程中存在_________。
(4)为了保证硫代硫酸钠的产量,生产中通入的SO2不能过量,原因是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)与汽油相比,氢气作为燃料的优点是_________(至少答出两点)。但是氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的负极反应式:____________。
(2)氢气可用于制备H2O2。已知:
H2(g)+A(l)=B(l) ΔH1
O2(g)+B(l)=A(l)+H2O2(l) ΔH2
其中A、B为有机物,两反应均为自发反应,则H2(g)+ O2(g)= H2O2(l)的ΔH____0(填“>”、“<”或“=”)。
(3)在恒温恒容的密闭容器中,某储氢反应:MHx(s)+yH2(g)![]() MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
MHx+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是________。
a.容器内气体压强保持不变
b.吸收y mol H2只需1 mol MHx
c.若降温,该反应的平衡常数增大
d.若向容器内通入少量氢气,则v(放氢)>v(吸氢)
(4)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为_______。
(5)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na2FeO4,同时获得氢气:Fe+2H2O+2OH![]() FeO42+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。
FeO42+3H2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO42,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na2FeO4只在强碱性条件下稳定,易被H2还原。

①电解一段时间后,c(OH)降低的区域在_______(填“阴极室”或“阳极室”)。
②电解过程中,须将阴极产生的气体及时排出,其原因是_______。
③c( Na2FeO4)随初始c(NaOH)的变化如图2,任选M、N两点中的一点,分析c(Na2FeO4)低于最高值的原因:_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com