
科目: 来源: 题型:
【题目】检验实验室配制的FeCl2溶液中的Fe2+是否被氧化生成Fe3+ , 应选用的最适宜的试剂是( )
A.稀硝酸
B.溴水
C.KSCN溶液
D.酸性高锰酸钾
查看答案和解析>>
科目: 来源: 题型:
【题目】氮化铝(AlN)是一种综合性能优良的陶瓷材料,能缓慢水解,不耐酸碱腐蚀。某小组探究在实验室制备AlN并测定产品纯度,设计实验如下。请回答:
Ⅰ.制备AlN
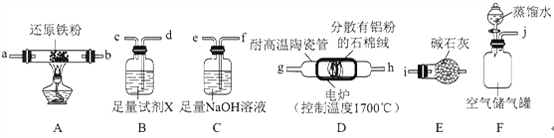
(1)实验时,以空气为原料制备AlN。按气流由左向右的方向,上述装置的正确连接顺序为j→________→i(填仪器接口字母编号)。
(2)上述装置中,需要检漏的仪器名称为________。
(3)试剂X的作用为________。
(4)装置D中发生反应的化学方程式为________。
Ⅱ.测定产品纯度
(5)设计实验证明:装置D的产品中含有Al单质________。
(6)测定产品纯度:取装置D中产品4.37g,加入足量NaOH浓溶液;通入水蒸气,将生成的气体全部蒸出,用V1mLc1mol·L-1的盐酸吸收;以酚酞作指示剂,用c2mol·L-1的NaOH标准溶液滴定过量的盐酸,达到滴定终点时,消耗V2mLNaOH标准溶液。则:
①达到滴定终点的现象为________。
②产品中A1N的质量分数为________(列出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】有关水解原理的应用,下列说法正确的是
A.将NaHCO3溶液蒸干并灼烧时,HCO3-+H2O![]() H2CO3+OH-向正向移动,最后可以得到NaOH固体
H2CO3+OH-向正向移动,最后可以得到NaOH固体
B.MgSO4酸性溶液中含有杂质离子Fe2+时,可以先加人氯水将Fe2+氧化成Fe3+,再加入MgO除去杂质
C.为抑制离子的水解,在配制SnCl2溶液时,可以加入适量稀硫酸加以酸化
D.用MgCl2 6H2O制取无水MgCl2时,需要在HCl气流中加热
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列有关叙述不正确的是( )
A.标准状况下,1L庚烷所含有的分子数为![]()
B.1mol甲基(-CH3)所含电子数为9NA
C.标准状况下,B2H6和C2H4的混合气体22.4L,所含的电子数为16NA
D.26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:CH3CH2OH+NaBr+H2SO4(浓)![]() CH3CH2Br+NaHSO4+H2O。实验室制备溴乙烷(沸点为38.4℃)的装置和步骤如下:
CH3CH2Br+NaHSO4+H2O。实验室制备溴乙烷(沸点为38.4℃)的装置和步骤如下:
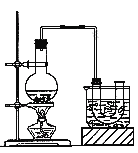
①按下图所示连接仪器,检查装置的气密性,然后向U形管和大烧杯里加入冰水;②在圆底烧瓶中加入10mL95%乙醇、28mL浓硫酸,然后加入研细的13g溴化钠和几粒碎瓷片;③小火加热,使其充分反应。
(1)反应时若温度过高可看到有红棕色气体产生,该气体的化学式为 。
(2)为了更好的控制反应温度,除用图示的小火加热,更好的加热方式是____ ______。
(3)反应结束后,U形管中粗制的溴乙烷呈棕黄色。将U形管中的混合物倒入分液漏斗中,静置,待液体分层后,分液,取下层液体。为了除去其中的杂质,可选择下列试剂中的 (填序号)。
A.Na2SO3溶液 B.H2O C.NaOH溶液 D.CCl4
(4)要进一步制得纯净的C2H5Br,可再用水洗,然后加入无水CaCl2干燥,再进行 (填操作名称)。
(5)下列几项实验步骤,可用于检验溴乙烷中的溴元素,其正确的操作顺序是:取少量溴乙烷,然后 (填序号)。
①加入AgNO3溶液 ②加入稀HNO3酸化③冷却④加热⑤加入NaOH溶液上述实验过程中C2H5Br发生的反应方程式为 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关硅的叙述中,正确的是( )
A.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有元素中居第一位
B.硅的化学性质不活泼,在常温下不与任何物质反应
C.硅在电子工业中是最重要的半导体材料
D.硅的性质很稳定,能以单质的形式存在于自然界中
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质的性质与应用对应关系不正确的是
A. 二氧化氯具有强氧化性,可用于杀菌消毒
B. 氢氧化铝具有弱碱性,可用于治疗胃酸过多
C. 二氧化硅的熔沸点很高,可用于制作石英坩埚
D. 钠钾合金的密度小,可用于快中子反应堆的热交换剂
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“ · ”代表一种元素,其中O点代表氢元素.下列说法中错误的是
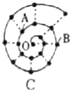
A. 离O点越远的元素原子半径越大
B. 虚线相连的元素处于同一族,A元素位于元素周期表ⅥA族
C. B元素是图中金属性最强的元素
D. B、C最高价氧化物的水化物可以相互反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com