
科目: 来源: 题型:
【题目】人体每天均需要从食物中获取各种营养物质。下列不属于人体能消化吸收的营养素是( )
A. 糖类、油脂 B. 蛋白质、维生素
C. 水、矿物质 D. 纤维素
查看答案和解析>>
科目: 来源: 题型:
【题目】海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是( )
A.利用潮汐发电是将化学能转化为电能
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备Na
D.海水中含有溴元素,只需经过物理变化就可以得到溴单质
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用0.1000 mol·L-1 NaOH溶液分别滴定20.00 mL 0.1000 mol·L-1 HBr溶液和20.00 mL0.1000 mol·L-1 CH3COOH溶液,得到2条滴定曲线,如图所示,下列说法不正确的是( )

A. 根据图1和图2判断,滴定HBr溶液的曲线是图1
B. a=20.00mL
C. c(Na+)=c(CH3COO-)的点是B点
D. E点对应溶液中离子浓度由大到小的顺序为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在体积为2L的密闭容器中通入气体M和N并发生反应,物质的量随时间的变化关系如图。下列说法正确的是( )
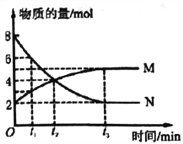
A. M、N之间转化的反应方程式为M =2N
B. t2时刻,反应达到平衡,正、逆反应速率达到相等
C. t3时刻,M的反应速率为![]() mol·L-1·min-l
mol·L-1·min-l
D. t1时刻,在容器内气体M和N的物质的量浓度之比为1:2
查看答案和解析>>
科目: 来源: 题型:
【题目】石油裂解气用途广泛,由石油裂解气合成生物可降解高聚物J的合成线路如下:
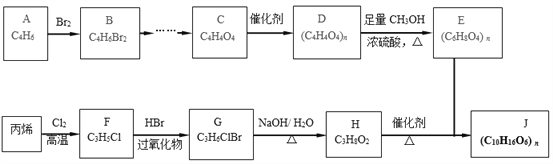
已知:
i.酯与酯可发生如下酯交换反应:RCOOR'+R"OH![]() RCOOR"+R'OH(R、R'、R"代表烃基)
RCOOR"+R'OH(R、R'、R"代表烃基)
ii.烯烃中,碳碳双键相邻为不稳定结构,碳碳双键易被氧化剂氧化。
(1)A为链状烃,其核磁共振氢谱中有两组峰且面积之比是1:2,则A的名称为____________。
(2)B 中所含官能团名称为____________ 。
(3)C→D的反应类型 ______________。
(4)C能与足量的 NaHCO3 溶液反应生成C4H2O4Na2, C的结构简式为_______________。
(5)D→E的化学方程式是 ______________。
(6)H中不含甲基,H与E形成对称型高聚物J的化学方程式是______________。
(7)请完成 B → C 的合理路线________________ 。( 无机试剂任选)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知碳碳单键可以绕键轴自由旋转,结构简式为如下图所示的烃,下列说法中正确的是( )

A. 分子中处于同一直线上的碳原子最多有6个
B. 分子中至少有12个碳原子处于同一平面上
C. 该烃苯环上的一氯代物共有 3种
D. 该烃苯环上一氯代物共有5种
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图是铜与硝酸反应的实验改进装置,根据实验回答下列问题:

(1)仪器a的名称是________;按图组装好装置后,首先进行的操作是____;
(2)c中放一小块铜片,由分液漏斗a向c中加入2mL浓硝酸,c中主要反应的离子方程式是____;充分反应后再由a向c中加2mL蒸馏水,此时c中气体颜色变浅,反应的离子方程式为________;
(3)表中是制取硝酸铜的三种方案,能体现环保理念的最佳方案是
方案 | 反应物 |
甲 | Cu、浓HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2.稀HNO3 |
(4)该兴趣小组还用上述装置制备收集氨气,回答下列问题:
①利用上述装置制氨气,最合理的试剂组合是_________。
A.Ca (OH)2溶液与NH4Cl溶液 B.浓氨水与新制生石灰 C.NH4HCO3溶液与硫酸
②上述选择的试剂能制氨气的理由是_________。
③此实验装置用于制备收集氨气不合理之处有:_________、_________。(写出两点)
查看答案和解析>>
科目: 来源: 题型:
【题目】氨是重要的化工产品之一,有着广泛的用途,运用化学反应原理的相关知识研究氨的合成及性质对工业生产有着十分重要意义。
I.合成氨用的氢气可以甲烷为原料制得:CH4(g)+H2O(g) ![]() CO(g)+3H2(g)。有关化学反应的能量变化如下图所示。CH4(g)与H2O (g)反应生成CO (g)和H2 (g)的热化学方程式为______________。
CO(g)+3H2(g)。有关化学反应的能量变化如下图所示。CH4(g)与H2O (g)反应生成CO (g)和H2 (g)的热化学方程式为______________。

II.恒温下,将一定量N2、H2置于10L的容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g) △H=-92.0kJ/mol,反应过程中各物质的物质的量随时间变化如下图。
2NH3(g) △H=-92.0kJ/mol,反应过程中各物质的物质的量随时间变化如下图。

(1)图中0~2s内的反应速率v(NH3)=______;该温度下达平衡时N2的转化率为_____。
(2)若其它条件不变,将恒容条件变为恒压,则平衡时c(N2)__,平衡常数___。(填编号)
A.增大 B.减小 C.不变 D.不能确定
(3)在不同温度下达到平衡时测得NH3的体积分数如下表所示:
T/℃ | 200 | 300 | 400 |
NH3的体积分数 | a1 | a2 | 38% |
①试比较a1、a2的大小:a1_____a2(填“>”、“<”或“=”)。
②若反应在恒容400℃条件下进行,下列能判断反应达到平衡状态的依据有____ (填编号)。
A.断裂1molH-H键同时断裂2molN-H键 B.v正(N2)=3V逆(H2)
C.容器内N2、H2、NH3;的物质的量之比为1:3:2 D.平衡常数保持不变
E.混合气体的平均相对分子质量保持不变 F.混合气体的密度保持不变
(4)工业上合成氨采用了高温高压、催化剂的条件,根据反应判断下列哪些条件有利于提高氨的产率____。
A.采用400℃~500℃高温 B.采用合适的高压
C.使用铁触媒做催化剂 D.将氨液化从体系中分离出来
(5)氨气制取尿素[CO (NH2)2]的反应:2NH3 (g) +CO2(g) ![]() CO (NH2)2 (1)+H2O (g)。
CO (NH2)2 (1)+H2O (g)。
①该反应温度升高,氨气的百分含量增大,则△H______0(填“>”、“<”或“=”)。
②CO的平衡转化率与温度、压强的关系如图所示, 若充入2mol NH3与1mol CO2在2L密闭容器中进行反应,则100℃时反应的平衡常数K=________;压强的大小关系:P1______P2(填“>”、“<”、“=”或“不确定”)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com