
科目: 来源: 题型:
【题目】部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数 (25℃) | Ka=1.77×104 | Ka=4.9×1010 | Ka1=4.3×107 Ka2=5.6×1011 |
下列选项正确的是
A.NaCN溶液中通入少量CO2气体:c(Na+) > c(![]() ) >c(
) >c(![]() )
)
B.稀释等体积、等浓度的HCOOH和HCN至相同pH,加水的体积前者小于后者
C.物质的量浓度相等的HCOONa和KCN溶液中:c(Na+)c(HCOO) >c(K+)c(CN)
D.等体积、等浓度的HCOOH和NaCN混合溶液中:c(H+)+c(HCN) =c(HCOO)+c(OH)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列条件下,两物质所含分子数不相等的是 ( )
A.同温度、相同质量的N2和CO
B.常温常压,同体积的H2O和O2
C.同压强、同物质的量的N2和O2
D.同温度、同压强、同体积的N2O和CO2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.增大体系压强,活化分子数增加,化学反应速率一定增大
B.加入反应物,使活化分子百分数增加,化学反应速率增大
C.活化分子间所发生的分子间的碰撞均为有效碰撞
D.升高温度,活化分子百分数增加,化学反应速率一定增大
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是( )
A. 溴水中有下列平衡Br2+H2O![]() HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅
B. 已知, N2 (g) + 3 H2(g)![]() 2NH3(g) △H﹤0 ,为提高氨的产率,理论上应采取降低温度的措施
2NH3(g) △H﹤0 ,为提高氨的产率,理论上应采取降低温度的措施
C. 反应CO(g)+NO2(g)![]() CO2(g)+NO(g)△H﹤0,达平衡后,升高温度体系颜色变深
CO2(g)+NO(g)△H﹤0,达平衡后,升高温度体系颜色变深
D. 对于2HI(g)![]() H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
H2(g)+I2(g),达平衡后,缩小容器体积可使体系颜色变深
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用盐酸酸化的FeCl3溶液腐蚀铜制线路板,分别取腐蚀后的滤液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是
A.通入过量Cl2:Fe3+、H+、Cu2+、Cl
B.加入过量SO2:Fe3+、H+、Cu2+、![]() 、Cl
、Cl
C.加入过量NaOH溶液:Na+、Fe2+、OH、Cl
D.加入过量CuO:Fe2+、H+、Cu2+、Cl、
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,向20.00mL 0.1000mol·L-1(NH4)2SO4溶液中逐滴加入0.2000mol·L-1NaOH时,溶液的pH与所加NaOH溶液体积的关系如下图所示(不考虑挥发)。下列说法正确的是

A. 点a所示溶液中:c(NH4+)>c(SO42-)>c(OH-)>c(H+)
B. 点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH-)
C. 点c所示溶液中:c(SO42-)+c(H+)=c(NH3H2O)+c(OH-)
D. 点d所示溶液中:c(SO42-)>c(NH3H2O)>c(NH4+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.油脂有油和脂肪之分,但都属于酯
B.糖类、油脂、蛋白质都是高分子化合物
C.糖类、油脂、蛋白质都能发生水解
D.葡萄糖与淀粉互为同分异构体
查看答案和解析>>
科目: 来源: 题型:
【题目】分子式为C4H10O且属于醇类的同分异构体有x种(不包括立体异构,下同),分子式为C5H10O且属于醛类的有机物的同分异构体有y种,则 x和y的关系为( )
A. x=yB. x>yC. x<yD. 无法确定
查看答案和解析>>
科目: 来源: 题型:
【题目】为解决能源短缺问题,工业生产中应合理利用化学能。
(1)25 ℃,1.01×105 Pa时,实验测得,4 g氢气在O2中完全燃烧生成液态水,放出572 kJ的热量,则表示H2的燃烧热的热化学方程式为______________________。
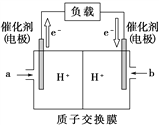
(2)上图是某笔记本电脑使用的甲醇燃料电池的结构示意图。放电时甲醇应从________处通入(填“a”或“b”),电池内部H+向_______(填“左”或“右”)移动。写出电池负极的电极反应式________。正极的电极反应式_______________________。
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
化学键 | H—H | N—H | N≡N |
键能/kJ·mol-1 | 436 | a | 945 |
已知:N2(g)+3H2(g)===2NH3(g) ΔH=-93 kJ·mol-1。
试根据表中所列键能数据计算a的数值________。
当可逆反应中净生成N—H物质的量为2mol 时,反应放热_____________。
(4)已知:C(s,石墨)+O2(g)===CO2(g) ΔH1=-393.5 kJ·mol-1 ①
2H2(g)+O2(g)===2H2O(l) ΔH2=-571.6 kJ·mol-1 ②
2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1 ③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)===C2H2(g)的ΔH=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com