
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 油脂一般相对分子质量很大,所以油脂是高分子化合物
B. 蛋白质水解的最终产物既能和强酸反应,又能和强碱反应
C. 葡萄糖、果糖、麦芽糖和蔗糖都能与新制氢氧化铜浊液发生反应
D. 纤维素属于高分子化合物,与淀粉互为同分异构体
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关常见的几种金属氧化物的性质和用途的说法不正确的是( )
A. 氧化钙可用作干燥剂
B. Al2O3可用作耐火材料
C. Fe2O3用于制作红色油漆和涂料
D. Na2O2、CuO、FeO都能溶于水,且与水反应都生成相应的碱
查看答案和解析>>
科目: 来源: 题型:
【题目】一种有机物燃烧后产生CO2,H2O,SO2据此可以断定该化合物中一定含有
A. C.S.O B. C.H.S C. C.H.O.S. D. C.H.O
查看答案和解析>>
科目: 来源: 题型:
【题目】已知分解100 g CaCO3需要177.7 kJ的热量,而12 g碳完全燃烧,则放出393 kJ的热。求:
(1)煅烧1 t石灰石需要多少热量?
(2)这些热量全部由碳燃烧提供,问理论上要消耗多少克碳?
查看答案和解析>>
科目: 来源: 题型:
【题目】碳及其化合物广泛存在于自然界。请回答下列问题:
(1)以CO2与NH3为原料可合成尿素[CO(NH2)2]。已知:
①2NH3(g) + CO2(g) === NH2COONH4(s) △H=-159.47 kJ·mol-1
②NH2COONH4(s) === CO(NH2)2(s) + H2O(g) △H=+116.49 kJ·mol-1
③H2O(l) === H2O(g) △H=+88.0 kJ·mol-1
写出NH3和CO2合成尿素和液态水的热化学方程式_____________。
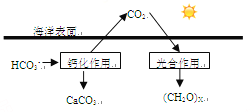
(2)海洋是地球上碳元素的最大“吸收池”。
①溶于海水中的CO2主要以四种无机碳形式存在,即:CO2、H2CO3、___________、_________。
②在海洋碳循环中,可通过右图所示的途径固碳。写出钙化作用的离子方程式_____________。
(3)常温常压下,空气中的CO2溶于水中达到平衡时,其转化关系如下:
①CO2 + H2O![]() H2CO3 K=1.8×10-3
H2CO3 K=1.8×10-3
②H2CO3![]() H++HCO3- K a 1=4.3×10-7,
H++HCO3- K a 1=4.3×10-7,
③HCO3-![]() H++CO32- K a2=5.6×10-11,
H++CO32- K a2=5.6×10-11,
通常情况下,海水的pH约为8,若忽略水的电离及H2CO3的第二级电离,则溶液中c(CO2)=____ mol/L。(保留两位有效数字)
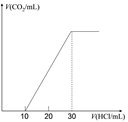
(4)为了测量某湖水中无机碳含量,量取100mL湖水,酸化后用 N2吹出CO2,再用NaOH溶液吸收。用1.0mol/L盐酸滴定吸收液,生成的V(CO2)随V(盐酸) 变化关系如左图所示,则吸收液中离子浓度由大到小的顺序为______,湖水中无机碳的浓度为___mol/L。
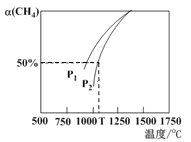
(5)用CO2和天然气可以制备CO和H2,CO2(g) +CH4(g) ![]() 2CO(g)+2H2(g)。密闭容器中浓度均为0. 1 mol/L的CH4与CO2,在一定条件下反应,测得CH4 的平衡转化率与温度及压强的关系如右图所示,则压强P1 ____P2(填“>”或“<”)。若P2= 3MPa,则T°C时该反应的平衡常数 Kp =_____MPa2
2CO(g)+2H2(g)。密闭容器中浓度均为0. 1 mol/L的CH4与CO2,在一定条件下反应,测得CH4 的平衡转化率与温度及压强的关系如右图所示,则压强P1 ____P2(填“>”或“<”)。若P2= 3MPa,则T°C时该反应的平衡常数 Kp =_____MPa2
(用平衡分压代替平衡浓度计算, 分压=总压×物质的量分数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列叙述正确的是
A. 12g石墨烯( )中含有C—C键的数目为1.5NA
)中含有C—C键的数目为1.5NA
B. 100g质量分数为17%的H2O2水溶液中含氧原子数目为0.5NA
C. 常温下,1 L0.5 mol/L NH4Cl溶液与2 L0.25 mol/L NH4Cl溶液所含NH4+的数目均为0.5 NA
D. 在KClO3+6HCl(浓) === KCl+ 3Cl2↑+3H2O反应中,每生成1 mol Cl2转移的电子数为2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在三个体积均为1 L的恒容密闭容器中发生如下反应:A(g)+2B2(g)![]() C(g)
C(g)
其中容器Ⅰ中的反应在5 min时达平衡。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
A(g) | B2(g) | C(g) | C(g) | ||
Ⅰ | 500 | 0.5 | 1.0 | 0 | 0.4 |
Ⅱ | 500 | a | b | 0.25 | 0.4 |
Ⅲ | 600 | 0.25 | 0.5 | 0.25 | 0.35 |
下列说法不正确的是
A. 容器Ⅰ中的反应在前5 min的平均反应速率v(A)=0.08 mol·L-1·min-1
B. 该反应的正反应为放热反应
C. 容器Ⅱ中起始时a=0.25,b=0.5
D. 若起始时向容器Ⅰ中加入A 0.8 mol、B2 1.6 mol,达到平衡时A的转化率为80%
查看答案和解析>>
科目: 来源: 题型:
【题目】利用甲烷和氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下图所示:

根据要求填空:
(1)写出A装置中反应的化学方程式 _____________________________ 。
(2)B装置有三种功能:________________;_______________;________________。
(3)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应_____________。
(4)在C装置中,经过一段时间的强光照射,生成的有机物有_____ 种,其中常温下以气态存在的是_________ (填写化学式)。
(5)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为___________,该装置的主要缺陷是______________________________________________________。
(6)已知丁烷与氯气的取代反应的产物之一为C4H8Cl2,其有 ________种同分异构体。
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。
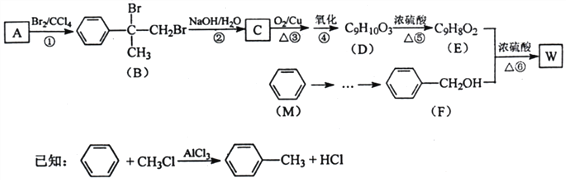
请回答下列问题:
(1)F的化学名称是_______________,①的反应类型是_______________。
(2)B中含有的官能团是_______________(写名称),
(3)D聚合生成高分子化合物的化学方程式为________________。
(4)反应③的化学方程式是___________________。
(5)芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为_________________。
(6)分子式C9H10O2的有机物,其结构中含有苯环且可以与饱和NaHCO3溶液反应放出气体的同分异构体有__________________种(不考虑立体异构)。
(7)参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线(无机试剂任选)。____________
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com