
科目: 来源: 题型:
【题目】醋酸在水中电离方程式可表示为:CH3COOH![]() CH3COO—+H+ ΔH>0,下列操作能使H+ 浓度增大的是 ( )
CH3COO—+H+ ΔH>0,下列操作能使H+ 浓度增大的是 ( )
A. 加入少量NaOH固体 B. 小心加热升温10oC C. 加入锌粉 D. 加入固体CH3COONa
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。
![]()
若A 是一种淡黄色固体单质.则C与H2O反应的生成物为______(填化学式)。
(2)Na2O2也是一种淡黄色固体,Na2O2与CO2反应生成O2和_______(填化学式)。
(3)写出在催化剂作用下N2与H2合成氨的化学方程式:_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】金属硫化物和硫酸盐在工农业生产中有广泛应用。
(1)二硫化钼(MoS2)是重要的固体润滑剂。
向体积为2L的恒容密闭容器中加入0.1molMoS2、0.2molNa2CO3,并充入0.4molH2,
发生反应:MoS2(s)+2Na2CO3(s)+4H2(g)![]() Mo(s) +2CO(g) + 4H2O(g) + 2Na2S(s) △H =akJ mol-1,测得在不同温度下达到平衡时各气体的物质的量分数如图所示。
Mo(s) +2CO(g) + 4H2O(g) + 2Na2S(s) △H =akJ mol-1,测得在不同温度下达到平衡时各气体的物质的量分数如图所示。

①a________0(填“<”“>”“=”,下同)。
②容器内的总压:P点________Q点。
③P点对应温度下,H2的平衡转化率为________,平衡常数K=________。
(2)辉铜矿(主要成分是Cu2S)在冶炼过程中会产生大量的SO2。已知冶炼过程中部分反应为:
①2Cu2S(s)+3O2(g)=2Cu2O(s)+2SO2(g) △H=-768.2kJ/mol
②2Cu2O+Cu2S(s)=6Cu(s)+SO2(g) △H=+116kJ/mol,则Cu2S与O2反应生成Cu与SO2的热化学方程式为___________________________。
(3)回收处理SO2的方法之一是用氨水将其转化为NH4HSO3。已知常温下 Kb(NH3H2O) =1.5×l0-5 Ka1(H2SO3) =1.6×l0-2 Ka2(H2SO3)=1×10-7,若吸收过程中氨水与SO2恰好完全反应,则所得溶液在常温下的pH________7(填“>”“ <”或“=”,下同),溶液中c(SO32-)________c(H2SO3)。

(4)在500℃下硫酸铵分解会得到4种产物,其含氮物质的物质的量随时间的变化如上图所示。则该条件下硫酸铵分解的化学方程式为_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,可用废镍催化剂(主要含Ni、Al,少量Cr、FeS等)来制备,其工艺流程如下:

回答下列问题:
(1)“浸泡除铝”时,发生反应的化学方程式为___________。
(2)“溶解”时放出的气体为________(填化学式)。硫酸镍溶液可用于制备合成氨的催化剂ConNi(1-n)Fe2O4。如图表示在其他条件相同时合成氨的相对初始速率随催化剂中n值变化的曲线,由图分析可知Co2+、Ni2+两种离子中催化效果更好的是________________。

(3)“氧化”时,酸性条件下,溶液中的Fe2+被氧化为Fe3+,其离子方程式为。
(4)已知该条件下金属离子开始沉淀和完全沉淀的pH如下表:
开始沉淀的pH | 完全沉淀的pH | |
Ni2+ | 6.2 | 8.6 |
Fe2+ | 7.6 | 9.1 |
Fe3+ | 2.3 | 3.3 |
Cr3+ | 4.5 | 5.6 |
“调pH1”时,溶液pH范围为________;过滤2所得滤渣的成分________(填化学式)。
(5)写出在空气中加热Ni(OH)2制取NiOOH的化学方程式________________。
(6)含镍金属氢化物MH-Ni燃料电池是一种绿色环保电池,广泛应用于电动汽车。其中M代表储氢合金,MH代表金属氢化物,电解质溶液可以是KOH水溶液。它的充、放电反应为:xNi(OH)2+M![]() MHx+xNiOOH;电池充电过程中阳极的电极反应式为________;放电时负极的电极反应式为________。
MHx+xNiOOH;电池充电过程中阳极的电极反应式为________;放电时负极的电极反应式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】“酒是陈的香”是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:

(1)装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是_______。
(2)该反应属于______(选字母,可多选)。
A.加成反应 B.取代反应 C.水解反应 D.酯化反应
(3)写出上述制取乙酸乙酯反应的化学反应方程式:________________。
(4)乙醇在一定条件下还能发生脱水反应产生乙烯。乙烯通入溴的四氯化碳溶液中,观察到的现象是__________;其反应方程式为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】浓度均为0.1 mol / L的①NaHCO3、②Na2CO3、③NaCl、④NaHSO4四种溶液,按pH值由小到大排列的顺序是
A. ①②③④ B.④③①② C.③④①② D.②①④③
查看答案和解析>>
科目: 来源: 题型:
【题目】法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖。轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是( )

A. 该化合物的名称为乙酸乙酯
B. 该化合物既能发生水解反应,又能发生氧化反应
C. 该化合物与Br2的四氯化碳溶液不反应
D. 该化合物的同分异构体中,能与NaHCO3反应放出CO2的只有2种
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:T℃时,Ksp(CaSO4)=4.90×10-5、Ksp(CaCO3)=2.8×10-9、Ksp(PbCO3)=8.4×10-14,三种盐的沉淀溶解平衡曲线如图所示,pM=-lgc(阴离子)、pN=-lgc(阳离子)。下列说法正确的是( )
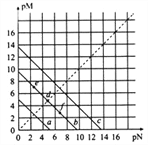
A. a线代表的是PbCO3
B. T℃时,向10 mL水中加入CaCO3和PbCO3至二者均饱和,溶液中c(Ca2+)∶c(Pb2+)=3×10-5
C. d点可以代表CaCO3的饱和溶液,且c(Ca2+)= c(CO32-)
D. T℃时,向CaCO3悬浊液中加入NH4Cl固体,会使图象中d点向f点转化
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 31g白磷(![]() )分子中含有1 NA 个P-P键
)分子中含有1 NA 个P-P键
B. 1molFeI2与1molCl2反应时转移的电子数为3NA
C. 标准状况下,4.48LCH4和乙烯(CH2=CH2)的混合气体完全燃烧,产生的水中所含O-H键数目为0.8NA
D. 常温下,将1 mol NH4NO3溶于稀氨水中使溶液呈中性,溶液中NH4+数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com