
科目: 来源: 题型:
【题目】下列操作不影响测定1mol氢气体积的实验结果的是
A.操作中漏气
B.镁带称量后,用砂皮擦去表面氧化层
C.硫酸稍过量
D.读取液体量瓶的体积读数作为氢气的体积
查看答案和解析>>
科目: 来源: 题型:
【题目】非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:

请回答下列问题
(1)有机化合物B中的含氧官能团为__________和__________(填名称)。
(2)上述反应中,过程②属于__________反应,过程④属于__________反应。
(3)若过程①发生的是取代反应,且另一种产物有HBr,写出由A到B发生反应的化学方程式__________________。
(4)非诺洛芬的一种同分异构体满足下列条件:
Ⅰ.能与NaHCO3反应放出CO2,能与 FeCl3溶液发生显色反应。
Ⅱ.分子中有6 种不同化学环境的氢,且分子中含有两个苯环。
写出符合条件的一种同分异构体的结构简式:________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】F(4-苯并呋喃乙酸)是合成神经保护剂依那朵林的中间体,某种合成路线如下:
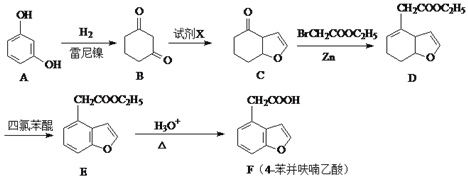
(1)化合物F中的含氧官能团为_________和___________(填官能团的名称)
(2)试剂X分子式为C2H3OCl,分子中既无甲基也无环状结构且可发生银镜反应,则X的结构简式为__________;由E→F的反应类型为___________。
(3)写出同时满足下列条件的E的一种同分异构体的结构简式____________。
Ⅰ. 能发生银镜反应 Ⅱ. 分子中含有1个苯环且有3种不同化学环境的氢
(4)借鉴由C到D的合成机理,请写出以![]() 和BrCH2COOC2H5为原料制备
和BrCH2COOC2H5为原料制备![]() 的合成路线流程图(无机试剂可任选)_____。
的合成路线流程图(无机试剂可任选)_____。
合成路线流程图示例如下:CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目: 来源: 题型:
【题目】【化学—选修3:物质结构与性质】
钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:

回答下列问题:
(1)基态钛原子的价电子排布图为 ,其原子核外共有 种运动状态不相同的电子。金属钛晶胞如下图1所示,为 堆积(填堆积方式)。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l-l >> l-b > b-b(l为孤对电子对,b为键合电子对),则关于H2O中的H-O-H键角可得出的结论是________。
A.180° | B.接近120°,但小于120° |
C.接近120°,但大于120° | D.接近109°28’,但小于109°28’ |
(3)已知TiCl4在通常情况下是无色液体,熔点为–37℃,沸点为136℃,可知TiCl4为________晶体。
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下图2。化合物乙的沸点明显高于化合物甲,主要原因是 。化合物乙中采取sp3杂化的原子的第一电离能由大到小的顺序为 。

(5)钙钛矿晶体的结构如右图所示。钛离子位于立方晶胞的角顶,被 个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被 个氧离子包围。钙钛矿晶体的化学式为 。若该晶胞的边长为a pm,则钙钛矿晶体的密度为 g.cm-3(只要求列算式,不必计算出数值)。

查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数,下列叙述正确的是
A. lmolO2作为氧化剂得到的电子数一定为4NA
B. 标准状况下,40gSO3所占的体积一定小于11.2L
C. 0.4mol/LNa2SO4溶液中,所含Na+和SO42-总数为1.2NA
D. 在标准状况下,0.1molFe粉在少量氯气中燃烧转移电子数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】霾天气严重影响人们的生活,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一。消除氮氧化物和硫氧化物有多种方法。
(1)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)![]() N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间(min) 浓度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0~10 min内,NO的平均反应速率v(NO)=_______________________,T1℃时,该反应的平衡常数K=____________。
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是_______(填字母)。
a.升高温度 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30 min后升高温度至T2℃,达到平衡时,容器中,NO、N2、CO2的浓度之比为5:3:3,则Q__________(填“>”、“=”或“<”)0。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
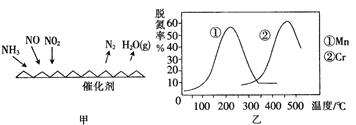
①由图甲可知,SCR技术中的氧化剂为_______________。已知c(NO2):c(NO)=1:1时脱氮效果最佳, 若生成1 mol N2时反应放出的热量为Q kJ。此时对应的脱氮反应的热化学方程式为__________________________
②图乙是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳的催化剂和相应温度分别为___________________________。
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液。已知常温下Ka1(H2SO3)=1.8×10-2 , Ka2(H2SO3)=6.0×10-9。常温下,测得某纯CaSO3与水形成的浊液pH=9,忽略SO32-的第二步水解,则Ksp(CaSO3)=____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求完成下列化学方程式或离子方程式。
(1)工业用电解饱和食盐水制氯气的化学方程式为____________________。
(2)向新制的Na2S 溶液中滴加新制的氯水的离子方程式为_______________。
(3)氯化铝与过量NaOH 溶液反应的离子方程式为____________________。
(4)乙醇催化氧化制乙醛的化学方程式为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】可充电“钠·二氧化碳”电池(如图),电池总反应为:4Na+3CO2![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,Na+向正极移动
B. 放电时,电子从钠薄经负载流向多壁纳米碳管
C. 充电时,钠薄和外接电源的负极相连,发生氧化反应
D. 充电时,阳极的电极反应为:2Na2CO3+C-4e-=4Na++3CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com