
科目: 来源: 题型:
【题目】闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质。软锰矿的主要成分为 MnO2;含少量A12O3和SiO2。现以闪锌矿和软猛矿为原料制备Zn和MnO2,其简化流程如下(中间产物的固体部分已经略去)。

已知:I.矿石中所有金属元素在滤液中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
Zn2+ | Mn2+ | Fe2+ | Fe,3+ | Al3+ | |
pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
回答下列问题:
(1)步骤①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式________________________________。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是_______________。
(3)步骤③与MnO2发生氧化还原反应的离子方程式_________________,物质X可以是__________(用字母表示。
A.Cu2(OH)2CO3 B.MnCO3 C. MgO D.Zn(OH)2
(4)流程中可以循环利用的物质是____________(填化学式)。
(5)MnO2与Li构成LiMnO2,该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。回答下列问题:

①外电路中的电子移动方向是由______极流向______极(填字母)。
②写出该锂离子电池的正极电极反应式_____________________________。
(6)已知:25℃时,HCN的电离常数K=4.9×10-10, H2S的电离常数K1=1.3×10-7 ,K2=7.0 ×10 -15,向NaCN溶液中通入少量的H2S气体,该反应的化学方程式为______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】分别由短周期元素m、n、p、q组成的单质依次为甲、乙、丙、丁,有关反应关系如图所示(部分产物省略)。其中甲为黄绿色气体,M、N均为10电子分子且M的水溶液呈碱性,Q为离子化合物,下列说法中正确的是

A. 原子半径的大小m>q>n>p
B. 元素非金属性q>n>p
C. Q的溶液可以保存在细口玻璃试剂瓶
D. n的氧化物的水化物一定为强酸
查看答案和解析>>
科目: 来源: 题型:
【题目】将氯气通过软管通入鼠洞中,可以用来消灭田鼠。在此过程中利用了氯气下列性质中的
①黄绿色 ②密度比空气大 ③有毒 ④易液化 ⑤溶于水 ( )
A. ①②③ B. ②③
C. ③④ D. ③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】利用硫酸钾、硫酸镁、硫酸铝三种溶液分别与相同体积、相同浓度的氯化钡溶液反应使Ba2+恰好完全沉淀,需要三种溶液的体积比为3∶2∶2,则三种溶液的溶质的物质的量浓度之比为( )
A. 3∶4∶2 B. 2∶3∶3 C. 6∶3∶1 D. 2∶3∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】电解质溶液电导率越大导电能力越强.常温下用0.100mol·L-1盐酸分别滴定10.00mL浓度均为0.100mol·L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氮相似,常温Kb[(CH3)2NH]=1.6×10-4。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
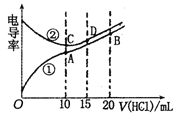
A. 曲线②代表滴定二甲胺溶液的曲线
B. A点溶液中:c(H+)=c(OH-)+c[(CH3)2NH·H2O]
C. D点溶液中:2c(Na+)=3c(Cl-)
D. 在相同温度下,A、B、C、D四点的溶液中,水的电离程度最大的是C点
查看答案和解析>>
科目: 来源: 题型:
【题目】以A、B为原料制备现行高分子化合物M和抗凝血药物N的一种路线如下(部分反应条件和试剂略去)

已知:Ⅰ.烃A的密度是相同条件下H2密度的14倍;
Ⅱ. ![]() ;
;
Ⅲ. ![]() 。
。
(1)A中含有的官能团的结构简式为____。B的名称为____。
(2)F的结构简式为____________。N中含氧官能团的名称为________。
(3)I的核磁共振氢谱有____组吸收峰。G分子最多有______个原子共平面。
(4)同时满足下列条件的J的同分异构体有_________种。
①苯环上连有两个取代基 ②1mol该物质于足量的NaHCO3反应,生成2molCO2
(5)参照上述信息和合成路线,以![]() 为起始原料(其他无机试剂任选),补充完整制备
为起始原料(其他无机试剂任选),补充完整制备![]() 的合成路线:___________________
的合成路线:___________________
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,电流表G的指针发生偏转,同时A极质量增加,B极质量减少,C为电解质溶液。则A、B、C分别可能为
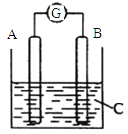
A.A是Zn,B是Cu,C是稀硫酸
B.A是Cu,B是Zn,C是稀硫酸
C.A是Fe,B是Ag,C是AgNO3稀溶液
D.A是Ag,B是Fe,C是AgNO3稀溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室欲用NaOH固体配制1.0 mol·L1的NaOH溶液240 mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④倒转摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却
其正确的操作顺序为________________。本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、还有________。
(2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图。烧杯的实际质量为____________ g,要完成本实验该同学应称出____________ g NaOH。

(3)使用容量瓶前必须进行的一步操作是________。
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是________。
①没有洗涤烧杯和玻璃棒
②转移溶液时不慎有少量洒到容量瓶外面
③容量瓶不干燥,含有少量蒸馏水
④定容时俯视刻度线
⑤未冷却到室温就将溶液转移到容量瓶并定容
⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于甲、乙、丙、丁四个图像的说法中,不正确的是

A. 若用甲表示某可逆反应的能量变化,说明催化剂能改变正、逆反应的活化能
B. 图乙表示在含Mg2+、Al3+、NH4+、Cl-的溶液中,加入一定浓度NaOH溶液时生成沉淀的图像,由图可得原溶液中,n(Mg2+):n(Al3+):n(NH4+)=10:2:3
C. 图丙表示MOH和ROH两种一元酸的溶液分别加水稀释时的pH变化,由图可得碱性:ROH>MOH
D. 图丁表示某温度时,BaSO4在水中的沉淀溶解平衡曲线,则加入Na2SO4可以使溶液由a点变到b点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com