
科目: 来源: 题型:
【题目】符合如图所示的转化关系,且当X、Y、Z的物质的量相等时,存在焓变ΔH=ΔH1+ΔH2。满足上述条件的X、Y可能是

①C、CO ②S、SO3 ③Na、Na2O
④AlCl3、Al(OH)3 ⑤Fe、Fe(NO3)2 ⑥NaOH、Na2CO3
A.①④⑤ B.①②③ C.①③④ D.①③④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】电解饱和食盐水可产生氯气、氢气和氢氧化钠,氯气与石灰乳反应可制漂白粉.
(1)请写出电解饱和食盐水的化学方程式.
(2)若电解饱和食盐水时消耗NaCl 58.5克,试计算理论上最多可得到氯气的体积(标准状况)?
(3)若将1mol氯气通入石灰乳中,理论上可得到次氯酸钙多少克?
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH= 99 kJ/mol。
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH= 99 kJ/mol。

请回答下列问题:
①图中A点表示: 。
C点表示: 。
E的大小对该反应的反应热 (填“有”或“无”)影响。
②图中ΔH = kJ/mol。
(2)由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量(25℃、101 kPa下测得)
①写出该反应的热化学方程式: 。
②若1 mol水蒸气转化为液态水放热45kJ,则反应H2(g)+![]() O2(g)
O2(g)![]() H2O( l )的ΔH = kJ/mol。氢气的燃烧热为ΔH = kJ/mol。
H2O( l )的ΔH = kJ/mol。氢气的燃烧热为ΔH = kJ/mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】醋酸和氢氧化钠溶液发生反应的离子方程式正确的是 ( )
A. H++OH-→H2O
B. H++ NaOH→Na++H2O
C. CH3COOH +OH-→CH3COO- +H2O
D. CH3COOH + NaOH→CH3COO-+ Na++H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨工业的核心反应:N2(g)+3H2(g)![]() 2NH3(g)的反应过程中能量变化如图所示,回答下列问题:
2NH3(g)的反应过程中能量变化如图所示,回答下列问题:

(1)ΔH=______;在反应体系中加入催化剂,反应速率增大,E2的变化是______(填“增大”“减小”或“不变”);△H (填“增大”“减小”或“不变”)。
(2)在500℃、2×107 Pa和催化剂条件下向一密闭容器中充入0.5 mol N2和1.5 mol H2,充分反应后,放出的热量_______(填“<”“>”或“=”)46.2 kJ,理由__________________________________。
(3)已知在25℃、101 kPa时,14克CO气体完全燃烧放出热量为Q kJ。
请写出CO燃烧热的热化学方程式:______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醛是一种重要的化工产品,可利用甲醇催化脱氢制备。甲醛与气态甲醇转化的能量关系如图所示。
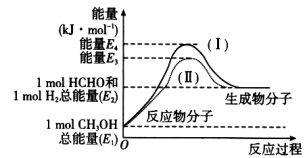
反应过程中的能量关系
(1)甲醇催化脱氢转化为甲醛的反应是_______(填“吸热”或“放热”)反应。
(2)过程Ⅰ与过程Ⅱ的反应热是否相同?_______,原因是___________________________________。
(3)写出甲醇催化脱氢转化为甲醛的热化学方程式:____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】运用盖斯定律可方便地计算出难以通过实验直接测定的反应热。
已知:①P4(白磷,s)+5O2(g)![]() P4O10(s) ΔH=2 983.2 kJ·mol1
P4O10(s) ΔH=2 983.2 kJ·mol1
②P(红磷,s)+![]() O2(g)
O2(g)![]()
![]() P4O10(s) ΔH=738.5 kJ·mol1
P4O10(s) ΔH=738.5 kJ·mol1
则白磷转化为红磷的热化学方程式为
A.P4(白磷,s)![]() 4P(红磷,s) ΔH=29.2 kJ·mol1
4P(红磷,s) ΔH=29.2 kJ·mol1
B.P4(白磷,s)![]() 4P(红磷,s) ΔH=+29.2 kJ·mol1
4P(红磷,s) ΔH=+29.2 kJ·mol1
C.P4(白磷,s)![]() 4P(红磷,s) ΔH=2 244.7 kJ·mol1
4P(红磷,s) ΔH=2 244.7 kJ·mol1
D.P4(白磷,s)![]() 4P(红磷,s) ΔH=+2244.7 kJ·mol1
4P(红磷,s) ΔH=+2244.7 kJ·mol1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com