
科目: 来源: 题型:
【题目】在某澄清溶液中,可能存在下列几种离子:H+、K+、Ba2+、SO42-、I-、CO32-。取该溶液进行下列实验:
①用pH试纸检验,该溶液呈强酸性;
②取20mL溶液加入少量氯水和少量CCl4振荡后静置,CCl4层呈紫色;
③另取部分溶液逐滴加入NaOH溶液当溶液是碱性时,再加入Na2CO3溶液,有白色沉淀生成。
(1)根据上述实验现象、推断原溶液中肯定在的离子是________,肯定不存在的离子是_____,可能存在的离子是________。
(2)若步骤②中消耗0.01molCl2,则溶液中与Cl2反应的离子的物质的量浓度为_________。
(3)写出实验③中生成白色沉淀的离子方程式_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某强酸性溶液X,可能含有Al3+、Ba2+、NH4+、Fe2+、Fe3+、CO32-、SO42-、SiO32-、NO3-中的一种或几种离子,取该溶液进行实验,其现象及转化如下图。反应过程中有一种气体是红棕色。请回答下列问题:

(1)由强酸性条件即可判断溶液X中一定不存在的离子有 。
(2)溶液X中,关于NO3-的判断一定正确的是_ ___。
a.一定有 b.一定没有 c.可能有
(3)产生气体A的离子方程式为 。
(4)转化⑥发生反应的现象为 。
(5)转化④中产生H的离子方程式为 。
(6)若转化③中,D、H2O、O2三种物质恰好发生化合反应生成E,则反应中D与O2的物质的量之比为____。
(7)对不能确定是否存在的离子,可以另取X溶液,加入下列溶液中的一种,根据现象即可判断,该试剂最好是 。
①NaOH溶液,②KSCN溶液,③石蕊试剂,④pH试纸,⑤KMnO4溶液,⑥氯水和KSCN的混合溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E、G、H、I均为气体,G可使湿润红色石蕊试纸变蓝,J为常见的液态物质,A、B、C、I、M为单质,且M为常见金属,G和H相遇时产生白烟,它们存在如图的转化关系(图中部分反应物或产物已省略),请回答有关问题:
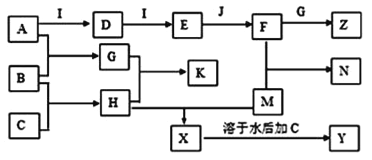
(1)请写出:A物质的化学式:___;
(2)①写出实验室用K制取G的化学方程式_______;
②实验室检验气体G是否收集满的方法:__________;
③G与H相遇可生成白烟K,请写出该反应的化学方程式______.
(3)①F的浓溶液与木炭反应的化学方程式为____________;
②工业F的浓溶液呈黄色,试用化学方程式解释原因:_________;若要消除黄色可向其中通入一定量的_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】I.现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量。量筒的规格为1000 mL,供选择的电极材料有纯铜片和纯锌片。请回答下列问题:
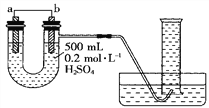
(1)b电极材料为__________,其电极反应式为_________________________。
(2)当量筒中收集到672 mL(标准状况下)气体时,通过导线的电子的物质的量为__________,此时a电极质量减少__________g。
II.某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的离子方程式有:_____________________________________________;
(2)硫酸铜溶液可以加快氢气生成速率的原因是_________________________________________;
(3)要加快上述实验中气体产生的速率,还可采取的措施有_____________________(答两种);
查看答案和解析>>
科目: 来源: 题型:
【题目】元素及其化合物的知识是高中化学重要的组成部分,是考查化学基本概念和理论、化学计算、化学实验知识的载体。
(1)元素周期表1-20号元素中,某两种元素的原子序数相差3,周期数相差1。
①这样的两种元素的组合有________种。
②若这样的两种元素形成的化合物中原子数之比为1∶1。
写出其中一种化合物的名称:_______________________;
(2)A是自然界存在最广泛的ⅡA族元素,常以化合物F存在.从单质A起始发生的一系列化学反应可由下图表示:
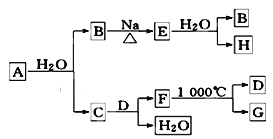
请回答下列问题:
①F的化学式为________,D的电子式为________________。
②E与水反应的化学方程式为___________________________________________;
③实际生产中,可由F为原料制备单质A,写出制备过程的化学方程式(不需考虑综合经济效益)_______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关防止或减少酸雨的措施中不可行的是( )
A. 对燃煤及燃煤烟气进行脱硫
B. 推广天然气、甲醇等作为汽车的燃料
C. 对含SO2、NO2的废气处理后再排空
D. 人工收集大气雷电产生的氮的氧化物
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸盐在能源、环保等方面有着广泛的用途。湿法、干法制备高铁酸盐的原理如下表所示。
湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如下图所示:

①反应I的化学方程式为 。
②反应II的离子方程式为 。
③进行溶解,沉淀、洗涤这些操作的共同目的是 。
(2)高铁酸钾是一种理想的水处理剂,其处理水的原理为________________。
(3)湿法、干法制备K2FeO4的反应中均利用的是+3价Fe元素的 性质。
(4)高铁电池是正在研制中的可充电干电池,下图为该电池和常用的高能碱性电池的放电曲线,由此可得出的高铁电池的优点有 。

查看答案和解析>>
科目: 来源: 题型:
【题目】某同学进行有关铜、硝酸、硫酸化学性质的实验,实验过程如图所示:

下列说法正确的是
A. ①中溶液呈蓝色,试管口有红棕色气体产生,稀硝酸被还原为NO2
B. ②中溶液存在:c(Cu2+) + c(H+) = c(NO3-) + c(OH-)
C. 由上述实验得出结论:常温下,Cu既可与稀硝酸反应,也可与稀硫酸反应
D. ③中反应的化学方程式:3Cu+Cu(NO3)2+4H2SO4 === 4CuSO4 +2NO↑+4H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃气体。而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊。D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体。
请回答下列问题:
(1)写出A、B、C、D、E、F的化学式
A________;B________;C________;D________;E________;F________。
(2)写出F和H反应的化学方程式 __________________________________。
(3)写出下列反应的离子方程式:
①D+盐酸 ________________________________________________;
②B+水 _____________________________________________________;
③D+A ______________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是( )

A. 在0-a范围内,只发生中和反应
B. ab段发生反应的离子方程式为:CO32-+2H+=H2O+CO2↑
C. a=0.3
D. 原混合溶液中NaOH与Na2CO3的物质的量之比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com