
科目: 来源: 题型:
【题目】在通风橱中进行下列实验:
步骤 |
|
| |
现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是( )
A. Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2═2NO2
B. Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C. 对此Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D. 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】已知1mol白磷完全转化为红磷放出29.2kJ热量,且P4(白,s)+5O2(g)=2P2O5(s)放出热量为Q1,4P(红,s)+5O2(g)=2P2O5(s)放出的热量为Q2,则Q1和Q2的关系为
A. Q1>Q2 B. Q12 C. Q1=Q2 D. 无法判断
查看答案和解析>>
科目: 来源: 题型:
【题目】使用化学手段可以消除某些环境污染。下列主要依靠化学手段消除环境污染的是( )
A. 在燃煤中添加生石灰
B. 将某些废旧塑料熔化后再成型
C. 把放射性核废料深埋于地下岩层
D. 用多孔吸附剂清除水面油污
查看答案和解析>>
科目: 来源: 题型:
【题目】一种可利用含碘废水制取KI的实验流程如下:

回答下列问题:
(1)含碘废水中碘的存在形式一般有I2、I-。检验是否含I2及I-的方法是用CCl4萃取后观察萃取液为紫色,证明含有I2,反复萃取后取水层少许于试管中,_____________。
(2)“制CuI”时,I2被还原为CuI,同时有S4O62-生成。
①该反应的离子方程式为_________________________________________________。
②已知上述反应的平衡常数为1.78×1026,实验中需控制CuSO4过量2%,其目的是_________________。
(3)“制FeI2溶液”的化学方程式为____________________________________;“滤渣3”的成分是________________(填化学式)。
(4)用HI调节溶液pH约为6,其目的是_____________________________________。
(5)准确称取产品0.1000g溶于50mL水,加入适量乙酸并加入曙红钠指示剂,然后用0.025mol·L-1AgNO3溶液滴定,至终点时消耗AgNO3溶液22.00mL,则产品中KI的质量分数为____________(保留三位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于化学反应速率和化学反应限度的说法中正确的是( )
A.化学反应速率是衡量化学反应进行快慢程度的物理量
B.化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示
C.当一个可逆反应达到平衡状态时,这就是这个反应所能达到的限度,即使条件改变,该限度都不会改变
D.平衡状态是一种静止的状态,因为反应物和生成物的浓度已经不再改变
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述不正确的是
A. 金属腐蚀的本质是金属原子失去电子而被氧化
B. 钢铁吸氧腐蚀的正极反应是:O2+4e-+2H2O=4OH-
C. 氢氧燃料电池中,氢气在负极发生氧化反应
D. 将地下钢管与直流电源的正极相连,用来保护钢管
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.O2和O3互为同位素
B.X的气态氢化物的化学式为H2X,则X的最高价氧化物的水化物的化学式为H3XO4
C.HCl的形成过程用电子式表示为 ![]()
D.铝与稀盐酸的反应既是氧化还原反应,又是放热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途,某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(l)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化,再向试管中通入空气,溶液逐渐变红。由此可知:①样品中没有Fe3+、②_______。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。
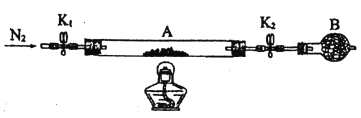
①将下列实验操作步骤正确排序_______(填标号):重复上述操作步骤,直至A恒重,记为m3g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却到室温
②根据实验记录,计算绿矾化学式中结晶水数目x=_______(列式表示)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为_______(填标号)。
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.液H2SO4
②写出硫酸亚铁高温分解反应的化学方程式__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】2013年,“雾霾”成为年度关键词。近年来,对“雾霾”的防护与治理成为越来越重要的环境问题和社会问题:雾霾主要由二氧化硫、氮氧化物和可吸入颗粒物这三项组成。
(I)燃煤尾气中的SO2用NaOH溶液吸收形成NaHSO3溶液,在pH为4-7之间时电解,硫元素在铅阴极上被电解还原为Na2S2O4。Na2S2O4俗称保险粉,广泛应用子染料、印染、造纸、食品工业以及医学上。这种技术是最初的电化学脱硫技术之一。请写出该电解反应中阴极的电极方程式:____________。
(2)SO2经过净化后与空气混合进行催化氧化后制取硫酸我者硫酸铵,其中SO2发生催化氧化的反应为:2 SO2 (g)+ O2(g)![]() 2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示:
2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示:
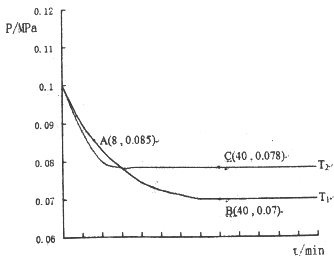
①图中A点时,SO2的转化率为____________。
②计算SO2催化氧化反应在图中B点的压强平衡常数K=_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
③若在T2℃,其他条件不变的情况下测得压强的变化曲线如图所示,则Tl__T2(填“>”、“<”、“=”);其中C点的正反应速率vc(正)与A点的逆反应速率VA(逆)的大小关系为vc(正)____VA(逆)(填“>”、“<”、“=”)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知25℃时,Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.3×10-17,将AgCl与AgI的饱和溶液等体积混合,再向混合液中加入足量的浓硝酸银溶液,充分反应,下列说法正确的是 ( )
A.混合液中只有AgI沉淀生成
B.混合液中生成AgI沉淀少于AgCl沉淀
C.常温下,AgCl在NaCl溶液中的溶解度与在纯水中的溶解度相同
D.常温下,AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com