
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列的字母分别表示一种化学元素。

(1)下列 ______(填写编号)组元素可能都是电的良导体。
①a、c、h ②b、g、k ③c、h、l ④d、e、f
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去。核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
A、原子核对核外电子的吸引力;B、形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(KJ/mol):
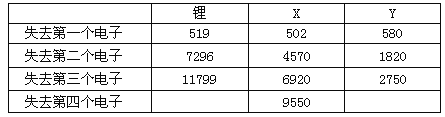
①表中X可能为以上13种元素中的________________(用化学用语表达)元素。用元素符号表示X和j形成化合物的化学式___________________;Y是周期表中_____________族元素。
②以上13种元素中,__________(用化学用语表达)元素原子失去核外第一个电子需要的能量最多。
③通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量:_________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】固体聚合硫酸铁(SPFS)是一种重要的无机高分子絮凝剂,极易溶于水,其化学组成可表示为Fex(OH)y(SO4)znH2O。
Ⅰ.SPFS的工业制备:
用绿矾(FeSO4·7H2O)与NaClO3溶液在酸性介质中充分反应,经水解、聚合、减压蒸发可得到聚合硫酸铁
Ⅱ.SPFS的组成测定:
取8.19g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得到9.32g白色沉淀;向滤液中加入NH3·H2O,调节溶液pH=6,经过滤、洗涤、干燥、灼烧得到4.00 g固体Fe2O3。
(1)从FeSO4溶液中得到绿矾的实验操作为 ___________________________。
(2)Ⅰ中绿矾与NaClO3溶液反应的离子方程式为______________________。
(3)Ⅱ中当溶液pH=6时,c(Fe3+)=_______。(已知:Ksp[Fe (OH) 3]=4.0×10-38)
(4)该SPFS的化学式为______________(写出计算过程)。
查看答案和解析>>
科目: 来源: 题型:
【题目】水热法制备纳米颗粒Y(化合物)的反应为3Fe2++2S2O32-+O2+aOH-=Y+S4O62-+2H2O,下列说法中,不正确的是
A.a = 4B.Y的化学式为Fe2O3
C.S2O32-是还原剂D.每有1molO2参加反应,转移的电子总数为4mol
查看答案和解析>>
科目: 来源: 题型:
【题目】表为元素周期表的一部分.
族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
一 | ① | |||||||
二 | ② | ③ | ④ | ⑤ | ⑥ | |||
三 | ⑦ | ⑧ | ⑨ | ⑩ | ||||
四 | ||||||||
(1)表中元素的非金属性最强;元素的金属性最强;元素的单质室温下呈液态(填写元素符号);
(2)表中元素⑦的原子结构示意图为
(3)表中元素⑥⑩氢化物的稳定性顺序为>(填写化学式,下同);
(4)表中元素⑩和最高价氧化物对应水化物的酸性:> .
(5)表中元素②和⑦最高价氧化物对应水化物的碱性> .
查看答案和解析>>
科目: 来源: 题型:
【题目】A,B,C为短周期元素,在周期表中所处的位置如表所示.
A | C | |
B |
A、C两元素的原子核外电子数之和等于B原子的质子数.
(1)写出B,C元素的名称、 .
(2)B位于元素周期表中第周期第族.
(3)用石墨为电极,电解B元素的最高价氧化物的水化物的水溶液,当电路中转移0.4mol电子时,在阴极收集到的产物是 , 质量为g,电解的总反应方程式为;
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式 .
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列各溶液的叙述中正确的是( )
A. NaHSO3与Na2SO3混合溶液中一定存在如下关系:2c(Na+)=3(c(HSO3﹣)+c(SO32﹣)+c(H2SO3))
B. 向0.1molL﹣1的醋酸钠溶液中滴加0.1molL﹣1盐酸至中性,所得溶液中:c (Na+)>c (CH3COO﹣)>c (Cl﹣)=c (CH3COOH)>c(H+)=c(OH﹣)
C. 等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:c(Na+)=c(SO42﹣)>c(NH4+)>c(H+)>c(OH﹣)
D. 向1.00 L 0.3molL﹣1NaOH溶液中缓慢通入0.2molCO2气体,溶液中:c(Na+)>c(CO32﹣)>c(HCO3﹣)>c(OH﹣)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( ) 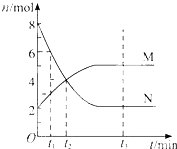
A.反应的化学方程式为:2MN
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com