
科目: 来源: 题型:
【题目】25 ℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq) ![]() Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
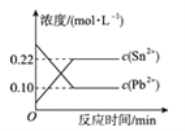
A. 往平衡体系中加入金属铅后,c(Pb2+)增大
B. 升高温度,平衡体系中c(Pb2+)增大,说明该反应ΔH>0
C. 25 ℃时,该反应的平衡常数K=2.2
D. 往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
查看答案和解析>>
科目: 来源: 题型:
【题目】下列推断正确的是
A. pH=6.5的溶液一定显酸性
B. 0.1mol L-1的Na2CO3溶液中:c(CO32-)+c(HCO3-)=0.1mol L-1
C. 常温下,等体积的0.2 mol L-1的盐酸与0.2 mol L-1的氢氧化钡溶液混合,所得溶液的pH=13
D. 常温下,某溶液中水电离出的c(OH-)=l×10-12 mol L-1,该溶液pH 一定等于2
查看答案和解析>>
科目: 来源: 题型:
【题目】为了测定实验室长期存放的Na2SO3固体的纯度,准确称取W g固体样品,配成250 mL溶液。设计了以下两种实验方案:
方案I:取25.00 mL上述溶液,加入过量的盐酸酸化的BaCl2溶液,过滤、洗涤和干燥沉淀,称得沉淀的质量为m1 g 。
方案Ⅱ:取25.00 mL上述溶液,加入过量的硝酸酸化的Ba(NO3)2溶液,过滤、洗涤和干燥沉淀,称重,其质量为m2 g 。
(1)准确配制250 mL Na2SO3溶液时,必须用到的实验仪器有:天平、烧杯、玻棒、胶头滴管、药匙和____________。
(2)写出Na2SO3固体氧化变质的化学方程式_____________________________________。
(3)方案I加入过量的盐酸酸化的BaCl2溶液,如何检验是否沉淀完全,其操作是_____________。
(4)方案I中,若滤液浑浊,将导致测定结果________(选填“偏高”或“偏低”)。
(5)由方案I :Na2SO3固体的纯度可表示为:___________。
(6)方案I、方案Ⅱ :m1________m2(填“>”、“<”或“=”)。
(7)取25.00 mL上述溶液,用滴定的方法测定Na2SO3的纯度。下列试剂可作为标准溶液进行滴定的是________。滴定终点的现象为________________________________。
A.酸性KMnO4溶液 B.H2O2溶液 C.Br2水 D.FeCl3溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度时,在2L容器中A,B两种物质间的转化反应中,A,B物质的量随时间变化的曲线如图所示,由图中数据分析得: 
(1)该反应的化学方程式为
(2)反应开始至4min时,A的平均反应速率为 .
(3)4min时,反应是否达到平衡状态?(填“是”或“否”), 8min时,v(正)v(逆)(填“>”、“<”或“=”).
查看答案和解析>>
科目: 来源: 题型:
【题目】下列能正确表示水解的离子方程式是( )
A. CH3COOH + H2O ![]() CH3COO- + H3O+
CH3COO- + H3O+
B. Br- + H2O ![]() HBr + OH-
HBr + OH-
C. CO32- + 2H2O![]() H2CO3 + 2OH-
H2CO3 + 2OH-
D. NH4+ + H2O ![]() NH3·H2O + H+
NH3·H2O + H+
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D是四种短周期元素,E是过渡元素.A、B、C同周期,C、D同主族,A的原子结构示意图为:![]() ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E元素的正三价离子的3d亚层为半充满.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E元素的正三价离子的3d亚层为半充满.回答下列问题:
(1)写出下列元素的名称:A________, B________, C________,D________。
(2)用元素符号表示D所在周期第一电离能最大的元素是__________,电负性最大的元素是__________。
(3)D的氢化物比C的氢化物的沸点__________(填“高“或“低“),原因__________。
(4)E元素的正三价离子的电子排布式为________________________。E元素在周期表中的位置是_________。
(5)用电子式表示B的硫化物的形成过程:_____________________________________。
(6)写出A的最高价氧化物与B的最高价氧化物的水化物反应的离子方程式________。
查看答案和解析>>
科目: 来源: 题型:
【题目】温度T℃时,在3个相同的恒容密闭容器中发生:CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
△H =-41kJ·mol—1,其起始时投料的方式、各物质的量及其达平衡过程体系热量的变化如下表所示:
容器编号 | 起始时各物质物质的量/mol | 达平衡过程体系热量的变化(均为正值) | |||
CO | H2O(g) | CO2 | H2 | ||
① | 1 | 4 | 0 | 0 | 32.8 kJ |
② | 8 | 2 | 0 | 0 | Q1 |
③ | 0 | 0 | 1 | 4 | Q2 |
下列说法中正确的是
A. 若经过10s容器①中反应达到平衡,则v(CO)=0.08 molL-1s-1
B. 容器②和容器③中热量变化:Q2=Q1=32.8 kJ
C. 若加入催化剂,改变了该反应的途径,反应的△H也随之改变
D. 保持相同条件,向平衡后的容器①中再加入0.1molCO 和0.4molCO2 (g),则平衡不发生改变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com