
科目: 来源: 题型:
【题目】完成下列各问题:
(1)①泡沫灭火器中的药品为NaHCO3和Al2(SO4)3,其反应的离子方程式为:__________;
②TiCl4水解生成TiO2·xH2O的化学方程式__________;
③酸性高锰酸钾溶液与草酸溶液反应的化学方程式____________;
④硫代硫酸钠溶液与稀硫酸反应的化学万式____________;
(2)碳酸氢钠溶液中的粒子物质的量浓度有多种关系,请分别写出
①电荷数守恒_________;
②物料守恒___________;
③质子守恒___________;
④下列粒子浓度由大到小的顺序为c(Na+)、c(HCO3-)、c(CO32-),c(H2CO3)、c(OH-)_________。
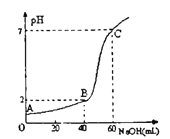
(3)常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示。所用NaOH溶液浓度为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)一定条件下,平衡常数如下:
2NO2![]() N2O4 K1 NO2
N2O4 K1 NO2![]() 1/2N2O4K2 N2O4
1/2N2O4K2 N2O4![]() 2NO2 K3
2NO2 K3
推导K1与K2,K1与K3的关系分别为:______________。
(2)衡量催化剂的性能指标有:活性、选择性、稳定性、价格等。对于给定条件下反应物之间能够同时发生多个反应的情况,理想的催化剂可以大幅度提高目标产物在最终产物中的____(填“产率”、“比率”、转化率),催化剂的这种特性,称作它的________性。
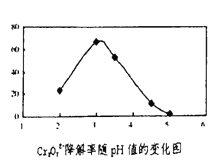
(3)溶液的pH对Cr2O72-降解率的影响如下图所示。
已知:Cu2O![]() Cu+CuSO4;
Cu+CuSO4;
酸性越大,Cr2O72-被还原率越大。
①由上右图可知,pH分别为2、3、4 时,Cr2O72-的降解率最好的是______,其原因是______。
②按右图加入10滴浓硫酸,溶液由橙黄色变为橙色,请结合化学用语用平衡移动原理解释其原因_____。
(4)一定条件下焦炭可以还原NO2,反应为:2NO2(g)+2C(s) ![]() N2(g)+2CO2(g)。在恒温的密闭容器下,6molNO2和足量C 发生该反应,测得平衡时NO2的物质的量与平衡总压的关系如图所示:
N2(g)+2CO2(g)。在恒温的密闭容器下,6molNO2和足量C 发生该反应,测得平衡时NO2的物质的量与平衡总压的关系如图所示:
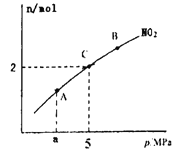
则C点NO2的转化率和C点时该反应的压强平衡常数Kp=(K,是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)分别为______、_______。
(5)已知由CO生成CO2的化学方程式为CO+O2![]() CO2+O。其正反应速率为v正=K正c(CO)·c(O2),逆反应速率为v逆=K逆c(CO2)·c(O),K正、K逆为速率常数。在2500K下,K正=1.21×105 L·s-1·mol-1,K逆=3.02×105L·s-1·mol-1。则该温度下上述反应的平衡常数K值为_______(保留小数点后一位小数)。
CO2+O。其正反应速率为v正=K正c(CO)·c(O2),逆反应速率为v逆=K逆c(CO2)·c(O),K正、K逆为速率常数。在2500K下,K正=1.21×105 L·s-1·mol-1,K逆=3.02×105L·s-1·mol-1。则该温度下上述反应的平衡常数K值为_______(保留小数点后一位小数)。
(6)利用水煤气合成二甲醚的三步反应如下:
①2H2(g) + CO(g) ![]() CH3OH(g); ΔH1
CH3OH(g); ΔH1
②CH3OH(g) ![]() CH2OCH3(g) + H2O(g); ΔH2
CH2OCH3(g) + H2O(g); ΔH2
③CO(g) + H2O(g) ![]() CO2(g) + H2(g); ΔH3
CO2(g) + H2(g); ΔH3
总反应: 3H2(g)+3CO(g) ![]() CH2OCH3(g)+CO2(g)的ΔH=_______。
CH2OCH3(g)+CO2(g)的ΔH=_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述错误的是
A. 常温下,pH=3的盐酸与pH=11的氨水溶液中水的电离程度相同
B. 常温下两种溶液①0.1mol/L CH3COOH溶液 ②0.3mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积的混合液,c(H+):①>②
C. 室温下向10mL pH=3的醋酸溶液中加入水稀释后溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]不变
D. MOH和ROH两种碱的溶液分别加水稀释时,pH变化如图所示则稀释前,c(ROH)<10c(MOH)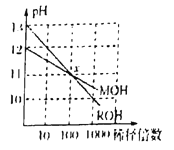
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组用如图所示装置A,B分别探究金属锌与稀硫酸的反应,实验过程中A烧杯内的溶液温度升高,B烧杯的电流计指针发生偏转,请回答以下问题. 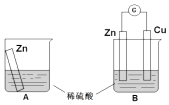
(1)A烧杯中反应的离子方程式为 .
(2)B中Zn板是极,发生的电极反应是 , Cu板上的现象是 , 发生的电极反应是 .
(3)从能量转化的角度来看,A,B中反应物的总能量(填“大于”、“小于”或“等于”)生成物总能量,A中是将化学能转变为 , B中主要是将化学能转变为 .
(4)该小组同学反思原电池的原理,其中观点正确的是(填字母序号).
A.原电池反应的过程中一定有电子转移
B.原电池装置需要2个电极
C.电极一定不能参加反应
D.氧化反应和还原反应可以拆开在两极发生.
查看答案和解析>>
科目: 来源: 题型:
【题目】元素是构成我们生活的世界中一切物质的“原材料”.
(1)自18世纪以来,科学家们不断探索元素之谜.通过从局部到系统的研究过程,逐渐发现了元素之间的内在联系.下面列出了几位杰出科学家的研究工作.
序号 | ① | ② | ③ | ④ |
科学家 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
工作 | 发现“八音律”,指出从某一指定的元素起,第八个元素是第一个元素的某种重复 | 创立 近代原子论,率先开始相对原子质量的测定工作 | 发现了5组性质相似的“三元素组”,中间元素的相对原子质量为前后两种元素相对原子质量的算术平均值 | 认为 各元素组之间并非毫不相关,可以用相对原子质量把它们按从小到大的顺序串联 |
上述科学家的研究按照时间先后排序合理的是(填数字序号).
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图1所示. 
①门捷列夫将已有元素按照相对原子质量排序,同一(填“横行”或“纵列”)元素性质相似.结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是 , 第5列方框中“Te=128?”的问号表达的含义是 .
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满.而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量递增呈现周期性变化,而是随着原子序数(核电荷数)递增呈现周期性变化.其本质原因是(填字母序号).
A.随着核电荷数递增,原子核外电子排布呈现周期性变化
B.随着核电荷数递增,原子半径呈现周期性变化
C.随着核电荷数递增,元素最高正化合价呈现周期性变化
(3)在现有的元素周期表中有A,B,D,E,X、Y、Z七种短周期元素.X与Y处于同一周期,Y的最高价氧化物的水化物与强酸、强碱均能反应.Z的单质常温下为气态,同条件下相对于氢气的密度比为35.5.其余信息如图2所示: ①上述七种元素中,处于第二周期的有(用元素符号表示,下同),X在周期表中的位置是 .
②E的原子结构示意图为 , 写出Z元素气态氢化物的电子式: .
③B单质与E的最高价氧化物的水化物在一定条件下发生反应的化学方程式为;Y单质与X的最高价氧化物的水化物溶液反应的离子方程式为 .
④B和D的最高价氧化物的水化物的化学式分别为、 , 二者酸性前者(填“强于”或“弱于”)后者,原因是B和D的非金属性有差异,利用原子结构解释产生差异的原因: .
查看答案和解析>>
科目: 来源: 题型:
【题目】下列具有特殊性能的材料中,由主族元素和副族元素形成的化合物是( )
A.半导体材料砷化镓
B.吸氢材料镧镍合金
C.透明陶瓷材料硒化锌
D.超导材料K3C60
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,属于氧化还原反应的是( )
A.2NaHCO3 ![]() ?Na2CO3+CO2↑+H2O
?Na2CO3+CO2↑+H2O
B.H2SO4+CuO═CuSO4+H2O
C.2 H2S+SO2═3S↓+2H2O
D.CO2+Ca(OH)2═CaCO3↓+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox , Cu为+2价),下列有关“汉紫”的说法中不正确的是( )
A.用盐的形式表示:BaSiO3·CuSiO3
B.用氧化物形式表示:BaO·CuO·2SiO2
C.易溶于强酸、强碱
D.性质稳定,不易褪色
查看答案和解析>>
科目: 来源: 题型:
【题目】每年10月23日上午6:02到晚上6:02被脊为“摩尔日"(Mole Day),这个时间的美式写法为6:0210/23,外观与阿伏加德罗常数6.02×1023相似。NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下22.4 LNO与11.2LO2 充分反应,产物的分子数为NA
B. 0.1mol/L的Na2SO4溶液中,SO42- 数目是0.1NA
C. 标准状况下.22.4L氯气与足量铁粉充分反应,转移的电子数为3NA
D. 0.1molCH4的核外电子数为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com