
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A. Si是常用的半导体材料,可以制作光电池
B. 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通足量的CO2
C. 二氧化硅不与任何酸反应,可用石英制造耐酸容器
D. 不能用石英坩埚加热熔化氢氧化钠固体
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与人类生产、生活密切相关,下列叙述中正确的是( )
A.泰国银饰和土耳其彩瓷是“一带一路”沿线国家的特色产品,其主要成分均为金属材料
B.从石墨中剥离出的石墨烯薄片能导电,因此是电解质
C.二氧化硫和氨气都易液化,液氨常用作制冷剂
D.生理盐水可用于养殖场消毒,以杀死H7N9等病毒
查看答案和解析>>
科目: 来源: 题型:
【题目】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡.根据要求回答问题
(1)铝盐的水解原理在生活中应用广泛,如明矾常作净水剂,其净水的原理是_________(用离子方程式表示);如硫酸铝常作泡沫灭火器原料之一,其原理是________________(用离子方程式表示)。
(2)室温下,0.1 mol/L的某二元酸H2B溶液中,溶液中存在的含B粒子只有HB一、B2-,回答下列问题:
①写出H2B在水中的电离方程式是_________________________________________;
②在0.1 mol/L 的Na2B溶液中,下列粒子浓度关系式正确的是_______;
A.c(B2-)+c(HB-)+c(H2B)=0.1 mol/L B.c(Na+)+c(OH-)=c(H+)+c(HB-)
C.c(Na+)+c(H+)=c(OH-)+c(HB-)+2c(B2-) D.c(Na+)=2c(B2-)+2c(HB-)
③已知0.1 mol/L NaHB溶液的pH=2, 0.1 mol/L NaHB溶液中各种离子浓度由大到小的顺序为______________________________________________。
(3)已知25 ℃时有关弱酸的电离平衡常数如下:HCN:4.9×10-10,H2CO3:K1=4.4×10-7 K2=4.7×10-11,向NaCN溶液中通入少量二氧化碳气体,写出发生反应的化学方程式 ________。
(4)含Cr2O72﹣的废水毒性较大,某工厂废水中含5.0×10﹣3 mol·L﹣1的Cr2O72﹣.为了使废水的排放达标,进行如下处理:
![]()
①绿矾为FeSO4·7H2O,反应(I)中FeSO4与Cr2O72﹣的物质的量之比为_________.
②常温下若处理后的废水中c(Cr3+)=6.0×10﹣7 mol·L﹣1,则处理后的废水的pH=______.(Ksp[Cr(OH)3]=6.0×10﹣31)
查看答案和解析>>
科目: 来源: 题型:
【题目】有关做焰色反应实验时的注意事项,下列说法不正确的是( )
A. 每次实验中都要先将铂丝灼烧到火焰无色,再蘸取被检验物质
B. 钾的焰色反应要透过蓝色钴玻璃观察
C. 实验时最好选择本身颜色较深的火焰
D. 没有铂丝可用光洁无锈铁丝代替进行实验
查看答案和解析>>
科目: 来源: 题型:
【题目】铁、钴(Co)、镍(Ni)是同族元素,它们的化合物在工业上有重要的应用。
(1)现将含0.5mol FeCl3的溶液和含0.5mol KSCN的溶液混合,混合后溶液体积为1L,已知溶液存在平衡:Fe3+(aq)+SCN-(aq) ![]() Fe(SCN)2+(aq)(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图所示:温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45 mol·L-1,求达到平衡时的平均反应速率v(SCN-)=____________,该温度下的Fe3+的平衡转化率为_____________,该温度下反应的平衡常数为__________。
Fe(SCN)2+(aq)(忽略其它过程)。平衡浓度c[Fe(SCN)2+]与温度T的关系如图所示:温度为T1时,反应在5秒钟时达到平衡,平衡时c[Fe(SCN)2+]=0.45 mol·L-1,求达到平衡时的平均反应速率v(SCN-)=____________,该温度下的Fe3+的平衡转化率为_____________,该温度下反应的平衡常数为__________。

(2)羰基法提纯镍涉及的一个反应为:Ni(s)+4CO(g)![]() Ni(CO)4(g)
Ni(CO)4(g)
①当温度升高时,![]() 减小,则该反应的⊿H_____0(填“>”或“<”)。
减小,则该反应的⊿H_____0(填“>”或“<”)。
②一定温度下,将一定量的粗镍和CO加入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________(填代号)。

(3)CoxNi(1-x)Fe2O4 (其中Co、Ni均为+2价)可用作H2O2分解的催化剂,具有较高的活性。两种不同方法制得的催化剂在10℃时催化、分解6%的H2O2溶液的相对初始速率随x变化的曲线如右图所示。

由图中信息可知__________法制取得到的催化剂活性更高;Co2+、Ni2+ 两种离子中催化效果较好的是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】向一定量的Cu、Fe2O3、的混合物中加入300mL 1mol/L的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+原混合物中Cu的质量为( )
A.9.6g
B.6.4g
C.3.2g
D.1.6g
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验:
(1)取冰醋酸配制250 mL 0.4 mol·L-1的醋酸溶液,用0.4 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
①将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如右图所示。则稀释过程中溶液的pH由大到小的顺序______(填字母)。

②配制250 mL 0.4 mol·L-1 醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、胶头滴管和____________。
③为标定该醋酸溶液的准确浓度,用0.2000 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
实验序号 | 1 | 2 | 3 | 4 |
消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
该醋酸溶液的准确浓度为_____________(保留小数点后四位),上述标定过程中,造成测定结果偏高的原因可能是_______________(多选、错选不得分)。
a.未用标准液润洗碱式滴定管
b.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
c.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
d.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
(2)该小组同学探究浓度对醋酸电离程度的影响时,用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
醋酸浓度( mol·L-1) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 |
pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
①根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是______________________________________________________________。
②简述用pH试纸测 0.1mol·L-1 醋酸溶液pH的方法___________。
③利用水解理论设计实验证明醋酸的酸性比碳酸的强:______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】向某含有SO ![]() 、SiO
、SiO ![]() 、CO
、CO ![]() 、Br﹣、Na+的溶液中缓慢通入Cl2直至过量,下列对该反应过程的判断不正确的是( )
、Br﹣、Na+的溶液中缓慢通入Cl2直至过量,下列对该反应过程的判断不正确的是( )
A.整个过程共发生2个氧化还原反应
B.所有阴离子的浓度都发生了变化
C.溶液的颜色发生了变化
D.反应过程中既有气体产生,也有沉淀产生
查看答案和解析>>
科目: 来源: 题型:
【题目】用硫酸分解磷尾矿[主要成份为Ca5(PO4)3F]可制得中强酸磷酸H3PO4。请回答:
(1)Na2HPO4溶液呈碱性,则在该溶液中c(H2PO4-)_____c(PO43-)(填“>”、“<”、“=”),向Na2HPO4溶液中加入足量的CaCl2溶液,溶液显酸性,溶液显酸性的原因是(从电离平衡移动角度分析):________________________。
(2)Ca5(PO4)3F(s) +OH-(aq)![]() Ca5(PO4)3(OH) (s)+F-,该温度下,溶液中c(F-)随溶液的pH和温度(T)的变化曲线如图所示。
Ca5(PO4)3(OH) (s)+F-,该温度下,溶液中c(F-)随溶液的pH和温度(T)的变化曲线如图所示。
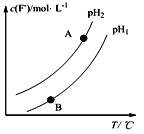
则:适当______温度有利于磷尾矿转化为羟基磷灰石(填“升高”、“降低”);pH1___pH2(填“>”、“<”、“=”);A、B两点的溶液中F—的速率v(A)____v(B)(填“>”、 “<”、“=”);
(3)已知:25℃时,H3PO4的电离平衡常数:K1=7.52×10-3;K2=6.23×10-8;K3=6.23×10-13,则:H3PO4(aq)+OH-(aq)![]() H2PO4-(aq)+H2O (l)的平衡常数K=____________。
H2PO4-(aq)+H2O (l)的平衡常数K=____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对于结构 ![]() 满足的有机物,下列描述中正确的是( )
满足的有机物,下列描述中正确的是( )
A.分子中有2种含氧官能团
B.能发生取代、加成、消去、氧化反应
C.1mol该有机物最多消耗3mol NaOH
D.苯环上的一溴代物最多有3种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com