
科目: 来源: 题型:
【题目】金刚乙烷、金刚乙胺等已经被批准用于临床治疗人感染禽流感,且临床研究表明金刚乙烷比金刚乙胺的副作用小.
(1)金刚乙烷可通过下列转化生成金刚乙胺:
①金刚乙烷的分子式为 .
②反应Ⅰ的反应类型为 . 反应Ⅱ的另一产物为 .
(2)金刚乙烷还可通过如图下列转化生成高分子化合物(用“R﹣”表示  ,如金刚乙烷表示为R﹣CH2CH3);
,如金刚乙烷表示为R﹣CH2CH3); ![]()
已知:E分子中有两个C=O双键,但不能发生银镜反应;标准状况下,1molF与足量的钠完全反应会生成22.4L气体,若与足量NaHCO3溶液完全反应也会生成22.4L气体.
①条件1为 .
②条件2为 , 写出C→D的化学方程式: .
③E分子中官能团的名称为 , G的结构简式为 .
④满足下列条件的F的同分异构体只有一种,其结构简式为 .
a.属于芳香族化合物
b.核磁共振氢谱图中只有两组吸收峰,且峰面积之比为1:1.
查看答案和解析>>
科目: 来源: 题型:
【题目】淀粉和纤维素都可以用(C6H10O5)n表示,下列叙述正确的是( )
A.它们都不是混合物
B.它们都不是天然高分子化合物
C.它们是同分异构体
D.它们水解的最终产物都是葡萄糖
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组中的两种物质作用时,反应条件或反应物的用量比改变,生成的化合物不会改变的是
A. 钠与氧气 B. 氢氧化钠与二氧化碳
C. 碳酸钠与盐酸 D. 过氧化钠与水反应
查看答案和解析>>
科目: 来源: 题型:
【题目】100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃ 的恒温槽中,烧瓶内气体逐渐变为红棕色:N2O4(g)![]() 2NO2 (g)。下列结论不能说明上述反在该条件下已经达到平衡状态的是()
2NO2 (g)。下列结论不能说明上述反在该条件下已经达到平衡状态的是()
①N2O4的消耗速率与NO2的生成速率之比为1:2 ②NO2生成速率与NO2消耗速率相等
③烧瓶内气体的压强不再变化 ④烧瓶内气体的质量不再变化
⑤NO2的物质的量浓度不再改变 ⑥烧瓶内气体的颜色不再变化
⑦烧瓶内气体的平均相对分子质量不再变化 ⑧烧瓶内气体的密度不再变化。
A. ①③⑦ B. ①④⑧ C. ①②⑤ D. ④⑥⑧
查看答案和解析>>
科目: 来源: 题型:
【题目】在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10﹣10 , 下列说法不正确的是( ) 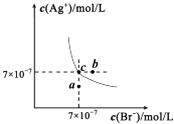
A.在t℃时,AgBr的Ksp为4.9×l0﹣13
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
D.在t℃时,AgCl(s)+Br﹣(aq)AgBr(s)+Cl﹣(aq)平衡常数K≈816
查看答案和解析>>
科目: 来源: 题型:
【题目】氨的合成是一项重要的化工生产.已知合成氨有关能量变化的图象如图1.
(1)反应N2(g)+3H2(g) ![]() 2NH3(g)△H=KJ/mol;
2NH3(g)△H=KJ/mol;
(2)已知键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.
化学键 | H﹣H | N﹣H | N≡N |
键能/kJmol﹣1 | 436 | X | 946 |
则表中X的值是 .
(3)在一定条件下按图2实线I进行,改变某条件按图2虚线II进行,则该条件可能是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol
C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol
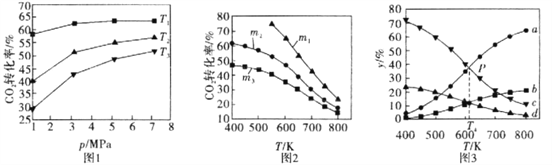
(1)图l、图2分别是CO2的平衡转化率随压强及温度的变化关系,已知m为起始时的投料比,即m=![]() 。
。
①图l中投料比相同,温度从高到低的顺序为________。
②图2中.m1、m2、m3投料比从大到小的顺序为________,理由是________。
(2)图3表示在总压为5MPa的恒压条件下,且m=3时,不同温度下各物质的物质的量分数与温度的关系。
①曲线b代表的物质为________(填化学式)。
②图3中P点时。CO2的转化率为________。
③T4温度时,该反应的平衡常数Kp=________。(提示:用平衡分压代替平衡浓度来计算,某组分平衡分压=总压×该组分的物质的量分数,结果保留小数点后三位)
查看答案和解析>>
科目: 来源: 题型:
【题目】用标准盐酸溶液滴定待测浓度的碱溶液时,下列操作中会引起碱溶液浓度的测定值偏大的是( )
A.锥形瓶里溶液在滴定过程中溅出
B.锥形瓶用蒸馏水冲洗后未用待测液润洗
C.指示剂变色15 s后又恢复为原来的颜色便停止滴定
D.滴定管装液后尖嘴部位有气泡,滴定后气泡消失
查看答案和解析>>
科目: 来源: 题型:
【题目】1967年舒尔滋提出金属互化物的概念,其定义为固相金属间化合物拥有两种或两种以上的金属元素,如Cu9Al4、Cu5Zn8等.回答下列问题:
(1)某种金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于(填“晶体”或“非晶体”).
(2)基态铜原子有个未成对电子,二价铜离子的电子排布式为 , 在CuS04溶液 中滴入过量氨水,形成配合物的颜色为 .
(3)铜能与类卤素(SCN)2反应生成Cu(SCN)2 , 1mol(SCN)2分子中含有.键的数目为;类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H﹣S﹣C≡N)的沸点低于异硫氰酸(H﹣N=C=S)的沸点,其原因是 .
(4)ZnS的晶胞结构如图1所示,在ZnS晶胞中,S2﹣的配位数为 .
(5)铜与金形成的金属互化物结构如图2,其晶胞边长为a nm,该金属互化物的密度为(用含“a、NA 的代数式表示)gcm﹣3 . 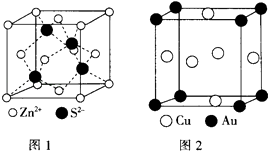
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com