
科目: 来源: 题型:
【题目】下列热化学方程式或叙述正确的是( )
A.1 mol液态肼在足量氧气中完全燃烧生成水蒸气,放出642kJ的热量:N2H4(l)+O2(g)═N2(g)+2H2O(g)△H=+642 kJ?mol﹣1
B.12 g石墨转化为CO时,放出110.5 kJ的热量:2C(石墨,s)+O2(g)═2CO(g)△H=﹣110.5 kJ?mol﹣1
C.已知:H2(g)+ ![]() O2(g)═H2O(l)△H=﹣286 kJ?mol﹣1 , 则:2H2O(l)═2H2(g)+O2(g)的△H=+572 kJ?mol﹣1
O2(g)═H2O(l)△H=﹣286 kJ?mol﹣1 , 则:2H2O(l)═2H2(g)+O2(g)的△H=+572 kJ?mol﹣1
D.已知N2(g)+3H2(g)?2NH3(g)△H=﹣92.4 kJ?mol﹣1 , 则在一定条件下向密闭容器中充入0.5 mol N2(g)和1.5 mol H2(g)充分反应放出46.2 kJ的热量
查看答案和解析>>
科目: 来源: 题型:
【题目】立方烷( ![]() )具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点.下面是立方烷衍生物I的一种合成路线:
)具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点.下面是立方烷衍生物I的一种合成路线: 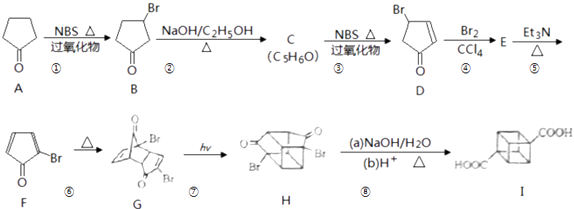
回答下列问题:
(1)C的结构简式为 , E的结构简式为 .
(2)③的反应类型为 , ⑤的反应类型为 .
(3)化合物A可由环戊烷经三步反应合成: ![]()
反应I的试剂与条件为 , 反应2的化学方程式为 , 反应3可用的试剂为 .
(4)在I的合成路线中,互为同分异构体的化合物是 . (填化合物代号)
(5)I与碱石灰共热可化为立方烷.立方烷的核磁共振氢谱中有个峰.
(6)立方烷经硝化可得到六硝基立方烷,其可能的结构有种.
查看答案和解析>>
科目: 来源: 题型:
【题目】现有下列反应:
①、2H2O+Cl2+SO2=H2SO4+2HCl
②、 KMnO4+ HCl(浓)= KCl+__MnCl2+___Cl2↑+___H2O
针对上述两个反应回答:
(1)配平②的化学方程式________;
(2)用单线桥标出①中电子转移的方向和数目________;
(3)Cl2、SO2和KMnO4的氧化性强弱顺序为____;
(4)反应①中氧化产物和还原产物的物质的量之比为___;
(5)反应②中氯化氢表现出的性质是___。
A.还原性 B.酸性 C.氧化性
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子的检验方法合理的是( )
A. 向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+
B. 向某溶液中通入Cl2,然后再加入KSCN溶液变红色,则原溶液中含有Fe2+
C. 向某溶液中加入NaOH溶液,得到红褐色沉淀,说明溶液中含有Fe3+
D. 向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明溶液中含有Fe2+,不含有Mg2+
【答案】C
【解析】试题分析:A.KSCN溶液与Fe3+溶液作用的方程式为:Fe3++3SCN-Fe(SCN)3,而Fe2+与KSCN溶液不反应,如果该溶液既含Fe3+,又含Fe2+,滴加KSCN溶液,溶液呈红色,证明存在Fe3+而不能证明没有Fe2+,故A错误;B.若原溶液中含Fe2+,通入Cl2,氯气将Fe2+氧化成Fe3+,滴加KSCN溶液后显红色,若原溶液中不含Fe2+,含有Fe3+,通入Cl2,加入KSCN溶液同样可以变血红色,故B错误;C.加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+,故C正确;D.氢氧化镁为白色沉淀,能被红褐色沉淀掩盖,无法确定,故D错误;故选C。
考点:考查物质的检验及鉴别。
【题型】单选题
【结束】
22
【题目】关于Na2CO3和NaHCO3性质的有关叙述正确的是
A. 在水中的溶解性:Na2CO3<NaHCO3
B. 热稳定性:Na2CO3<NaHCO3
C. 与酸反应的快慢:Na2CO3<NaHCO3
D. Na2CO3不能转化成NaHCO3,而NaHCO3能转化为Na2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】元素性质随原子序数的递增呈周期性变化的实质是( )
A. 元素的相对原子质量增大,量变引起质变
B. 原子的电子层数增多
C. 原子核外电子排布呈周期性变化
D. 原子半径呈周期性变化
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是重要的工业原料.煤化工可以利用煤炭制取水煤气从而合成甲醇:CO(g)+2H2(g)CH3OH(g).已知常温常压下反应的能量变化如图1所示: 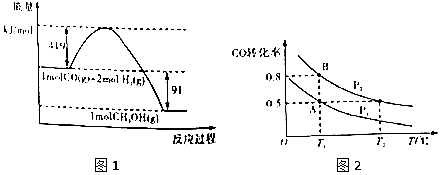 ②
②
化学键 | H﹣H | H﹣O | O=O |
键能kj/mol | 436 | x | 496 |
③CO(g)+ ![]() O2(g)=CO2(g)△H=﹣280kJ/mol
O2(g)=CO2(g)△H=﹣280kJ/mol
H2(g)+ ![]() O2(g)=H2O(I)△H=﹣284kJ/mol
O2(g)=H2O(I)△H=﹣284kJ/mol
H2O(I)=H2O(g)△H=+44kJ/mol
请回答下列问题:
(1)甲醇气体分解为CO和H2两种气体这一反应的活化能为kj/mol;
(2)请写出表示气态甲醇燃烧热的热化学方程式;
(3)H﹣O的键能x值为;
(4)如图2:在一容积可变的密闭容器中充入10molCO气体和30molH2气体,当达到平衡状态A时,容器的体积为20L.如反应开始时仍充入10molCO和30molH2 , 则在平衡状态B时容器的体积V(B)=L;
(5)在甲、乙、丙三个不同密闭容器中按不同方式投料,一定条件下发生该反应(起始温度和起始体积相同,反应物和生成物反应前后均为气态).相关数据如表所示:
容器 | 甲 | 乙 | 丙 |
相关条件 | 恒温恒容 | 绝热恒容 | 恒温恒压 |
反应物投料 | 1molCO、2molH2 | 1molCH3OH | 1molCH3OH |
平衡时容器体积 | V(甲) | V(乙) | V(丙) |
反应的平衡常数K | K(甲) | K(乙) | K(丙) |
平衡时CH3OH的浓度/molL﹣1 | C(甲) | C(乙) | C(丙) |
平衡时CH3OH的反应速率/molL﹣1min﹣1 | v(甲) | v(乙) | v(丙) |
则下列说法正确的是 .
A.V(甲)>V(丙)
B.K(乙)>K(丙)
C.c(乙)>c(甲)
D.v(甲)=v(丙)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是( )
A.CH3CH2CH3
B.CH3CH(CH3)CH2CH3
C.CH3CH2OH
D.CH3OCH3
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上通常采用N2(g)和H2(g)崔华成NH3(g):N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJmol﹣1
(1)在一定温度下,若将10amolN2和30amolH2放入2L的密闭容器中,充分反应后测得平衡时N2的转化率为60%,则该反应的平衡常数为(用含a的代数式表示).若此时再向该容器中投入10amolN2、20amolH2和20amolNH3 , 判断平衡移动的方向是(填“正向移动”“逆向移动”或“不移动”).
(2)若反应起始时N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.1mol/L.则NH3达到平衡时浓度的范围为;若平衡时N2、H2、NH3的浓度分别为0.1mol/L、0.3mol/L、0.1mol/L,则NH3起始时浓度的范围为 .
(3)一定条件下,在容积相同的三个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如表:
容器 | 甲 | 乙 | 丙 | |
反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 | |
平衡时数据 | 反应能量变化的绝对值(kJ) | Q1 | Q2 | Q3 |
反应物转化率 | a1 | a2 | a3 | |
体系压强(Pa) | p1 | P2 | P3 | |
则Q1+Q2=kJ;a1+a2l(填“<”“>”或“=”下同):2p2p3
(4)如图:A是恒容的密闭容器,B是一个体积可变的充气气囊.保持恒温,关闭K2 , 将1molN2和3molH2通过K3充入B中,将2molN2和6molH2通过K1充入A中;起始时A、B的体积相同均为1L,达到平衡时,V(B)=0.9L;然后打开K2 , 一段时间又达到平衡时,B的体积为L(连通管中气体体积不计). 
查看答案和解析>>
科目: 来源: 题型:
【题目】现有①乙酸乙酯和乙酸钠溶液、②溴化钠溶液和溴水的混合液,分离它们的正确方法依次是( )
A. 分液、蒸馏B. 分液、萃取C. 萃取、分液D. 蒸馏、分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com