
科目: 来源: 题型:
【题目】常温下,将一定量的钠铝合金置于水中,合金全部溶解,所得的溶液中仍含有0.02mol的NaOH ,然后向溶液中逐滴加入lmol/L的盐酸,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是( )
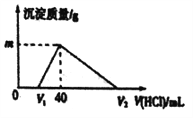
A. 原合金质量为0.92g B. 图中V2的值为60mL
C. 产生氢气的体积为1120mL D. 图中m的值为1.56g
查看答案和解析>>
科目: 来源: 题型:
【题目】等体积的硫酸铝、硫酸锌、硫酸钠溶液分别与足量氯化钡溶液反应。若生成硫酸钡沉淀的质量比为1:2:3,则三种硫酸盐的物质的量浓度之比为( )
A. 1:2:3 B. 1:6:9 C. 1:3:3 D. 1:3:6
查看答案和解析>>
科目: 来源: 题型:
【题目】磷在氧气中燃烧,可能生成P2O3和P2O5 , 已知单质磷(P)的燃烧热为X kJ/mol,0.1molP在2.24L O2(标准状况下)燃烧至反应物耗尽时,放出Y kJ 的热量,则下列说法错误的是( )
A.生成0.025 mol P2O5
B.生成 P2O3所释放的热量为(Y﹣0.05X) kJ
C.2P(s)+ ![]() O2(g)=P2O3(s)△H=﹣(40Y﹣2X)kJ?mol﹣1
O2(g)=P2O3(s)△H=﹣(40Y﹣2X)kJ?mol﹣1
D.生成的 P2O3与 P2O5的质量之比为 1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,在两份相同的 Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( ) 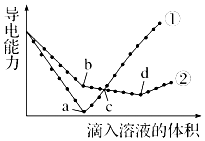
A.①代表滴加H2SO4溶液的变化曲线
B.b点,水电离产生的c(H+)<10﹣7mol/L
C.c点,两溶液中含有相同量的 OH﹣
D.a、d两点对应的溶液均显中性
查看答案和解析>>
科目: 来源: 题型:
【题目】能证明某烃分子里只含有一个碳碳双键的事实是( )
A. 该烃分子里碳氢原子个数比为1:2
B. 该烃能使酸性KMnO4溶液褪色
C. 该烃完全燃烧生成的CO2和H2O的物质的量相等
D. 该烃容易与溴水发生加成反应,且1mol该烃完全加成消耗1mol溴单质
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是 ( )
A. 摩尔是国际单位制中七个基本物理量之一
B. 1molSO2的质量为64 g·mol-1
C. 12 g 12C中所含碳原子数即为阿伏加德罗常数
D. 气体的摩尔体积约为22.4 L·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】如图,隔板K可左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处.发生反应2A(g)+B(g)2C(g),达到平衡后,恢复至温度.下列有关说法不正确的是
( )
A.达平衡后,隔板K最终停留在左侧刻度0~2之间
B.若平衡时K停留在左侧1处,则活塞停留在右侧6处
C.达到平衡时,甲容器中B的物质的量小于于乙容器中B的物质的量
D.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
查看答案和解析>>
科目: 来源: 题型:
【题目】醋是重要的调味品,我国劳动人民在很早以前就知道酒在空气中能“酸败成醋”,该事实的实质是
A. 酒中的乙醇挥发,使乙醇的含量降低B. 酒中的杂质腐败成酸
C. 酒中的乙醇被氧化成乙醛D. 酒中的乙醇被氧化成乙酸
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素A、B、C、D在周期表中的位置如图所示,B、D最外层电子数之和为12,二者可形成DB2、DB3两种分子,DB2具有漂白性.
A | B | |
C | D |
回答下列问题:
(1)A位于元素周期表周期,族,其氢化物的分子式是 .
(2)下列叙述中,正确的是(填字母).
a.稳定性:A的氢化物>C的氢化物 b.还原性:B2﹣>D2﹣
c.酸性:H4CO4>H2DO4 d.最高化合价值:D=B>A>C
(3)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2 . 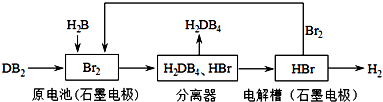
①原电池中DB2参与反应的电极为 , 写出电极反应式;若有5mol DB2参加反应(假若反应物无损耗),则生成标准状况下L H2 .
②为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到 , 证明分离效果较好.
③将该工艺流程用总反应的化学方程式表示为:
查看答案和解析>>
科目: 来源: 题型:
【题目】中国古代四大发明之一﹣﹣黑火药,它的爆炸反应为:2KNO3+3C+S ![]() A+N2↑+3CO2↑(已配平)
A+N2↑+3CO2↑(已配平)
①除S外,上列元素的电负性从大到小依次为 . 除K、S外第一电离能从大到小的顺序为 .
②在生成物中,A的晶体类型为 , 含极性共价键的分子的中心原子轨道杂化类型为 .
③CN﹣与N2互为 , 推算HCN分子中σ键与π键数目之比 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com