
科目: 来源: 题型:
【题目】向体积均为10 mL、物质的量浓度相同的两份NaOH 溶液中分别通入一定量的CO2,得到溶液甲和乙。向甲、乙两溶液中分别滴加0.1mol/L的盐酸,此时反应生成CO2体积(标准状况)与所加盐酸体积的关系如图所示。则下列叙述中不正确的是

A. 原NaOH溶液的物质的量浓度为0.5 mol/L
B. 当0盐酸)<10 mL时,甲溶液中发生反应的离子方程式为H++CO32-=HCO3-
C. 乙溶液中含有的溶质是Na2CO3、NaOH
D. 向乙溶液中滴加过量盐酸后产生CO2体积的最大值为224 mL
查看答案和解析>>
科目: 来源: 题型:
【题目】向体积均为10 mL、物质的量浓度相同的两份NaOH 溶液中分别通入一定量的CO2,得到溶液甲和乙。向甲、乙两溶液中分别滴加0.1mol/L的盐酸,此时反应生成CO2体积(标准状况)与所加盐酸体积的关系如图所示。则下列叙述中不正确的是

A. 原NaOH溶液的物质的量浓度为0.5 mol/L
B. 当0盐酸)<10 mL时,甲溶液中发生反应的离子方程式为H++CO32-=HCO3-
C. 乙溶液中含有的溶质是Na2CO3、NaOH
D. 向乙溶液中滴加过量盐酸后产生CO2体积的最大值为224 mL
查看答案和解析>>
科目: 来源: 题型:
【题目】写出下列反应的化学方程式:
(1)乙烯与溴化氢在一定条件下反应:反应类型:
(2)甲烷与氯气在光照的条件下生成一氯甲烷:反应类型:
(3)写出2﹣氯丙烷与氢氧化钠醇溶液反应的化学方程式:反应类型:
(4)写出2﹣氯丙烷与氢氧化钠水溶液反应的化学方程式:反应类型: .
查看答案和解析>>
科目: 来源: 题型:
【题目】如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3.试回答下列问题:
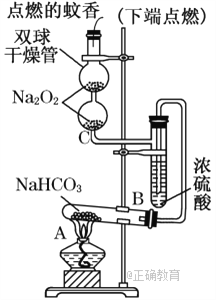
(1)在A试管内发生反应的化学方程式是____________________________________.
(2)B装置的作用是_______________________________________________________.
(3)在双球干燥管内发生反应的化学方程式为___________________________________.
(4)双球干燥管内观察到的实验现象是_________________________________________.上述实验现象说明________________________________________________________.
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是______________________________________________________________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】请同学们根据官能团的不同对下列有机物进行分类.把正确答案填写在题中的横线上①CH3CH2OH② ![]() ③CH3CH2Br④
③CH3CH2Br④ ![]() ⑤
⑤ ![]() ⑥
⑥ ![]() ⑦
⑦ ![]() ⑧
⑧ ![]() ⑨
⑨ ![]() ⑩
⑩ ![]()
(1)芳香烃:;
(2)卤代烃:;
(3)醇:;
(4)酚:;
(5)醛:;
(6)酮:;
(7)羧酸:;
(8)酯: .
查看答案和解析>>
科目: 来源: 题型:
【题目】现有五种物质A、B、C、D、E,其中有一种是碱,四种是盐,溶于水后电离可以产生下表中的离子:
阳离子 | Na+ H+ Ba2+ |
阴离子 | OH- CO32- SO42- |
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以与C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸。
请根据上述实验结果,填空:
(1)写出物质的化学式:A______ X______。
(2) B溶于水后的电离方程式为______________________。
鉴别B中阴离子的实验操作方法是_____________________。
(3)写出 A溶液与B溶液反应的离子方程式:
________________________________________________________________________。
(4)D与E的混合物a g,加入足量盐酸,反应完毕生成标准状况下的气体b L,则D在混合物中的质量分数为________。(列出算式即可)
查看答案和解析>>
科目: 来源: 题型:
【题目】铝土矿的主要成分是Al2O3,含有Fe2O3、SiO2(已知SiO2不溶于水,也不与强酸和强碱反应)等杂质,按下列操作从铝土矿中提取Al2O3。回答下列问题:

(1)写出沉淀物的化学式:a______; f______。
(2)写出加入过量NaOH溶液时所发生主要反应的离子方程式:________________、______________。
(3)写出通入气体B(过量)时溶液C中发生反应的离子方程式:___________________、_______________。
(4)铁有许多重要的化合物,中学化学常见的有三种氧化物和两种氢氧化物,则 Fe(OH)2 转化成Fe(OH)3的现象为___________________________。同时铁元素还有许多盐,FeSO4·7H2O是一种浅绿色晶体,俗称绿矾,常用于处理含有氧化性离子的废水。现用绿矾对某工厂废水(含有强氧化性离子Cr2![]() O72-)进行处理。在酸性条件下Cr2
O72-)进行处理。在酸性条件下Cr2![]() O72-被还原为Cr3+,写出在酸性条件下FeSO4·7H2O与Cr2
O72-被还原为Cr3+,写出在酸性条件下FeSO4·7H2O与Cr2![]() O72-反应的离子方程式:_______________________________________________________________________________
O72-反应的离子方程式:_______________________________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com