
科目: 来源: 题型:
【题目】下列电离方程式的书写正确的是
A.CuCl2=Cu +Cl2↑B.Na2CO3=2Na++CO32-
C.H2SO4=2H++S6++4O2-D.Ba(OH)2=Ba +2OH
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是部分短周期主族元素原子半径与原子序数的关系图。下列说法错误的是 ( )
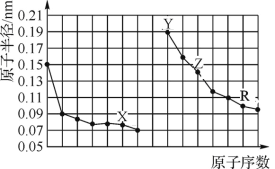
A. X、Y两种单质在常温下反应生成的产物为碱性氧化物
B. Z制成的槽车可以密封贮运R的氧化物对应的水化物
C. Y、Z、R三种元素最高价氧化物对应水化物相互之间可以发生反应
D. 电解熔融的X与Z组成的化合物可以得到单质Z
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物其结构简式如图,关于该有机物,下列叙述不正确的是( )
A.能使酸性KMnO4溶液、溴水褪色,原理相同
B.1 mol该有机物能与H2发生反应,消耗H2 4mol
C.一定条件下,能发生加聚反应
D.该有机物苯环上的一个H被取代,有3种同分异构体
查看答案和解析>>
科目: 来源: 题型:
【题目】麻黄素是中枢神经兴奋剂,其合成路线如下图所示。
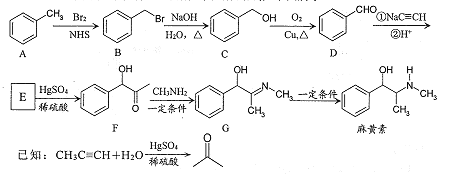
(1)F中的含氧官能团名称为 ____和_____。
(2)E的结构简式为 ____。
(3)写出B→C的化学反应方程式:_______。
(4) F→G历经两步反应,反应类型依次为_____、 ______。
(5)请写出同时满足下列条件的F的一种同分异构体的结构简式_____。
①能发生银镜反应;②水解产物能与FeCl3显色:③核磁共振氢谱显示有四组峰。
(6)请写出以乙醇为原料制备强吸水性树脂![]() 的合成路线流程图(可选择题干中相关试剂,无机试剂任选,合成路线流程图示例见本题题干)___________________。
的合成路线流程图(可选择题干中相关试剂,无机试剂任选,合成路线流程图示例见本题题干)___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】第一代半导体材料(Si、Ge等)与第二代半导体材料(GaAs、InSb等)一起,将人类推进了信息时代。近年来,以碳化硅(SiC)、氮化镓(GaN)为代表的第三代半导体材料的出现,开辟了人类资源和能源节约型社会的新发展,也成为了科学家研究的热点。
(1)N、P、AS位于同一主族,基态氮原子的核外共有___种不同运动状态的电子,N2O的空间构型为_______。
(2)酞菁钴近年来在光电材料、非线性光学材料、光动力学中的光敏剂、催化剂等方面得到广泛的应用,其结构如图所示,中心离子为钴离子。酞菁钻中碳原子的杂化轨道类型为___;与钴离子通过配位健结合的氮原子的编号是_______。

(3)C与N处于同周期相邻元素,C形成的一种重要物质可燃冰是天然气水合物,具有笼形结构如图A(表面的小球是水分子,内部的大球是甲烷分子)。图A中最小的环中连接的原子总数是_______。可燃冰晶体具有多种笼状结构,其中一种由1个图A所示笼分别用2个面与另外两个相同的笼共面而成,则中间笼实际占有____个水分子。

(4)已知PH3分子的键角约为94%,而AsH3分子的键角约为91.8°,试用价层电子对互斥理论解释PH3的键角比AsH3的键角大的原因________________。
(5)第三周期主族元素中,按第一电离能大小排序,第一电离能在磷和铝之间的元素有____。
(6)氮化硼、氮化铝、氮化镓的结构类似于金刚石,熔点如表中所示;试从结构的角度分析它们熔点不同的原因__________________。
物质 | BN | AIN | GaN |
熔点/℃ | 3000 | 2200 | 1700 |
(7)磷化铝晶胞如图所示,若两个铝原子之间的最近距离为dpm,NA代表阿伏加德罗常数的值,则磷化铝晶体的密度p=_____g/cm3。

查看答案和解析>>
科目: 来源: 题型:
【题目】SO2是危害最为严重的大气污染物之一,SO2的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法或吸收法处理SO2。催化还原SO2不仅可以消除SO2污染,而且可得到有价值的单质S。
(1)在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2 和H2O。已知CH4和S的燃烧热分别为890.3kJ/mol和297.2kJ/mol,CH4和SO2反应的热化学方程式为________________。
(2)用H2还原SO2生成S的反应分两步完成,如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:
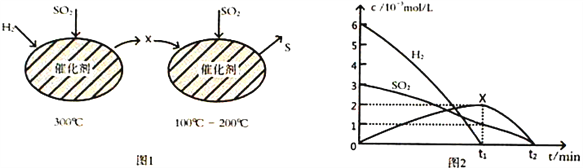
①分析可知X为____________(写化学式),0~t1时间段的温度为_________________,0~t1时间段用SO2 表示的化学反应速率为________________________________。
②总反应的化学方程式为_______________________________。
(3)焦炭催化还原SO2生成S2,化学方程式为:2C(s)+2SO2(g)![]() S2(g)+2CO2(g),恒容容器中,lmol/LSO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。
S2(g)+2CO2(g),恒容容器中,lmol/LSO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。
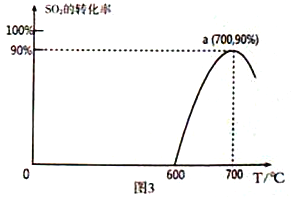
①该反应的ΔH_______________0 (填“>”或“<”)。
②计算a点的平衡常数为_______________________。
(4)工业上可用Na2SO3溶液吸收SO2,该反应的离子方程式为__________________________,25℃时用1mol/L的Na2SO3溶液吸收SO2,当溶液pH=7时,溶液中各离子浓度的大小关系为__________________。已知:H2SO3的电离常数K1=1.3×10-2,K2=6.2×10-8
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.1gH2和4gO2反应放出71.45kJ热量,则氢气的燃烧热为142.9 kJmol﹣1
B.在稀溶液中,H+(aq)+OH﹣(aq)═H2O(1)△H=﹣57.3 kJmol﹣1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的氢氧化钠溶液混合,放出的热量大于57.3kJ
C.HCl和NaOH反应的中和热△H=﹣57.3 kJmol﹣1,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJmol﹣1
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com