
科目: 来源: 题型:
【题目】下列各组变化中,化学反应的△H前者小于后者的一组是( )
①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1;CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H2;
②S(s)+O2(g)═SO2(g)△H1;S(g)+O2(g)═SO2(g)△H2;
③2H2(g)+O2(g)═2H2O(l)△H1;H2(g)+ ![]() O2(g)═H2O(l)△H2;
O2(g)═H2O(l)△H2;
④CaCO3(s)═CaO(s)+CO2(g)△H1;CaO(s)+H2O(l)═Ca(OH)2(s)△H2 .
A.①②
B.②③
C.①③
D.③④
查看答案和解析>>
科目: 来源: 题型:
【题目】根据问题进行计算:
(1)实验测得16g甲醇[CH3OH(l)]在氧气中充分燃烧生成二氧化碳气体和液态水时释放出363.25kJ的热量,试写出甲醇燃烧热的热化学方程式: .
(2)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程.已知反应:N2(g)+3H2(g)2NH3(g)△H=a kJmol﹣1 . 有关键能数据如表:
化学键 | H﹣H | N﹣H | N≡N |
键能(kJmol﹣1) | 436 | 391 | 945 |
试根据表中所列键能数据估算a的数值 .
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算.已知:
C(s,石墨)+O2(g)═CO2(g)△H1=﹣393.5kJmol﹣1
2H2(g)+O2(g)═2H2O(l)△H2=﹣571.6kJmol﹣1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H3=﹣2599kJmol﹣1
根据盖斯定律,计算298K时由C(s,石墨)和H2(g)生成1mol C2H2(g)反应的反应热为:△H= .
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3﹣ . 两步反应的能量变化示
意图如图: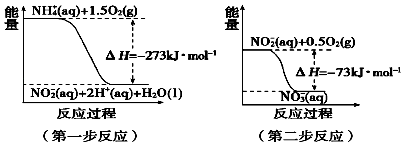
第一步反应是反应(填“放热”或“吸热”),原因是 .
查看答案和解析>>
科目: 来源: 题型:
【题目】关于化学电源的叙述中错误的是
A.化学电源是根据原电池的工作原理设计的
B.在干电池中,碳棒只起导电作用,并不参加化学反应
C.镍镉电池不能随意丢弃的主要原因是镍、镉的资源有限,价格昂贵
D.氢氧燃料电池是一种高效、环保的新型化学电源
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,其合成反应为CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
(1)下表列出了一些化学键断裂需要的能量数据,则CO(g)+2H2(g)![]() CH3OH(g) △H=________。
CH3OH(g) △H=________。
化学键 | H-H | C-O | C | H-O | C-H |
E(kJ·mol-1) | 436 | 343 | 1076 | 465 | 413 |
工业上用天然气为原料合成甲醇,分为两阶段。
I制备合成气:CH4+H2O(g)=CO+3H2。
(2)为解决合成气中H2过量CO不足问题,原料气中添加CO2,发生反应CO2+H2=CO+H2O。为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳体积比为___ 。
Ⅱ合成甲醇
实验室进行模拟合成实验。将1 molCO和2molH2通人密闭容器中,测得CO在不同温度下的平衡转化率与压强的关系如图所示:
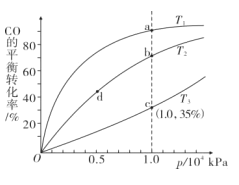
(3)比较T1、T2、T3的大小,并说明理由____。
(4)平衡常数K(b)___ K(d)、正反应速率v(a) ___v(b)(均填“大于”“小于”或“等于”)。
(5)c点时反应的压强平衡常数Kp=___ (kPa)-2(用数字表达式表示,Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(6)a点时,保持温度不变,将密闭容器的容积压缩刮原来的,对平衡体系产生的影响是______。
A. c(H2)减少 B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加 D.重新平衡时![]() 减小
减小![]() E. CH3OH的体积分数增加
E. CH3OH的体积分数增加
(7)科研人员设计了一种新型甲醇燃料电池,其电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-,该电池工作时的负极电极反应式为 ________。
查看答案和解析>>
科目: 来源: 题型:
【题目】人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是
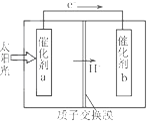
A. 该过程是将太阳能转化为化学能的过程
B. 催化剂a表面发生氧化反应,有O2产生
C. 催化剂a附近酸性减弱,催化剂b附近酸性增强
D. 催化剂b表面的反应是CO2+2H++2e一=HCOOH
查看答案和解析>>
科目: 来源: 题型:
【题目】物质A是生产各种塑料的重要单体,工业上采用物质B分解制备物质A的同时释放出氢气,其制备原理是:
B(g)A(g)+H2(g)△H=+125kJmol﹣1
(1)该反应的平衡常数表达式为K= . 随着温度的升高,K值(填“增大”、“减小”或“不变”).
(2)实际生产中常以高温水蒸气作为反应体系的稀释剂(稀释剂不参加反应).物质B的平衡转化率与水蒸气的用量、体系总压强关系如图.
①由图可得出:
结论一:其他条件不变,水蒸气的用量越大,平衡转化率越;
结论二:
②加人稀释剂能影响反应物B的平衡转化率的原因是: .
(3)某些工艺中,在反应的中途加入O2和特定的催化剂,有利于提高B的平衡转化率.试解释其原因: .
查看答案和解析>>
科目: 来源: 题型:
【题目】电解法生产锰时会产生大量的阳极泥,其主要成分为MnO2和Pb,还含有少量其他金属化合物。下图是回收电解锰阳极泥生产MnCO3的工艺流程。

已知:Al(OH)3、Mn(OH)2、MnCO3的Ksp分别为1.0×10-33、1.9×10-13、2.2×10-11。
(l)“还原酸浸”时氧化产物为CO2,发生反应的化学方程式为____。
(2)“还原酸浸”实验中,锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为 ____ 。

(3)滤液l中的阳离子组成见下表:
组成 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
浓度/(mol·L-1) | 0.85 | 2.4×10-3 | 1.0×10-2 | 2.0×10-3 |
“除杂”时先加MnO2,MnO2的作用为 ___。
再加氨水调节pH使杂质离子沉淀完全,通过计算说明Al3+沉淀完全时Mn2+是否开始沉淀 ___。
(4)“沉锰”时发生反应的离子方程式为 ___。
(5)“沉锰”的关键操作有2点:①将NH4HCO3溶液滴入MnSO4溶液中;②反应终点pH=7。如果颠倒试剂滴加顺序,将MnSO4溶液滴人NH4HCO3,溶液中,或反应终点pH>7可能造成同样的后果,该后果是____;如粜反应终点pH<7,可能的后果是______。
(6)从滤液2中回收得到的副产品的用途为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】ICl(氯化碘)红棕色液体,熔点13.9℃,沸点97 4℃,易水解,接触空气时能形成五氧化二碘,能与许多单质发生作用,溶于乙醇、乙醚等。某校研究性学习小组的同学拟用下列仪器制备氯化碘。回答下列问题:
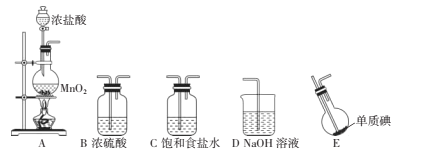
![]()
(1)检查A装置气密性的方法为 ___。
(2)上述装置,按气流方向连接的顺序为____(装置可重复使用),A中发生反应的离子方程式为____。
(3)C装置的作用是____。
(4)E装置的烧瓶反应时需放在水中,控制温度大约40℃,其目的是____。
(5)按上述连接好的装置进行实验,实验步骤如下:
①检查装置气密性后,装入药品 ②打开分液漏斗活塞 ③关闭分液漏斗活塞 ④停止加热E,充分冷却 ⑤水浴加热E
请按正确的顺序填入上述步骤的序号____。
(6)在A装置后可连接如图的装置,当反应结束关闭分液漏斗活塞后,关闭K,该装置的作用是____。
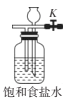
![]()
(7)IC1和水反应的化学方程式为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下反应4A(s)+3B(g)![]() 2C(g)+D(g)经2minB的浓度减少0.6mol·L-1,对此反应速率的表示正确的是( )
2C(g)+D(g)经2minB的浓度减少0.6mol·L-1,对此反应速率的表示正确的是( )
A. 用A表示的反应速率是0.4mol·L-1·min-1
B. 分别用B、C、D表示反应的速率,其比值是1∶2∶3
C. 2min末的反应速率v(B)=0.3mol·L-1·min-1
D. 在这2min任意一段时间内用B和C表示的正反应速率的值随时间变化都是逐渐减小的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com