
科目: 来源: 题型:
【题目】同温同压下,向两个体积可变的密闭容器中分别充满等质量的O2、O3气体,下列说法正确的是
A. 两种气体的密度之比是3∶2 B. 两个容器的体积之比为2∶3
C. 两种气体的分子数目相等 D. 两气体的物质的量之比为3∶2
查看答案和解析>>
科目: 来源: 题型:
【题目】某短周期非金属元素,其原子核外最外层电子数是次外层电子数的一半,该元素( )
A.在自然界中以化合态的形式存在
B.单质常用作半导体材料
C.最高价氧化物不与任何酸反应
D.气态氢化物比甲烷稳定
查看答案和解析>>
科目: 来源: 题型:
【题目】铵盐在工农业生产中有着重要的用途。回答下列问题:
Ⅰ.某化学兴趣小组欲从下列装置中选取必要的装置制取(NH4)2SO4溶液: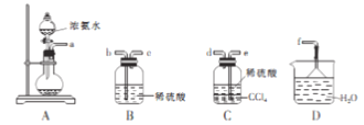
(1)用装置A制备氨气时,检验a处是否有氨气产生的方法是____________________。
(2)制取(NH4)2SO4 溶液时仪器连接的顺序(用接口字母和箭号“→”表示)是a→______________(所选装置不重复使用)。
(3)将装置C中两种液体分离,所需的主要玻璃仪器是______________________。
Ⅱ.为提高氯化铵的经济价值,我国化学家设计了利用用氢氧化镁热分解氯化铵制干燥氨气并得到碱式氯化镁[Mg(OH)Cl]的工艺。某同学根据该原理设计的实验装置如图:
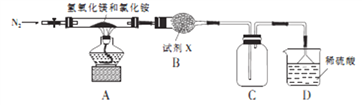
(4)氯化铵的电子式为_________________,装置A中发生反应生成碱式氯化镁的化学方程式为_____________________。
(5)装置B中试剂X为_______________________。
(6)上述装置图中有一处错误,请指出改正的方法:_______________________。
(7)MgCl2·6H2O在空气中加热,生成Mg(OH)Cl,若由MgCl2·6H2O制备无水MgCl2,实验方法为________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】现有镁铝铜合金5.2g,加入过量的盐酸中,在标准状况下放出氢气5.6L,反应后过滤得沉淀0.1g。若将此合金放入过量的烧碱溶液中,反应后,在标准状况下大约能产生多少升氢气?镁铝铜的质量各为多少克? (写计算过程)___________________
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定量的SO2(g)和O2(g)分别通入体积为2L的恒容密闭容器中,在不同温度下进行反应:2SO2(g)+ O2(g)![]() 2SO3 △H<0。得到如表中的两组数据,下列说法不正确的是
2SO3 △H<0。得到如表中的两组数据,下列说法不正确的是
实验编号 | 温度/℃ | 平衡常数/mol-1·L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
A. T1、T2的关系:T1 > T2
B. x= 1.6,y=0.2 ,t<6
C. K1、K2的关系:K2>K1
D. 实验1在前6min的反应速率υ(SO2)=0.2 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是教师在课堂中演示的两个实验装置(铁架台等辅助仪器略去)

请回答下列问题
(1)实验一的实验目的是 _____________________________________ , 实验过程中可以观察到烧杯中的现象是_______________________________________________________ ,加热后试管中发生反应的化学方程式是: ____________________________
(2)实验二用来验证Na2O2与CO2的反应,观察到的实验现象是:包有Na2O2的棉花燃烧。Na2O2与CO2的反应的化学方程式________________________________________ ,该实验可以得出许多结论,请你写出由该实验得出的两个结论。
结论1:__________________________________
结论2:__________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】室温时,体积为1mL、浓度均为0.1mol·L-1的两种常见物质X(OH)n、K2AO3的溶液分別加水稀释至体积为VmL,pH随lgV的变化情况如下图所示。下列叙述错误的是( )
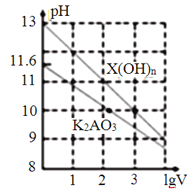
A. n=1
B. H2AO3的二级电离常数Ka2约为1.0×10-10.2
C. pH=10的两种溶液中水的电离程度相同
D. 升高温度,K2AO3溶液pH增大,X(OH)n溶液pH减小
查看答案和解析>>
科目: 来源: 题型:
【题目】I.(1)图I表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,则量筒中液体的体积是①,由于放置位置不当读数时俯视,读出的数值为②则①②的正确数值为___________

A①3.2mL、②小于3.2mL B.①4.8mL、②大于4.8mL
C.①3.2mL、②大于3.2mL D.①4.8mL、②小于4.8mL
(2)实验室需配制1mol·L-1的NaOH溶液200mL,在用托盘天平称取NaOH固体时,天平读数为________填代号,下同)。
A.大于8.0g B.小于8.0g C.8.0g
II.表示溶液浓度的方法通常有两种;溶液中溶质的质量分数(W)和物质的量浓度 (c),因此在配制溶液时,根据不同的需要,有不同的配制方法。请完成下列填空题。
(1)用10%(密度为1.01g/cm3)的氢氧化钠溶液配制成27.5g 2%的氢氧化钠溶液。
①计算:需_________g 10%(密度为1.01g/cm3)的氢氧化钠溶液
②量取:用_________mL量筒量取10%的氢氧化钠溶液
(2)把98%(密度为1.84g/cm3)的浓硫酸稀释成2mol/L的稀硫酸100mL,回答下列问题:
①需要量取浓硫酸_______ mL
②下列实验操作使配制的溶液浓度偏的是__________
A.容量瓶洗涤后未干燥
B.量取溶液时,仰视刻度线
C.装入试剂瓶时,有少量溶液溅出
D.没有洗涤烧杯和玻璃棒
E.定容时,加水不慎超出刻度线,又倒出一些
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com