
科目: 来源: 题型:
【题目】实验室欲配制80 g质量分数为10%的氢氧化钠溶液,如图是配制该氢氧化钠溶液的实验操作示意图。
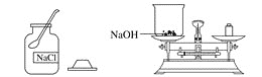
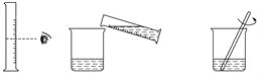
实验步骤
(1)计算:需要氢氧化钠固体__________g,水__________mL(水的密度为1 g·mL-1)。
(2)称量:用托盘天平称取氢氧化钠固体,用规格为__________(填“10mL”“50mL”或“100mL”)的量筒量取所需要的水,倒入盛有氢氧化钠的烧杯中。
(3)溶解:用玻璃棒搅拌,使氢氧化钠固体完全溶解。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物M是二苯乙炔类液晶材料的一种,最简单二苯乙炔类化合物是![]() 。以互为同系物的芳香烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
。以互为同系物的芳香烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
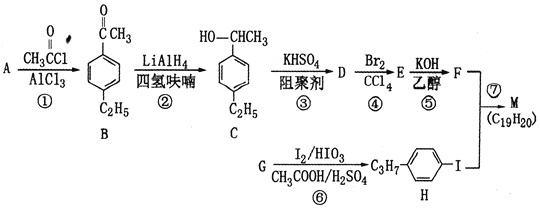
回答下列问题:
(1)G的结构简式为________________。
(2)C中含有的官能团名称是________________________。
(3)反应②的反应类型是________________,反应⑥的反应类型是________________。
(4)反应⑤的化学方程式为____________________。
(5)能同时满足下列条件的B的同分异构体有________种(不考虑立体异构)。
①苯环上有两个取代基 ②能发生银镜反应
写出其中核磁共振氢谱为5组峰,且峰面积之比为6:2:2:1:1的同分异构体的结构简式_______。
(6)参照上述合成路线,设计一条由苯乙烯和甲苯为起始原料制备![]() 的合成路线。_________________________
的合成路线。_________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋植物如海带和海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋中提取碘的流程如下:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
某化学兴趣小组将上述流程②、③设计成如下图所示操作。
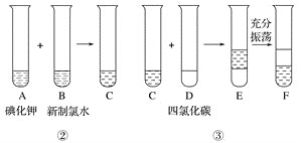
已知过程②发生反应的化学方程式为Cl2+2KI===2KCl+I2
回答下列问题:
(1)写出提取过程①、③中实验操作的名称:①____________,③____________。
(2)在灼烧过程中,使用到的实验仪器有酒精灯、____________、____________(除泥三角外)。
(3)F中下层液体的颜色为________色,上层液体中溶质的主要成分为____________。
(4)从F中得到固态碘还需进行的操作是_______________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,E是具有果香气味的烃的衍生物。A、B、C、D、E在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
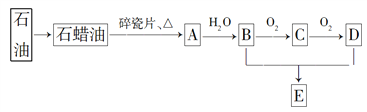
(已知乙醛在一定条件下可被氧化生成乙酸)
(1)丁烷是由石蜡油获得A的过程中的中间产物之一,它的一种同分异构体中含有三个甲基,则这种同分异构体的结构简式为________。
(2)B、D分子中官能团的名称分别是________、________,A→B的反应类型是________。
(3)写出反应A→B 、B→C的化学方程式:____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】研究物质制备是化学学科的任务之一。
(1)请从Cl2、H2、CO2、NO、NH3五种气体中选择一种气体,该气体在实验室可用如图装置制取、净化、收集(可以含水蒸气),制取该气体的化学方程式为____________。

(2)已知: +4NaOH→NaCl+CH2=CH2↑+Na3PO4+3H2O,可用下述装置制取1,2-二溴乙烷(无色液体,密度2.18g·cm-3,熔、沸点分别为9.79℃、131.4 ℃,不溶于水);试管d中装有液溴(表面覆盖少量水)。
+4NaOH→NaCl+CH2=CH2↑+Na3PO4+3H2O,可用下述装置制取1,2-二溴乙烷(无色液体,密度2.18g·cm-3,熔、沸点分别为9.79℃、131.4 ℃,不溶于水);试管d中装有液溴(表面覆盖少量水)。

①e装置的作用是_________;当观察到_________现象时,试管d中反应基本结束;
②若用冰水代替烧杯中的冷水,可能引起的不安全后果是_________;
③实验后,需通过水洗、________、水洗、用干燥剂干燥、蒸馏等操作对试管d中的粗产品进行精制:
④实验消耗40%乙烯利(摩尔质量为M)溶液50g,制得产品m g,则乙烯利合成1,2-二溴乙烷的产率为____________(用含M、m的代数式表示);
⑤设计实验证明,反应后烧瓶中的混合溶液含有C1-、PO43-。简述实验方案:_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积,请回答以下问题。
该小组设计的简易实验装置如图所示:
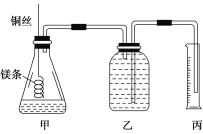
该实验的主要操作步骤如下:
①配制100 mL 1.0 mol/L的盐酸溶液;
②用________(填仪器名称并注明规格)量取10.0 mL 1.0 mol/L的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请将上述步骤补充完整并回答下列问题。
(1)用文字表述实验步骤④中检查装置气密性的方法:
___________________________________________________
(2)实验步骤⑤中应选用________(填序号)的量筒。
A.100 mol B.200 mL C.500 mL
读数时除恢复到室温外,还要注意_________________________________________。
(3)若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算式为Vm=________,若未除去镁条表面的氧化膜,则测量结果________(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列五种短周期元素的电离能数据(单位:kJ·mol-1),回答下列问题。

(1)在这五种元素中,最可能处于同一族的两种元素是______________(填元素符号),S元素最可能是________区元素。
(2)基态Q元素原子的价电子排布式是___________。Q和T同周期,化合物QT中T元素的化合价为____________;第一电离能介于Q、T之间的同周期元素有____________种。
(3)化合物RT3中含有的化学键类型为____________,RT3中阴离子的几何构型为__________。
(4)下列元素中,化学性质和物理性质与U元素相似的是________(填序号)。
A.硼 B.铍 C.锂 D.氦 E.碳
(5)R的某种氧化物X的晶胞结构如图所示,晶胞参数a=0.566nm,X的化学式为________:晶体X的密度是____________(g·cm-3)。

查看答案和解析>>
科目: 来源: 题型:
【题目】ag 硝酸钾溶于bg水,形成VmL饱和溶液。下列关系式错误的是( )
A. 该溶液的物质的量浓度:c(KNO3)=![]() mol·L-1
mol·L-1
B. 该溶液的质量分数:w(KNO3)=![]() %
%
C. 20 ℃时KNO3的溶解度S=![]() g
g
D. 该溶液的密度ρ=![]() g·L-1
g·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】消除SO2、NOx对大气造成的污染具有重要现实意义。
(1)将一定量的空气样品用蒸馏水溶解制成待测试样(忽略OH-)。常温下测得该试样的组成及其浓度如下表:
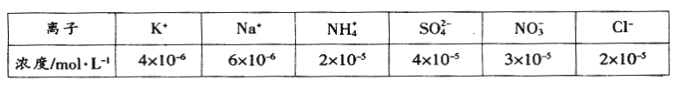
根据表中数据判断该试样的pH=____________。
(2)为减少SO2的排放,可将煤转化为清洁气体燃料,或将含SO2的烟气洗涤。
①已知:H2(g)+![]() O2(g)=H2O(g) △H=-241.8 kJ·mol-1
O2(g)=H2O(g) △H=-241.8 kJ·mol-1
C(s)+![]() O2(g)=CO(g) △H=-110.5 kJ·mol-1
O2(g)=CO(g) △H=-110.5 kJ·mol-1
写出焦炭与水蒸汽反应的热化学方程式____________。
②下列可作为洗涤含SO2烟气的洗涤剂是_________(填序号)。
A.浓氨水 B.碳酸氢钠饱和溶液
C.FeCl2饱和溶液 D.酸性CaCl2饱和溶液
(3)实验室中研究有无CO对NO的有效消除程度,测得NO的转化率随温度的变化曲线如图所示。当无CO时,温度超过750K,发现NO的分解率降低,其可能的原因是________。当有CO且n(CO)/n(NO)=1时,为更好地除去NO,应控制的最佳温度为________K左右。
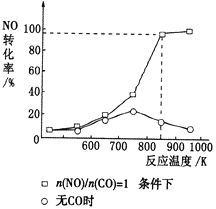
(4)用活性炭可处理大气污染物NO。在 5L密闭容器中加入NO和活性炭(假设无杂质),一定条件下生成气体E和F。当温度分别在T1℃和T2℃时,测得各物质平衡时物质的量(n/mol)如下表:
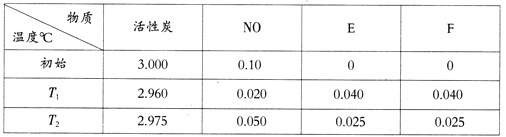
①写出NO与活性炭反应的化学方程式____________;
②若T1<T2,则该反应的△H________0(填“>”、“<”或“=”);
③上述反应T1℃时达到化学平衡后再通入0.1 mol NO气体,则达到新化学平衡时NO的转化率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com