
科目: 来源: 题型:
【题目】氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲。黑火药在发生爆炸时,发生如下反应:2KNO3+3C+S=K2S+N2↑+3CO2↑。其中被氧化的元素是____________,还原产物是____________。
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为4CuI+Hg=Cu2HgI4+2Cu。
①上述反应产物Cu2HgI4中,Cu元素显________价。
②以上反应中的氧化剂为________,当有1 mol CuI参与反应时,转移电子________mol。
③标明上述反应电子转移的方向和数目______________________________。
(3)工业上常用酸性高锰酸钾溶液处理含有CuS和Cu2S的矿物,其反应原理如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2↑+6Mn2++14H2O
根据上述反应原理,某学习小组用400 mL 0.075 mol·L-1的酸性高锰酸钾溶液处理2 g含有CuS和Cu2S的混合物。反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350 mL 0.1 mol·L-1的(NH4)2Fe(SO4)2溶液完全反应。
①配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
______MnO4-+______Fe2++______H+=______Mn2++______Fe3++______H2O。
②KMnO4溶液与固体混合物反应后,剩余KMnO4的物质的量为________mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)铁钉在氯气中被锈蚀为棕褐色物质FeCl3,而在盐酸中生成浅绿色的FeCl2溶液。在Cl2、Cl-、H+中,具有氧化性的是____________,其中氧化性最强的是____________。
(2)盐酸在不同的反应中可以分别表现出酸性、氧化性和还原性。现在有如下三个反应,请写出盐酸在三个反应中分别起何种作用:
①Zn+2HCl===ZnCl2+H2↑____________________;
②NaOH+HCl===NaCl+H2O__________________;
③2HCl![]() H2↑+Cl2↑________________________。
H2↑+Cl2↑________________________。
(3)铁钉在氯气中被锈蚀成棕褐色物质FeCl3,而在盐酸中生成浅绿色溶液(FeCl2);向浓盐酸中滴加KMnO4溶液产生淡黄绿色气体(Cl2)。在Cl2、H+、![]() 中,__________________氧化性最强。
中,__________________氧化性最强。
(4)高锰酸钾与氢溴酸溶液可以发生下列反应:2KMnO4+16HBr===5Br2+2MnBr2+2KBr+8H2O。其中还原剂是________________。若消耗15.8 g氧化剂,则被氧化的还原剂的质量是______________g。HBr的作用是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对下列事实的解释正确的是()
A.SO2能使品红溶液褪色,说明SO2具有漂白性
B.向蔗糖中加入浓硫酸后出现发黑现象,说明浓H2SO4具有吸水性
C.用HF来刻蚀玻璃,说明SiO2是碱性氧化物
D.雨水显酸性是因为吸收了空气中的CO2,pH小于1的雨水称为酸雨
查看答案和解析>>
科目: 来源: 题型:
【题目】在2Mg+O2![]() 2MgO的化学反应中:
2MgO的化学反应中:
(1)氧元素的化合价由0价降低为________价,降低了________价;氧气得到电子的总数为________。
(2)镁原子失去电子的总数为________,1 mol Mg反应时转移电子的物质的量为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铜的相关化合物在生产生活中具有重要的作用。
回答下列问题:
(1)铜元素在周期表中的位置是____,基态铜原子中,核外电子占据最高能层的符号是___,占据该最高能层的电子数为_________。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu6Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于___(填“晶体”或”非晶体”)。
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为_____。
(SCN)2对应的酸有硫氰酸(H-S-C≡N)、异硫氰酸(H-N=C=S)两种,理论上前者沸点低于后者,其原因是__________。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为__。
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为anm,该金属互化物的密度为_____________(用含a、NA的代数式表示)g/cm3。
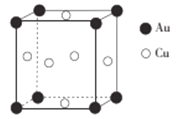
查看答案和解析>>
科目: 来源: 题型:
【题目】某浅绿色晶体X[x(NH4)2SO4·yFeSO4·zH2O]在分析化学中常用作还原剂. 为确定其组成,某小组同学进行如下实验.
I.NH4+的测定
采用蒸馏法,蒸馏装置如图所示。
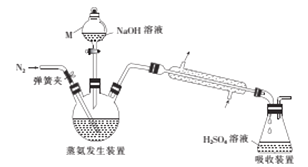
相关的实验步骤如下:
①准确称取58.80g晶体X,加水溶解后,将溶液注入三颈烧瓶中;
②准确量取50.00mL3.0300molL-1H2SO4溶液于锥形瓶中;
③向三颈烧瓶中加入足量NaOH溶液,通入氮气,加热,蒸氨结束后取下锥形瓶;
④用0.120molL-1NaOH标准溶液滴定锥形瓶中过量的硫酸,滴定终点时消耗25.00mL NaOH标准溶液.
(1)仪器M的名称为__________。
(2)步骤③中,发生的氧化还原反应的化学方程式为____________。蒸氨结束后,为了减少实验误差,还需要对直形冷凝管进行“处理”,“处理”的操作方法是_____________。
(3)步骤④中,若振荡时锥形瓶中有液体溅出,则所测得的n(NH4+)的值将______(填“偏大”“偏小”或“不变”)。
II.SO42-含量的测定
采用重量分析法,实验步骤如下:
①另准确称取58.80g晶体X 于烧杯中,加水溶解,边搅拌边加入过量的BaCl2溶液;
②将得到的溶液用无灰滤纸(灰分质量很小,可忽略)过滤,洗涤沉淀3~4次;
③用滤纸包裹好沉淀取出,灼烧滤纸包至滤纸完全灰化;
④继续灼烧沉淀至恒重、称量,得沉淀质量为69.90g。
(4)步骤①中,判断BeCl 溶液已过量的实验操作和现象是___________。
(5)步骤②中,采用冷水洗讓沉淀,其主要目的是___________。
(6)结合实验Ⅰ、Ⅱ通过计算得出晶体X的化学式为__________。实验I 的步骤①中,溶液中离子溶度由大到小的顺序为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】钚(23994Pu)是制造威力更大原子弹的良好原料。下列有关说法错误的是
A. 原子序数为94 B. 电子数为94 C. 中子数为94 D. 质量数为239
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨厂和硝酸厂的烟气中含有大量的氮氧化物(NOx),脱硝通常是指将烟气中的氮氧化物转化为无毒无害的物质的化学过程。
(1)选择性催化还原技术(SCR)是目前最成熟的脱硝技术,即在金属催化剂的作用下,用还原剂(如NH3)选择性的与NOx反应生成N2和H2O。
已知:4NH3(g)+5O2(g)4NO(g)+6H2O(g)△H=-905.5kJmol-1
N2(g)+O2(g)2NO(g) △H=+180kJmol-1
脱硝反应:4NH3(g)+6NO(g)5N2(g)+6H2O(g)的△H=_______kJmol-1
(2)将amolN2和3amolH2通入一密闭容器中在不同的温度和压强下发生反应:N2(g)+3H2(g)2NH3(g)。测得平衡体系中NH3的物质的量的分数如图所示。
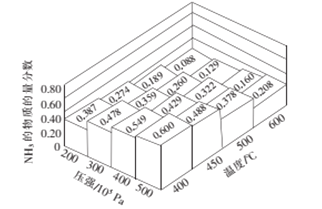
①下列可提高氨气产率的途径是__________。
A.尽量提高反应温度 B.对原料气适当加压
C.采用适当的催化剂 D.将氨气液化,不断移出液氨
②上图所示平衡体系中当NH3的物质的量分数分别为0.549和0.429时,该反应的平衡常数分别为K1和K2,则K1________K2(填写“>”,“<”或“=”)。当NH3的物质的量分数为0.600时,容器的体积为2L,此时该反应的化学平衡常数K=________。
(3)常温下,将NO和H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中其物质转化过程如图所示,
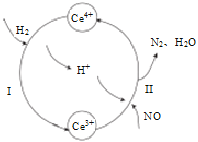
①反应I中氧化剂与还原剂的物质的量之比为_______。
②写出该过程的总化学反应方程式_____________________________________。
(4)直接电解吸收也是脱硝的一种方法,先用6%的稀硝酸吸收NOx,会生成HNO2(一种一元弱酸),再将吸收液导入电解槽中进行电解,使之转化为硝酸,其电解装置如图所示。
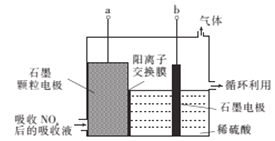
①图中b应连接电源的_______(“正极”或“负极”)。
②阳极的电极反应式为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com