
科目: 来源: 题型:
【题目】某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是( )
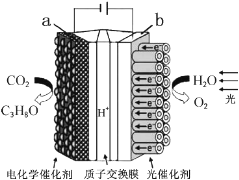
A. 该装置将化学能转化为光能和电能
B. 该装置工作时,H+从b极区向a极区迁移
C. 每生成1molO2,有44g CO2被还原
D. a电极的反应为:3CO2+18H+-18e-=C3H8O+5H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】氮、硫及其化合物在工农业生产生活中有着重要作用。回答下列问题:
(1)有人设想利用CO还原SO2。已知S和CO的燃烧热分别是296.0 kJ·mol1、283.0 kJ·mol1,请写出CO还原SO2的生成CO2和S(s)热化学方程式___________________________________。
(2)某科研小组研究臭氧氧化碱吸收法同时脱除SO2和NO工艺,氧化过程反应原理及反应热、活化能数据如下:
反应Ⅰ:NO(g)+O3(g)![]() NO2(g)+O2(g) △H1=-200.9 kJmol1 Ea1=3.2 kJmol1
NO2(g)+O2(g) △H1=-200.9 kJmol1 Ea1=3.2 kJmol1
反应Ⅱ:SO2(g)+O3(g)![]() SO3(g)+O2(g) △H2=-241.6 kJmol1 Ea2=58 kJmol1
SO3(g)+O2(g) △H2=-241.6 kJmol1 Ea2=58 kJmol1
已知该体系中臭氧发生分解反应:2O3(g)![]() 3O2(g)。请回答:
3O2(g)。请回答:
其它条件不变,每次向容积为2 L的反应器中充入含2.0 mol NO、2.0 mol SO2的模拟烟气和4.0 mol O3,改变温度,反应相同时间t后体系中NO和SO2的转化率如图所示:

①由图1可知相同温度下NO的转化率远高于SO2,结合题中数据分析其可能原因_______。
②下列说法正确的是________。
A.Q点一定为平衡状态点
B.温度高于200℃后,NO和SO2的转化率随温度升高显著下降、最后几乎为零
C.其它条件不变,若扩大反应器的容积可提高NO和SO2的转化率
D.臭氧氧化过程不能有效地脱除SO2,但后续步骤碱吸收可以有效脱硫
③假设100℃时P、Q均为平衡点,此时反应时间为5min,发生分解反应的臭氧占充入臭氧总量的10%,则体系中剩余O3的物质的量是________mol;SO2的平均反应速率为________;反应Ⅰ在此时的平衡常数为_______________。
(3)以连二硫酸根(S2O42-)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:

①ab是_______离子交换膜(填“阳”或“阴”)。阴极区的电极反应式为_____________。
②若NO吸收转化后的产物为NH4+,通电过程中吸收4.48LNO(标况下),则阳极可以产生____mol气体。
查看答案和解析>>
科目: 来源: 题型:
【题目】若定义pAg=-lgc(Ag+),pCl=-1gc(C1-),根据不同温度下氯化银饱和溶液的PAg和pCl 可绘制图像如右图所示,且己知氯化银的溶解度随温度的升高而增大,根据该图像,下列表述正确的是

A. T3 >T2 >T1
B. 将A点的溶液降温,可能得到C 点的饱和溶液
C. 向B点所表示的溶液中加入氯化钠溶液,溶液可能改变至D点
D. A点表示的是T 1温度下的不饱和溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下图所示为按树状分类法对一组物质进行的分类。回答下列问题

①类别1_________,类别2_________,分类标准2_________。
②上述物质中属于电解质的是_________,非电解质的是_________。
③向NaHSO4溶液中加Fe可产生气体,对应的离子方程式_________。
④将NaHSO4溶液和Ba(OH)2溶液混合,恰好呈中性,对应的离子方程式为__________。
(2)请对以下过程形成的分散系进行分类:
①花生油加入到水中后充分搅拌;②向蒸馏水中加入硝酸钾至恰好饱和;
③饱和氯化铁溶液中加入氢氧化钠溶液;④氢氧化钡溶液中通入过量的CO2;
⑤用滤纸过滤氢氧化铁胶体后得到的滤液;⑥将纳米材料分散在塑料中制备复合材料;⑦碘水和酒精的混合物。
属于浊液的是________(填序号,下同);属于溶液的是________;属于胶体的是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化铬(Cr2O3)主要用于冶炼金属铬、有机化学合成的催化剂等。工业上是以铬铁矿[主要成份为Fe(CrO2)2,还含有Al2O3、SiO2等杂质]为主要原料进行生产,其主要工艺流程如下:

(1)亚铬酸亚铁[Fe(CrO2)2]中Cr的化合价是___________。
(2)焙烧时的主要反应为:4FeO·Cr2O3+8Na2CO3+7O2![]() 8Na2CrO4+2Fe2O3+8CO2,其中被氧化的元素为______,每产生32 g Fe2O3,转移电子的数目为_______。该步骤不能使用陶瓷容器,原因是_____________________________。
8Na2CrO4+2Fe2O3+8CO2,其中被氧化的元素为______,每产生32 g Fe2O3,转移电子的数目为_______。该步骤不能使用陶瓷容器,原因是_____________________________。
(3)操作I包括过滤与洗涤,简述实验室中洗涤沉淀的操作:___________。
(4)硫磺在与铬酸钠的反应中转化为硫代硫酸钠,反应的离子方程式为__________。滤渣中除Al(OH)3外还有__________(填化学式)。
(5)某工厂用448 kg铬铁矿粉[含Fe(CrO2)280%]制备Cr2O3,最终得到产品182.4 kg,产率为______%。
(6)Cr3+也有一定毒性,会污染水体,常温下要除去废液中多余的Cr3+,调节pH至少为_______,才能使铬离子沉淀完全。已知Cr(OH)3的溶度积常数为1.0×10-32。
查看答案和解析>>
科目: 来源: 题型:
【题目】从某含Br-废水中提取Br2的过程包括:过滤、氧化、萃取(需选择合适萃取剂)及蒸馏等步骤。
已知:①2NaOH+Cl2==NaCl+NaClO+H2O
②Br2极易溶于四氯化碳和正十二烷
物质 | Br2 | CCl4 | 正十二烷 |
密度/g·cm-3 | 3.119 | 1.595 | 0.753 |
沸点/℃ | 58.76 | 76.8 | 215~217 |
在水中溶解性 | 微溶 | 难溶 | 难溶 |

下列说法不正确的是
A. 甲装置中Br-发生的反应为:2Br-+Cl2===Br2+2Cl-
B. 甲装置中NaOH溶液每吸收1个Cl2,转移1个e-
C. 用乙装置进行萃取,溶解Br2的有机层在下层
D. 用丙装置进行蒸馏,先收集到的是Br2
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,分别向体积相同、浓度均为0.1 mol/L的MOH、ROH两种碱溶液中不断加水稀释,溶液的pH与溶液浓度的对数(lgc)间的关系如图。下列说法错误的是

A. Kb(MOH)的数量级为10-5
B. a、b两点溶液中,水的电离程度:a<b
C. 等体积等浓度的ROH和MCl混合后所得溶液中:c(OH-)>c(H+)
D. 用相同浓度的盐酸分别中和a、b两点溶液,消耗盐酸体积:Va>Vb
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,水只表现出还原性的是
A. 2Na+2H2O=2NaOH+H2↑
B. 2F2+2H2O=4HF+O2
C. 3NO2+H2O=2HNO3+NO
D. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】在300 mL的密闭容器中,放入镍粉并充入一定量的CO气体,一定条件下发生反应:Ni(s)+4CO(g) ![]() Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
Ni(CO)4(g),已知该反应平衡常数与温度的关系如表所示:
温度/℃ | 25 | 80 | 230 |
平衡常数 | 5×104 | 2 | 1.9×10-5 |
下列说法正确的是( )
A. 上述生成Ni(CO)4(g)的反应为吸热反应
B. 25 ℃时反应Ni(CO)4(g) ![]() Ni(s)+4CO(g)的平衡常数为0.5
Ni(s)+4CO(g)的平衡常数为0.5
C. 在80 ℃时,测得某时刻,Ni(CO)4、CO浓度均0.5 mol/L,则此时v正>v逆
D. 80 ℃达到平衡时,测得n(CO)=0.3 mol,则Ni(CO)4的平衡浓度为2 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com