
科目: 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是 ( )


A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目: 来源: 题型:
【题目】反应4A(g)+5B(g)![]() 4C(g)+6D(g)在0.5 L密闭容器中进行,0.5 min后,A减少了0.90 mol,则反应的速率可表示为( )
4C(g)+6D(g)在0.5 L密闭容器中进行,0.5 min后,A减少了0.90 mol,则反应的速率可表示为( )
A. v(A)=3.6mol·L-1·s-1B. v(B)=0.030 mol·L-1·s-1
C. v(C)=0.03 mol·L-1·s-1D. v(D)=0.09 mol·L-1·s-1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的( )
A. 玛瑙、水晶、钻石等装饰品的主要成分不相同
B. 铁粉可作食品袋内的脱氧剂
C. 漂白液、漂白粉、漂粉精的成分尽管不同,但漂白原理是相同的
D. 浓硫酸可刻蚀石英制艺术品
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A。其结构如图4所示:

(1)Cu元素基态原子的外围电子排布式为______________。
(2)元素C、N、O的第一电离能由大到小排列顺序为_______________。
(3)配合物A中碳原子的轨道杂化类型为_______________________。
(4)1mol氨基乙酸钠(H2N-CH2-COONa)含有![]() 键的数目为____________mol。
键的数目为____________mol。
(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体:____________(写化学式)。
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图2所示,则该化合物的化学式是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等。
(1)Fe2+基态核外电子排布式为______。
(2)科学研究表明用TiO2作光催化剂可将废水中CN-转化为OCN-、并最终氧化为N2、CO2。OCN-中三种元素的电负性由大到小的顺序为_______。
(3)与CN-互为等电子体的一种分子为______(填化学式);1mol Fe(CN)63-中含有σ键的数目为______。
(4)铁的另一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于_______(填晶体类型)。
(5)铁铝合金的一种晶体属于面心立方结构,其晶胞可看成由8个小体心立方结构堆砌而成。已知小立方体如图所示。该合金的化学式为_______。
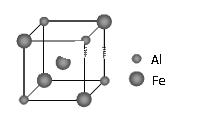
查看答案和解析>>
科目: 来源: 题型:
【题目】在学习了元素周期律之后,某化学实验小组设计了如下实验,验证碳元素的非金属性比硅元素的非金属性强,请回答下列问题:
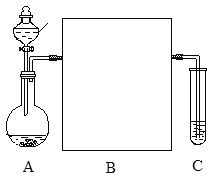
(1)装置A的分液漏斗中盛装的试剂是_____,烧瓶中加入块状固体是_____。
(2)装置C中盛放的试剂是_____(选填字母)
A.Na2CO3溶液 B.Na2SiO3溶液 C.NaOH溶液
(3)画出实线框内的实验装置图,并注明所加试剂,该装置的作用是_____,
(4)C中实验现象为_____,化学反应方程式是_____。若没有B装置,虽然C中出现的现象相同,但也不能得出正确结论,原因是_____。
(5)从碳、硅在周期表中的位置角度,简要分析碳元素的非金属性比硅元素的非金属性强的原因是_____。
(6)还有哪些事实能够说明碳元素的非金属性比硅元素的非金属性强(试举一例)_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关乙烯和乙烷的说法中错误的是![]()
![]()
A. 乙烯是平面分子,乙烷分子中所有原子不可能在同一平面内
B. 溴的四氯化碳溶液和酸性![]() 溶液都可以鉴别乙烯和乙烷
溶液都可以鉴别乙烯和乙烷
C. 溴的四氯化碳溶液和酸性![]() 溶液都可以除去乙烷中混有的乙烯
溶液都可以除去乙烷中混有的乙烯
D. 乙烯的化学性质比乙烷的化学性质活泼
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E 是五种短周期元素,其中A、B、C 在同一周期。0.5molA 元素的原子失去9.03×1023 个电子后,转化为具有与氖原子相同电子层结构的离子,A 元素最高价氧化物的水化物能分别与B、C 元素最高价氧化物的水化物反应,且都生成盐,B 元素原子各层电子数均为偶数,C 元素原子最外层电子数比最内层少一个。D 元素的一种同位素原子中没有中子。E 元素与其它四种元素均不在同一周期,E 的最高价氧化物的水化物是一种强酸。请回答下列问题:
(1)A 离子结构示意图为:_____;E 元素在周期表中的位置是_____;
(2)用电子式表示B 与C 形成化合物的过程:_____;
(3)A 元素最高价氧化物的水化物与 C 元素最高价氧化物的水化物反应的离子方程式是:_____;
(4)E 与D 形成的某种化合物,其水溶液呈碱性,其原因是_____(用离子方程式作答)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com