
科目: 来源: 题型:
【题目】Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究。利用如图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件。下列判断正确的是

A. e、f两管中的试剂可以分别是浓氨水和NaOH固体
B. 玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应
C. c、d两根导管都必须插入BaCl2溶液中,保证气体与Ba2+充分接触
D. Y形管乙中产生的为氧化性气体,将BaSO3氧化为BaSO4沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于元素周期律和元素周期表的论述中正确的是( )。
A.同一主族的元素从上到下金属性逐渐减弱
B.元素周期表是元素周期律的具体表现形式
C.同一周期从左到右,元素原子半径逐渐增大
D.非金属元素的最高正化合价等于它的负化合价的绝对值
查看答案和解析>>
科目: 来源: 题型:
【题目】2011年3月日本地震引起福岛核反应堆事故,冷却反应堆需要大量的水。下列有关说法正确的是( )。
A.H2O分子中只含有非极性共价键
B.H2O分子中只含有极性共价键
C.水分子间只存在氢键
D.冷却反应堆用水在地球上常温下是固态
查看答案和解析>>
科目: 来源: 题型:
【题目】Na2CO3溶液与盐酸反应过程中的能量变化示意图如下,下列选项错误的是
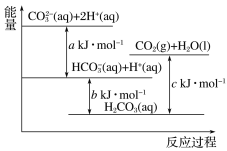
A. 等浓度、等体积的碳酸钠溶液和碳酸氢钠溶液分别与足量的盐酸反应均有气泡产生
B. CO32-(aq)+2H+(aq)=CO2(g)+H2O(l) 是放热反应
C. HCO3-(aq)+H+(aq)=CO2(g)+H2O(l) 是放热反应
D. CO2(g)+H2O(l)=H2CO3(aq) 是放热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在工业上,铝常用于冶炼难熔金属,这一用途主要是由于铝( )
A.具有强还原性,反应中放出大量的热
B.高温时在空气中能燃烧
C.具有良好导热性
D.反应后生成熔点更高的氧化铝
查看答案和解析>>
科目: 来源: 题型:
【题目】为测定含镁3%~5%的铝镁合金中镁的质量分数,设计了2种实验方案,说法不正确的是
方案一:镁铝合金加入足量的氢氧化钠溶液中充分反应后过滤,测定剩余固体质量;
方案二:称量m g铝镁合金粉末,放在图中惰性电热板上,通电使其充分灼烧。测得固体质量增重。
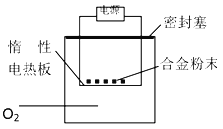
A. 方案一中若称取5.4 g合金粉末样品,投入V mL 2.0 mol/L NaOH溶液中反应,则V≥100 mL
B. 方案一中测定剩余固体质量时,过滤后未洗涤固体就干燥、称量,则镁的质量分数偏高
C. 方案二中欲计算镁的质量分数,实验中还需测定灼烧后固体的质量
D. 方案二中若用空气代替O2进行实验,则测定结果偏高
查看答案和解析>>
科目: 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,下列叙述正确的是

A. 两烧杯中锌片质量均减小,铜片质量均不变
B. 甲烧杯中锌片和铜片表面均产生气泡,乙烧杯中只有锌片表面产生气泡
C. 甲烧杯中铜片失去电子,乙烧杯中铜不参与化学反应
D. 当转移1mol电子时,甲烧杯中产生氢气比乙烧杯中产生的氢气多
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关合金的叙述中正确的是( )
A.合金的密度比各成分金属小
B.合金的抗腐蚀性能都很好
C.合金的导电性比各成分金属强
D.合金的种类和性能与成分有关
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)工业上以粗铜为原料采取如下图所示流程制备硝酸铜晶体:

①在步骤a中,还需要通入氧气和水,其目的是___________________________。
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在____________范围。
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Fe3+ Cu2+ | 1.9 4.7 | 3.2 6.7 |
不用加水的方法调节溶液pH的原因是_______________________________________。
③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明)
_________________________________________________________________________。
(2)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是______________________。
(3)下图是某小组同学查阅资料所绘出的硝酸铜晶体[ Cu(NO3)2·nH2O ]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是__________(填字母)。

a.A点时的溶液为不饱和溶液
b.B点时两种晶体可以共存
c.按上述流程最终得到的晶体是Cu(NO3)2·3H2O
d.若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2·6H2O晶体
(4)某些共价化合物(如H2O、NH3、N2O4等)在液态时有微弱的导电性,主要是因为发生了电离,如:2NH3![]() NH
NH![]() +NH
+NH![]() ,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应。液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是______________________________________;Cu与液态N2O4反应制得无水硝酸铜的化学方程式是______________________________________。
,由此制备无水硝酸铜的方法之一是用Cu与液态N2O4反应。液态N2O4电离得到的两种离子所含电子数相差18,则液态N2O4电离的方程式是______________________________________;Cu与液态N2O4反应制得无水硝酸铜的化学方程式是______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com