
科目: 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如下图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是
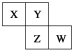
A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性Z比W强
C. Y的气态氢化物的稳定性较Z的弱
D. 四种元素的单质中,Z的熔、沸点最高
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关细胞中元素和化合物的叙述错误的是
A. 休眠的种子比萌发的种子结合水含量高
B. 镁是参与叶绿素合成的微量元素
C. 蛋白质和脂质是所有细胞共有的化合物
D. 磷脂和胆固醇均属于组成动物细胞膜的脂质
查看答案和解析>>
科目: 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl- 六种粒子。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是

A. 该反应的还原剂是Cl-
B. 消耗1 mol还原剂,转移6 mol电子
C. 氧化剂与还原剂的物质的量之比为2:3
D. 反应后溶液的酸性明显增强
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中,正确的是
A. 1s电子云界面图是一个球面,表示在这个球面以内,电子出现的概率为![]()
B. 在能层、能级、以及电子云的伸展方向确定时,电子的运动状态才能确定下来
C. 在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析
D. 原子核外的电子就像行星围绕太阳一样绕着原子核做圆周运动
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A. 过氧化钠与水反应生成0.1mol氧气时,转移的电子数为0.2NA
B. 常温下,56g铁片投入足量浓H2SO4中生成NA个SO2分子
C. 相同质量的铝,分别与足量的盐酸和氢氧化钠溶液反应放出的氢气体积一定不相同
D. 标准状况下,11.2L N2和O2的混合气体中所含的原子数为2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式中正确的是
A. FeBr2溶液中加入等物质的量的Cl2:2Fe2+ + 2Br- + 2Cl2 = 2Fe3++Br2+4Cl-
B. 用氢氟酸在玻璃上“刻字”:SiO2 + 4H+ + 4F- = SiF4↑+ 2H2O
C. 将铜丝投入稀硝酸中:Cu + 4H+ + 2NO3-= Cu2+ + 2NO2↑+ 2H2O
D. NaOH与NH4Cl溶液混合加热:NH4+ + OH- ![]() NH3·H2O
NH3·H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下表部分短周期元素信息,判断以下叙述正确的是( )

A. 氢化物的沸点为H2T<H2R B. 单质与稀盐酸反应的剧烈程度L<Q
C. M与T形成的化合物具有两性 D. L2+与R2﹣的核外电子数相等
查看答案和解析>>
科目: 来源: 题型:
【题目】水是最宝贵的资源之一。下列表述正确的是( )
A.40℃时,纯水的pH=7
B.温度升高,纯水中的c(H+)增大,c(OH-)减小
C.水的电离程度很小,纯水中主要存在形态是水分子
D.向水中加入酸或碱,都可抑制水的电离,使水的离子积减小
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:

c电极的反应方程式为:__________________________。
(2)有机物C4H10与氯气发生取代反应,生成的一氯代物有_______种。
(3) 已知反应H2(g)+Br2(l)2HBr(g)在25 ℃、101 kPa下进行,放出热量为72 kJ,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
H2(g) | Br2(g) | HBr(g) | |
1 mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
则表中a为(_____________)
(4) 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。

一定条件,在水溶液中1 mol Cl-、ClOX-(x=1,2,3,4)的能量(KJ)相对大小如上图所示。
①D是__________(填离子符号)。
②B→A+C反应的离子方程式为__________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com