
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвЛЖЈЬѕМўЯТЃЌФГЗДгІДяЕНЦНКтЃЌЦфЦНКтГЃЪ§ЮЊ K=c(CO2)ЁЄc(NO)/c(NO2)ЁЄc(CO)ЃЌКуШнЪБЩ§ИпЮТЖШЃЌЛьКЯЦјЬхЕФбеЩЋМгЩюЃЌЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ
A. ИУЗДгІЕФьЪБфЮЊИКжЕ
B. ЛЏбЇЗНГЬЪНЮЊ NO2ЃЈgЃЉ+COЃЈgЃЉCO2ЃЈgЃЉ+NOЃЈgЃЉ
C. НЕЮТЃЌе§ЗДгІЫйТЪМѕаЁ
D. КуЮТЪБЃЌдіДѓбЙЧПбеЩЋМгЩюЃЌЦНКтФцЯђвЦЖЏ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЖЬжмЦкдЊЫиWЁЂXЁЂYЁЂZЕФдзгађЪ§вРДЮдіДѓЃЌЦфжаВПЗждЊЫидкжмЦкБэжаЕФЮЛжУШчЭМЫљЪОЁЃвЛИіWX2ЗжзгжаКЌга22ИіЕчзгЃЌYЕФжЪзгЪ§ЪЧXЁЂZЕФКЫЕчКЩЪ§жЎКЭЕФЁЊАыЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
W | X | |
Z |
A. ЗЧН№ЪєадЃКW < Z
B. МђЕЅРызгЕФАыОЖЃКX2- < Y2+
C. ЗаЕуЃКH2X < H2Z
D. WX2ЕФЕчзгЪНЮЊЃК![]()
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
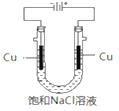
ЁОЬтФПЁПжЊЪЖЕФЪсРэКЭИаЮђЪЧгааЇбЇЯАЕФЗНЗЈжЎвЛЁЃФГбЇЯАаЁзщНЋгаЙиЁАЕчНтБЅКЭЪГбЮЫЎЁБЕФЯрЙиФкШнНјааЪсРэЃЌаЮГЩШчЯТЮЪЬт(ЯдЪОЕФЕчМЋОљЮЊЪЏФЋ)ЁЃ

ЃЈ1ЃЉЭМ1жаЃЌЕчНтвЛЖЮЪБМфКѓЃЌЦјЧђbжаЕФЦјЬхЪЧ__________(ЬюЛЏбЇЪН)ЃЌUаЮЙм________(ЬюЁАзѓЁБЛђЁАгвЁБ)БпЕФШмвКБфКьЁЃ
ЃЈ2ЃЉРћгУЭМ2жЦзївЛжжЛЗБЃаЭЯћЖОвКЗЂЩњЦїЃЌЕчНтПЩжЦБИЁА84ЁБЯћЖОвКЕФгааЇГЩЗжЃЌдђcЮЊЕчдДЕФ________МЋЃЛИУЗЂЩњЦїжаЗДгІЕФзмРызгЗНГЬЪНЮЊ_______________________________ЁЃ
ЃЈ3ЃЉЖўбѕЛЏТШ(ClO2)ЮЊвЛжжЛЦТЬЩЋЦјЬхЃЌЪЧЙњМЪЩЯЙЋШЯЕФИпаЇЁЂЙуЦзЁЂПьЫйЁЂАВШЋЕФЩБОњЯћЖОМСЁЃЯТЭМЪЧФПЧАвбПЊЗЂГігУЕчНтЗЈжЦШЁClO2ЕФаТЙЄвеЁЃ

ЂйбєМЋВњЩњClO2ЕФЕчМЋЗДгІЪНЃК__________________________________________________ЁЃ
ЂкЕБвѕМЋВњЩњБъзМзДПіЯТ112 mLЦјЬхЪБЃЌЭЈЙ§бєРызгНЛЛЛФЄЕФРызгЮяжЪЕФСПЮЊ________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПТШЛЏбЧЭЃЈCuClЃЌАзЩЋЁЂвзБЛбѕЛЏЃЌKsp=1.2ЁС10-6ЃЉЙуЗКгУзїДпЛЏМСЁЂЭбГєМСЁЂЭбЩЋМСЕШЁЃЙЄвЕЩЯгУГѕМЖЭПѓЗлЃЈжївЊКЌCu2SЁЂCuSЁЂFe2O3ЁЂFeOЕШЃЉжЦБИЛюадCuClЕФСїГЬШчЯТЃК

ЃЈ1ЃЉТЫдќЂёЪЧFe(OH)3КЭЕЅжЪСђЕФЛьКЯЮяЃЌЗДгІЂёжаCu2SВЮгыЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃКCu2S+MnO2 + H2SO4ЁњCuSO4 +S+MnSO4 + H2OЃЈЮДХфЦНЃЉЃЛбѕЛЏВњЮяЮЊЃК__________ЁЃ
ЃЈ2ЃЉГ§Mn2+ЪБЕУMnCO3ГСЕэЃЌИУЗДгІЕФРызгЗНГЬЪНЮЊ_________________________ЁЃ
ЃЈ3ЃЉвбжЊЃКCu(OH)2ПЩШмгкАБЫЎаЮГЩЩюРЖЩЋШмвКЁЃCu(OH)2+4NH3![]() [Cu(NH3)4]2++2OHЃЁЃеєАБЬѕМўМАеєАБаЇЙћМћЯТБэЃК
[Cu(NH3)4]2++2OHЃЁЃеєАБЬѕМўМАеєАБаЇЙћМћЯТБэЃК
ађКХ | ЮТЖШ/Ёц | ЪБМф/min | бЙЧП/KPa | ВавКбеЩЋ |
a | 110 | 60 | 101.3 | ЧГРЖЩЋ |
b | 100 | 40 | 74.6 | МИКѕКмЧГ |
c | 90 | 30 | 60.0 | ЮоЩЋЭИУї |
гЩБэжааХЯЂПЩжЊеєАБЕФЬѕМўгІбЁ_______ЃЈЬюађКХЃЉЃЌЧыгУЦНКтвЦЖЏдРэНтЪЭбЁдёИУЬѕМўЕФдвђЪЧ__________________________________________________ЁЃ
ЃЈ4ЃЉЗДгІЂђЕФРызгЗНГЬЪН___________________________ЁЃ
ЃЈ5ЃЉЪЕбщжЄУїЭЈЙ§ШчЭМзАжУвВПЩЛёЕУCuClЃЌЯжЯѓЮЊвѕМЋЃКВњЩњЮоЩЋЦјЬхЃЛбєМЋЃКгаАзЩЋНКзДГСЕэЩњГЩЧвж№НЅдіЖрЃЛUаЮЙмЕзВПЃКППНќвѕМЋЧјАзЩЋНКзДГСЕэж№НЅзЊЛЏЮЊЕЛЦЩЋГСЕэЁЃ
ЂйЩњГЩCuClЕФЕчМЋЗДгІЪНЮЊ________________________________ЁЃ
ЂкгаЭЌбЇЬсГіЃКЕЛЦЩЋГСЕэПЩФмЪЧCuOHЃЌвдЯТЪЧДгзЪСЯжаВщдФЕНCuOHЕФгаЙиаХЯЂЃЌФФаЉПЩвджЇГжИУЭЌбЇЕФЫЕЗЈ________ЁЃЃЈЬюађКХЃЉ
aЃЎШнвзЭбЫЎБфГЩКьЩЋЕФCu2O
bЃЎCuOHЪЧЛЦЩЋЛђЕЛЦЩЋЙЬЬхЃЌВЛШмгкЫЎ
cЃЎCuOHЕФKsp=2ЁС10-15
d
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГЛЏЙЄВЩгУЯЁNaOHШмвКЭбГ§CO2ЃЌШєМюЯДЭбГ§КѓЫљЕУЗЯвКЕФpHдМЮЊ13(вбжЊЃКЯрЭЌЮТЖШЯТБЅКЭNa2CO3ШмвКЕФpHдМЮЊ12)ЃЌдђЯТСаЫЕЗЈе§ШЗЕФЪЧ
A. ИУШмвКжаЃКc(OH)>c(Na+)>c(CO32-)>c(HCO3-)>c(H+)
B. ИУШмвКжаЃКc(Na+)+c(H+)=c(OH)+c(CO32-)+c(HCO3-)
C. МгЫЎЯЁЪЭИУШмвКЃЌЛжИДжСдЮТЖШЃЌpHМѕаЁЃЌKwВЛБф
D. ИУШмвКpHдМЮЊ13ЕФдвђЃКCO32-+H2O===HCO3-+OH
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЮяжЪжаЃЌВЛФмгЩЕЅжЪжБНгЛЏКЯЩњГЩЕФЪЧЃЈ ЃЉ
A. NO2B. Cu2SC. SO2D. FeCl3
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕЩЯгУжиИѕЫсФЦ(Na2Cr2O7)НсОЇКѓЕФФИвК(КЌЩйСПдгжЪFe3+)ЩњВњжиИѕЫсМи (K2Cr2O7)ЃЌЦфЙЄвеСїГЬМАЯрЙиЮяжЪШмНтЖШЧњЯпШчЯТЭМЫљЪОЁЃ
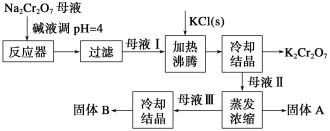

ЃЈ1ЃЉЯђNa2Cr2O7ФИвКжаМгМювКЕїpHЕФФПЕФЪЧ_____________________ЁЃ
ЃЈ2ЃЉЭЈЙ§РфШДНсОЇЮіГіДѓСПK2Cr2O7ЕФдвђЪЧ________________________________ЁЃ
ЃЈ3ЃЉЙЬЬхAЕФжївЊГЩЗжЮЊ__________ЃЈЬюЛЏбЇЪНЃЉЃЌгУШШЫЎЯДЕгЙЬЬхAЃЌЛиЪеЕФЯДЕгвКзЊвЦЕНФИвК___________(ЬюЁАIЁБЁАЂђЁБЛђЁАЂѓЁБ)жаЃЌМШФмЬсИпВњТЪгжПЩЪЙФмКФНЕЕЭЁЃ
ЃЈ4ЃЉВтЖЈВњЦЗжаK2Cr2O7КЌСПЕФЗНЗЈШчЯТЃКГЦШЁВњЦЗЪдбљ2.500 g ХфГЩ250 mLШмвКЃЌгУвЦвКЙмШЁГі25.00 mLгкЕтСПЦПжаЃЌМгШы10 mL 2 molЁЄL-l H2SO4ШмвККЭзуСПKIШмвК(ИѕЕФЛЙдВњЮяЮЊCr3+)ЃЌЗХжУгкАЕДІ5 minЃЌШЛКѓМгШы100 mLеєСѓЫЎЁЂ3 mL ЕэЗлжИЪОМСЃЌгУ0.1200 molЁЄL-l Na2S2O3БъзМШмвКЕЮЖЈ(вбжЊI2+ 2S2O32-=2I-+S4O62-)ЁЃ
ЂйЫсадШмвКжаKI гыK2Cr2O7ЗДгІЕФРызгЗНГЬЪНЮЊ_____________________________ЁЃ
ЂкШєЪЕбщжаЙВгУШЅNa2S2O3БъзМШмвК40.00 mLЃЌдђЫљЕУВњЦЗжажиИѕЫсМиЕФДПЖШЮЊ__________%( БЃСє2 ЮЛаЁЪ§ЃЌЩшећИіЙ§ГЬжаЦфЫћдгжЪВЛВЮгыЗДгІ)ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПРюПЫЧПзмРэдкЁЖ2018ФъЙњЮёдКеўИЎЙЄзїБЈИцЁЗжаЧПЕїЁАНёФъЖўбѕЛЏСђЁЂЕЊбѕЛЏЮяХХЗХСПвЊЯТНЕ3%ЁЃЁБвђДЫЃЌбаОПбЬЦјЕФЭбЯѕ(Г§NOx)ЁЂЭбСђ(Г§SO2)ММЪѕгазХЛ§МЋЕФЛЗБЃвтвхЁЃ
ЃЈ1ЃЉЦћГЕЕФХХЦјЙмЩЯАВзАЁАДпЛЏзЊЛЏЦїЁБЃЌЦфЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊЃК2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ІЄH=-746.50kJЁЄmol-1ЁЃTЁцЪБЃЌНЋЕШЮяжЪЕФСПЕФNOКЭCOГфШыШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌШєЮТЖШКЭЬхЛ§ВЛБфЃЌЗДгІЙ§ГЬжа(0~15min) NOЕФЮяжЪЕФСПЫцЪБМфБфЛЏШчЭМЁЃ
2CO2(g)+N2(g) ІЄH=-746.50kJЁЄmol-1ЁЃTЁцЪБЃЌНЋЕШЮяжЪЕФСПЕФNOКЭCOГфШыШнЛ§ЮЊ2LЕФУмБеШнЦїжаЃЌШєЮТЖШКЭЬхЛ§ВЛБфЃЌЗДгІЙ§ГЬжа(0~15min) NOЕФЮяжЪЕФСПЫцЪБМфБфЛЏШчЭМЁЃ

ЂйЭМжаaЁЂbЗжБ№БэЪОдкЯрЭЌЮТЖШЯТЃЌЪЙгУжЪСПЯрЭЌЕЋБэУцЛ§ВЛЭЌЕФДпЛЏМСЪБЃЌДяЕНЦНКтЙ§ГЬжаn (NO)ЕФБфЛЏЧњЯпЃЌЦфжаБэЪОДпЛЏМСБэУцЛ§НЯДѓЕФЧњЯпЪЧ___________ЁЃЃЈЬюЁАaЁБЛђЁАbЁБЃЉ
ЂкTЁцЪБЃЌИУЗДгІЕФЛЏбЇЦНКтГЃЪ§K=_______________ЃЛЦНКтЪБШєБЃГжЮТЖШВЛБфЃЌдйЯђШнЦїжаГфШыCOЁЂCO2Иї0.2 molЃЌдђЦНКтНЋ_________вЦЖЏЁЃ(ЬюЁАЯђзѓЁБЁЂЁАЯђгвЁБЛђЁАВЛЁБ)
Ђл15minЪБЃЌШєИФБфЭтНчЗДгІЬѕМўЃЌЕМжТn (NO)ЗЂЩњЭМжаЫљЪОБфЛЏЃЌдђИФБфЕФЬѕМўПЩФмЪЧ_______________________________________________ (ШЮД№вЛЬѕМДПЩ)ЁЃ
ЃЈ2ЃЉдкДпЛЏМСзїгУЯТЃЌгУЛЙдМС[ШчыТ(N2H4)]бЁдёадЕигыNOxЗДгІЩњГЩN2КЭH2OЁЃ
вбжЊ200ЁцЪБЃКЂё.3N2H4(g)=N2(g)+4NH3(g) ІЄH1=-32.9 kJЁЄmol-1ЃЛ
II. N2H4(g)+H2(g) =2NH3(g) ІЄH2=-41.8 kJЁЄmol-1ЁЃ
ЂйаДГіыТЕФЕчзгЪНЃК____________________ЁЃ
Ђк200ЁцЪБЃЌыТЗжНтГЩЕЊЦјКЭЧтЦјЕФШШЛЏбЇЗНГЬЪНЮЊЃК_____________________________ЁЃ
ЂлФПЧАЃЌПЦбЇМве§дкбаОПвЛжжвдввЯЉзїЮЊЛЙдМСЕФЭбЯѕдРэЃЌЦфЭбЯѕТЪгыЮТЖШЁЂИКдиТЪ(ЗжзгЩИжаДпЛЏМСЕФжЪСПЗжЪ§)ЕФЙиЯЕШчЯТЭМЫљЪОЁЃ

ЮЊДяЕНзюМбЭбЯѕаЇЙћЃЌгІВЩШЁЕФЬѕМўЪЧ_________________________________________ЁЃ
ЃЈ3ЃЉРћгУЕчНтзАжУвВПЩНјаабЬЦјДІРэЃЌШчЭМПЩНЋЮэіВжаЕФNOЁЂSO2ЗжБ№зЊЛЏЮЊNH4+КЭSO42-ЃЌбєМЋЕФЕчМЋЗДгІЪНЮЊ____________________________ЃЛЮяжЪAЪЧ______________ (ЬюЛЏбЇЪН)ЁЃ

ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЮЊЬНОП![]() ЕФаджЪЃЌФГЭЌбЇАДШчЭМЫљЪОЕФзАжУНјааЪЕбщЁЃ
ЕФаджЪЃЌФГЭЌбЇАДШчЭМЫљЪОЕФзАжУНјааЪЕбщЁЃ

ЭъГЩЯТСаЬюПеЃК
ЃЈ1ЃЉзАжУAжаЪЂЗХХЈМюЫсЕФвЧЦїУћГЦЪЧ________________ЃЌAжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ___________________ЁЃ
ЃЈ2ЃЉзАжУBжаЕФЯжЯѓЪЧ________________________ЃЌЫЕУї![]() Опга________ЃЈЬюДњТыЃЉЃЛзАжУCжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ________________________________ЃЌЫЕУї
Опга________ЃЈЬюДњТыЃЉЃЛзАжУCжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ________________________________ЃЌЫЕУї![]() Опга________ЃЈЬюДњТыЃЉЁЃ
Опга________ЃЈЬюДњТыЃЉЁЃ
aЃЎбѕЛЏад bЃЎЛЙдад cЃЎЦЏАзад dЃЎЫсад
ЃЈ3ЃЉзАжУDЕФФПЕФЪЧЬНОП![]() гыЦЗКьзїгУЕФПЩФцадЃЌаДГіЪЕбщВйзїМАЯжЯѓ________________________ЮВЦјПЩВЩгУ________ШмвКЮќЪеЁЃ
гыЦЗКьзїгУЕФПЩФцадЃЌаДГіЪЕбщВйзїМАЯжЯѓ________________________ЮВЦјПЩВЩгУ________ШмвКЮќЪеЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃК РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЙЄвЕКЯГЩАБдквЛЖЈЬѕМўЯТЗЂЩњШчЯТЗДгІЃК![]() ЃЌЕБНјШыКЯГЩЫўЕФ
ЃЌЕБНјШыКЯГЩЫўЕФ![]() КЭ
КЭ![]() ЕФЬхЛ§БШЮЊ1:3ЪБЃЌОВтЖЈЃЌдквЛЖЈЮТЖШЁЂбЙЧПКЭДпЛЏМСЬѕМўЯТЫљЕУАБЕФЦНКтХЈЖШЃЈЬхЛ§ЗжЪ§ЃЉШчЯТБэЫљЪОЃК
ЕФЬхЛ§БШЮЊ1:3ЪБЃЌОВтЖЈЃЌдквЛЖЈЮТЖШЁЂбЙЧПКЭДпЛЏМСЬѕМўЯТЫљЕУАБЕФЦНКтХЈЖШЃЈЬхЛ§ЗжЪ§ЃЉШчЯТБэЫљЪОЃК
20MPa | 50MPa | |
500Ёц | 19.1 | 42.2 |
ЖјЪЕМЪДгКЯГЩЫўГіРДЕФЛьКЯЦјЬхжаКЌгаАБдМ15%ЁЃ
ЭъГЩЯТСаЬюПеЃК
ЃЈ1ЃЉФПЧАЙЋШЯЕФКЯГЩАБЙЄвЕзюЧЁЕБЕФДпЛЏМСЪЧ________ЁЃ
aЃЎУИ bЃЎЖўбѕЛЏУЬ cЃЎЬњДЅУН dЃЎЮхбѕЛЏЖўЗА
ЃЈ2ЃЉ298KЪБКЯГЩАБЃЌУПЩњГЩ![]() ЃЌЭЌЪБЗХГі46.2kJЕФШШСПЁЃдђИУЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ__________ЃЛИУЮТЖШЯТЃЌШЁ
ЃЌЭЌЪБЗХГі46.2kJЕФШШСПЁЃдђИУЗДгІЕФШШЛЏбЇЗНГЬЪНЮЊ__________ЃЛИУЮТЖШЯТЃЌШЁ![]() КЭ
КЭ![]() ЗХдквЛУмБеШнЦїжаЃЌдкДпЛЏМСЬѕМўЯТЗДгІЃЌВтЕУЗДгІЗХГіЕФШШСПзмаЁгк92.4kJЃЌЦфдвђЪЧ________________________________ЁЃ
ЗХдквЛУмБеШнЦїжаЃЌдкДпЛЏМСЬѕМўЯТЗДгІЃЌВтЕУЗДгІЗХГіЕФШШСПзмаЁгк92.4kJЃЌЦфдвђЪЧ________________________________ЁЃ
ЃЈ3ЃЉКЯГЩАБЕФЮТЖШКЭбЙЧПЭЈГЃПижЦдкдМ500ЁцвдМА20-50MPaЕФдвђЪЧ_________________________________ЁЃ
ЃЈ4ЃЉЪЕМЪЩЯДгКЯГЩЫўГіРДЕФЛьКЯЦјЬхжаАБЕФЬхЛ§ЗжЪ§аЁгкРэТлжЕЕФдвђЪЧ________ЁЃ
aЃЎБэжаЫљВтЪ§ОнгаУїЯдЮѓВю bЃЎЩњГЩЬѕМўПижЦВЛЕБ
cЃЎАБЕФЗжНтЫйТЪДѓгкдЄВтжЕ dЃЎКЯГЩЫўжаЕФЗДгІЮДДяЕНЦНКт
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com