
科目: 来源: 题型:
【题目】按下图所示装置进行实验,并回答下列问题:

(1)装置的名称:A池为_____________,B池为__________(填电解池、原电池)。
(2)石墨棒C1为________极,电极反应式为________________________________。石墨棒C2附近发生的实验现象_________________________________________________________。反应结束后,B池溶液的pH值________。(增大、减小、不变,忽略气体溶于水) 。
(3)当C2极析出2.24L气体(标准状况下),锌的质量________(增加或减少)________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】如表所示的四种短周期元素 W、X、Y、Z,这四种元素的原子最外层电子数之和为 22,下列说法错误的是( )

A. X、Y 和氢三种元素形成的化合物中可能既有离子键、又有共价键
B. 物质 W3X4 中,每个原子最外层均达到 8 电子稳定结构
C. W 元素的单质是良好的半导体材料,它与 Z 元素可形成化合物 WZ4
D. X、Y、Z 三种元素最低价氢化物的沸点 HZ 最高
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠可由亚硫酸钠和硫粉通过化合反应制得:Na2SO3+S=Na2S2O3。常温下溶液中析出晶体为Na2S2O35H2O。Na2S2O35H2O于4045℃熔化,48℃分解:Na2S2O3 易溶于水,不溶于乙醇。在水中有关物质的溶解度曲线 如图所示。

I.现按如下方法制备Na2S2O35H2O:
将硫化钠和碳酸钠按反应要求比例一并放入三颈烧瓶中,注入150mL蒸馏水使其溶解,在分液漏斗中,注入浓盐酸,在装置2中加入亚硫酸钠固体,并按如下图示安装好装置。
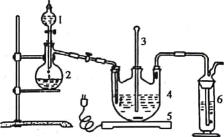
(1)仪器2的名称为__________,装置6中可加入________。
A. BaCl2溶液 B.浓 H2SO4 C.酸性KMnO4溶液 D. NaOH溶液
(2)打开分液漏斗活塞,注入浓盐酸使反应产生的二 氧化硫气体较均匀的通入Na2S和Na2CO3的混合溶液中,并用磁力搅拌器搅动并加热,反应原理为:
①Na2CO3+SO2═Na2SO3+CO2 ②Na2S+SO2+H2O═Na2SO3+H2S
③2H2S+SO2═3S↓+2H2O ④Na2SO3+S![]() Na2S2O3
Na2S2O3
随着SO2气体的通入,看到溶液中有大量浅黄色固体析出,继续通SO2气体,反应约半小时。当溶液中pH接近或不小于7时,即可停止通气和加热。溶液pH要控制不小于7的理由是:______(用文字和相关离子方程式表示)。
Ⅱ.分离Na2S2O35H2O并测定含量:

(3)为减少产品的损失,操作①为_______,操作②是抽滤、洗涤、干燥,其中洗涤操作是用______(填试剂名称)作洗涤剂。
(4)蒸发浓缩滤液,直至溶液呈微黄色浑浊为止。蒸发时要控制温度不宜过高,其原因是_______________。
(5)制得的粗产品中往往含有少量杂质。为了测定粗产品中Na2S2O35H2O的含量,一般采用在酸性条件下用KMnO4标准液滴定的方法(假定杂质与酸性KMnO4溶液不反应)。 称取1.28g粗样品溶于水,用0.40mol/LKMnO4溶液(加入适量硫酸酸化)滴定,当溶液 中S2O32-全部被氧化时,消耗KMnO4溶液20.00mL。(5S2O32-+ 8MnO4-+14H+=8Mn2++l0SO42-+7H2O)
试回答:
①滴定终点时的颜色变化_______________。
②产品中Na2S2O35H2O的质量分数为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室中需要配制2 mol·L-1的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
A.950 mL,111.2 gB.500 mL,117 g
C.1 000 mL,117 gD.任意规格,111.2 g
查看答案和解析>>
科目: 来源: 题型:
【题目】从海水中提取部分物质的过程如下图所示

下列有关说法错误的是
A. 过程①需要加入化学试剂、沉淀、过滤等操作
B. 由“母液→无水MgCl2”一系列变化中未涉及氧化还原反应
C. 工业上一般用金属钠与无水MgCl2反应制取Mg单质
D. 反应③和⑤均可由下列反应实现:2Br-+Cl2=Br2+2Cl-,该反应属于置换反应
查看答案和解析>>
科目: 来源: 题型:
【题目】我国古代的物质文明华夏民族在认识、改造和应用物质方面有着辉煌的历史。
①东晋《抱扑子》中记载:“以曾青涂铁,铁赤色如铜”(“曾青”即硫酸铜溶液)。
②战国《周礼》中记载;“煤饼烧砺房成灰”(“砺房”即牡砺壳,主要成分是碳酸钙)。将“灰”溶于水可制得沤浸树皮脱胶的碱液。
③元代《庚道集》中记载:“点铜戍银”(即单质铜与砷融合形成银白色的物质)
请运用你学过的化学知识回答下列问题;
(1)在①~③中,发生了化学变化的是___(填编号)其中发生分解反应的化学方程式为___。
(2)①中发生变化的化学方程式为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中不正确的是( )
A.  能使溴水、酸性高锰酸钾溶液褪色
能使溴水、酸性高锰酸钾溶液褪色
B. 用燃烧法鉴别乙醇、苯和四氯化碳
C. 油脂的种类很多,但它们水解后都一定有一产物相同
D. 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水浴加热,来检验蔗糖水解产物具有还原性
查看答案和解析>>
科目: 来源: 题型:
【题目】铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法中,不正确的是

A. 正极电极反应式为:2H++2e—→H2↑
B. 此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
C. 此过程中铜并不被腐蚀
D. 此过程中电子从Fe移向Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】25 ℃时,在2 L的恒容密闭容器中,气态A、B、C的物质的量n(mol)随时间t的变化如图所示。

(1)该反应的化学方程式____________________________________________________。
(2)在________________min时反应刚好达到平衡。
(3)在0~3minA物质的平均速率为_____________________,此时A物质的转化率为______,3min末时A物质的浓度为_____________。
(4)5~7 min内B的平均速率___________1~3min内B的平均速率(填大于、小于、等于)。
(5)下列措施可加快该反应速率的是__________。
A.扩大容器体积 B.使用恰当的催化剂 C.提高反应的温度 D.液化并转移出C物质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com