
科目: 来源: 题型:
【题目】某溶液可能含有Al3+、NH4+、Fe2+、Na+、CO32-、SO42-、Cl-、NO3-中的若干种,若在该溶液中逐滴加入稀盐酸至过量,无明显现象,并得到X溶液,对X溶液进行如下实验,下列结论正确的是(忽略水的电离,且原溶液中各离子浓度均为0.5mol L-1)

A. 原溶液中一定存在NH4+、Fe2+、SO42-、Cl-
B. 原溶液中可能含有NO3-和Al3+
C. 白色沉淀C可能是Al(OH)3
D. 沉淀B可能是Fe(OH)2和Fe(OH)3的混合物
查看答案和解析>>
科目: 来源: 题型:
【题目】镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O![]() Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是
A.充电时阳极反应:Ni(OH)2 -e— + OH- = NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室需要480 mL 0.200 mol·L-1的Na2CO3溶液,现用Na2CO3固体配制,可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤漏斗 ⑥天平 ⑦药匙 ⑧500 mL容量瓶 ⑨250 mL容量瓶。
请回答下列问题:
(1)上述仪器中,在配制Na2CO3溶液时必须使用的仪器除①③⑥⑦外,还有_____(填数字序号)。
(2)经计算,需Na2CO3固体的质量为________。
(3)在容量瓶中确定溶液体积的过程中,最后加入少量水的做法_________。
(4)将所配制的Na2CO3溶液进行测定,发现浓度小于0.200 mol·L-1。请你分析配制过程中可能引起该误差的原因是(填字母代号)________。
A.定容时俯视液面
B.转移时没有洗涤烧杯和玻璃棒
C.配制时容量瓶不干燥
D.称Na2CO3固体的质量时物码倒置
(5)将配好的溶液盛装于下列(填字母代号)_______仪器中,贴好标签备用。
A.带玻璃塞的广口瓶 B.带玻璃塞的细口瓶
C.带胶塞的广口瓶 D.带胶塞的细口瓶
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)基态溴原子的价层电子轨道排布式为________。第四周期中,与溴原子未成对电子数相同的金属元素有_______种。
(2)铍与铝的元素性质相似。下列有关铍和铝的叙述正确的有___________(填标号)。
A.都属于p区主族元素B.电负性都比镁大
C.第一电离能都比镁大D.氯化物的水溶液pH均小于7
(3)Al元素可形成[AlF6]3-、[AlCl4]-配离子,而B元素只能形成[BF4]-配离子,由此可知决定配合物中配位数多少的因素是________________;[AlCl4]-的立体构型名称为______。
(4)P元素有白磷、红磷、黑磷三种常见的单质。
①白磷(P4)易溶于CS2,难溶于水,原因是________________
②黑磷是一种黑色有金属光泽的晶体,是一种比石墨烯更优秀的新型材料。白磷、红磷都是分子晶体,黑磷晶体与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是_________。

A.黑磷晶体中磷原子杂化方式为sp2杂化
B.黑磷晶体中层与层之间的作用力是分子间作用力
C.黑磷晶体的每一层中磷原子都在同一平面上
D.P元素三种常见的单质中,黑磷的熔沸点最高
(5)F2中F-F键的键能(157kJ/mol)小于Cl2中Cl-Cl键的键能(242.7kJ/mol),原因是_________。
(6)金属钾的晶胞结构如图。若该晶胞的密度为a g/cm3,阿伏加得罗常数为NA,则表示K原子半径的计算式为______。

查看答案和解析>>
科目: 来源: 题型:
【题目】硝酸工业中产生的NO是一种大气污染物,可以通过如下反应处理:2NO(g)+2CO(g) ![]() N2 (g)+ 2CO2(g); △H1。
N2 (g)+ 2CO2(g); △H1。
(1)已知:2CO(g)+O2(g)=2CO2(g);△H2=-566 kJ·mol-l,N2(g)+O2(g) ![]() 2NO(g); △H3=+181 kJ ·mol-l,则△H1=___________
2NO(g); △H3=+181 kJ ·mol-l,则△H1=___________
(2)在一定温度下,向体积为2L的密闭容器中充入4 moI NO、2 mol CO。
①若为恒容密闭容器,在10min时达到平衡状态,压强为原来的14/15,这段时间内,NO的平均反应速率为___________,平衡常数为___________L· mol-1,此时NO的转化率a%;平衡后,向恒容密闭容器中再充入2 mol NO、1 mol CO,重新达到平衡时,NO的转化率将___________(填“增大”、“不变”或“减小”);
②若为恒压密闭容器,平衡后NO的转化率为b%,则a%________b%(填“<”、“=”或>”)
(3)工业上,NO与CO混合气体以一定流速和一定的比例,通过填充有A、B催化剂的反应器,在A、B两种催化剂作用下,CO转化率与温度的关系如下图所示。

①工业上选择催化剂___________(填“A”或“B),理由是___________。
②在催化剂B作用下,高于550K时,CO转化率下降的理由可能是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜.下列有关说法正确的是( )
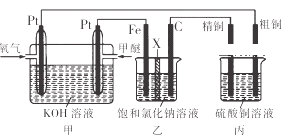
A. 反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B. 乙装置中铁电极为阴极,电极反应式为Fe﹣2e ﹣=Fe2+
C. 通入氧气的一极为正极,发生的电极反应为O2﹣4e ﹣+2H2O═4OH﹣
D. 反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
查看答案和解析>>
科目: 来源: 题型:
【题目】氢氧化钡是分析化学中的重要试剂。工业上以重晶石矿(主要成分BaSO4,含杂质Fe2O3、SiO2)为原料,生产Ba(OH)2·8H2O的流程示意如下:

已知:高温焙烧,炭还原重晶石的反应方程式为:BaSO4+4C![]() CO↑+BaS
CO↑+BaS
(1)氢氧化钡的电子式为___________。
(2)水浸并过滤后的滤渣中含三种单质,分别为C、______和____ (填化学式),滤液1显______(填“酸性”或“碱性”)。向滤液1中加入CuO后,会生成黑色沉淀,该反应的化学方程式为___________。
(3)还可采用如下流程对滤液1进行处理:

若D物质为AB型,其组成与MnO2相同,滤液1中加入MnO2的化学方程式为_______。该方法的优点是_____。
(4)由滤液2得到产品需采用的操作是___________、___________、过滤。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为______。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为________。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为________。
(4)相同条件下,体积比为a∶b和质量比为a∶b的H2和O2的混合气体,其平均摩尔质量分别是________和________。
(5)在标准状况下,CO和CO2的混合气体共39.2 L,质量为61 g,则两种气体的物质的量之和为________mol,CO占总体积的________%。
(6)在某温度时,一定量的元素A的氢化物AH3,在恒温恒压的密闭容器中完全分解为两种气态单质,此时容器的体积变为原来的7/4,则A单质的分子式为_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在t℃时,Ag2CrO4(橘红色)在水溶液中的沉淀溶解平衡曲线如图所示.又知AgCl的Ksp=1.8×10-10。下列说法不正确的是( )

A. t℃时,Y点和Z点时Ag2CrO4的Ksp相等
B. 饱和Ag2CrO4溶液中加入K2CrO4不能使溶液由Y点变为X点
C. t℃时,Ag2CrO4的Ksp为1×10-8
D. t℃时,将0.01mol·L-1 AgNO3溶液滴入20mL0.01mol·L-1 KCl和0.01mol·L-1 K2CrO4的混合溶液中,Cl-先沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】25℃条件下,向10 mL 0.1 mol·Lˉ1的HR溶液中逐滴滴入0.1 mol·Lˉ1的NH3·H2O溶液,所得溶液pH及导电性变化如图。下列分析不正确的是( )
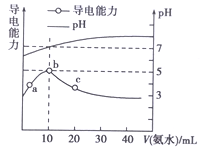
A. a~b点导电能力增强,说明HR为弱酸
B. b点溶液pH=7说明NH4R没有发生水解
C. c点溶液存在c(NH4+)>c(Rˉ)、c(OHˉ)>c(H+)
D. b~c任意点溶液均有c(H+)·c(OHˉ)=KW=1.0×10ˉ14
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com