
科目: 来源: 题型:
【题目】轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列对该化合物的说法中,正确的是( )

A. 名称是乙醚
B. 只含有一种官能团
C. 链状同分异构体中,属于羧酸的有3种
D. 既能发生加聚反应,又能发生缩聚反应
查看答案和解析>>
科目: 来源: 题型:
【题目】下列氧化还原反应中,水作为氧化剂的是( )
A. CO+H2O![]() CO2+H2B. CuO+H2
CO2+H2B. CuO+H2![]() Cu+H2O
Cu+H2O
C. 2F2+2H2O═4HF+O2D. 3NO2+H2O═2HNO3+NO
查看答案和解析>>
科目: 来源: 题型:
【题目】某学习小组以废催化剂(主要成分SiO2、ZnO、ZnS和CuS)为原料,制备锌和铜的硫酸盐晶体。设计的实验方案如下:

下列说法不正确的是( )
A. 步骤①中能溶于稀硫酸的是ZnO、ZnS
B. 步骤①、③中发生的反应均为氧化还原反应
C. 步骤③涉及的离子反应可能为CuS+H2O2+2H+![]() Cu2++S+2H2O
Cu2++S+2H2O
D. 步骤②和④,采用蒸发浓缩、冷却结晶,过滤后均可获取粗晶体
查看答案和解析>>
科目: 来源: 题型:
【题目】科学家将水置于足够强的电场中,在20℃时水分子瞬间凝固可形成“暖冰”。某兴趣小组做如图所示实验,发现烧杯中酸性KMnO4溶液褪色,且有气泡产生。将酸性KMnO4溶液换成FeCl3溶液,烧杯中溶液颜色无变化,但有气泡产生。则下列说法中正确的是( )

A. 20℃时,水凝固形成的“暖冰”所发生的变化是化学变化
B. “暖冰”是水置于足够强的电场中形成的混合物
C. 烧杯中液体为FeCl3溶液时,产生的气体为Cl2
D. 该条件下H2燃烧的产物中可能含有一定量的H2O2
查看答案和解析>>
科目: 来源: 题型:
【题目】氮化钙(Ca3N2)是一种重要的化工试剂,遇水剧烈水解。实验室可由氮气和钙加热制得氮化钙,实验装置如下图(省略部分固定装置)。
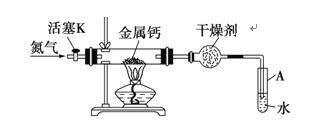
(1)氮化钙中所含的化学键有(填“共价键”或“离子键”)_________。
(2)球形干燥管中的干燥剂可选用(至少写一种)_________,结合化学方程式解释其作用_________。
(3)制备过程中末端导管必须始终插入试管A的水中,目的是①便于观察N2的流速;②_________。
(4)制备氮化钙的操作步骤:①按图示连接好实验装置;②_________;③打开活塞K并通入N2;④点燃酒精灯,进行反应;⑤反应结束后,熄灭酒精灯,继续通N2,使装置冷却至室温;⑥拆除装置,取出产物。
(5)上述步骤中③和④_________(填“能”或“不能”)交换,理由是_________。
(6)氮气不足会影响实验制得Ca3N2的纯度。为测定氮化钙的纯度,实验结束后取一定量的固体混合物于足量水中,微热使气体完全逸出,收集到气体共6.72 L(已折算到标准状况),将该气体通入装有足量灼热CuO的硬质玻璃管中充分反应,测得硬质玻璃管中固体质量减轻6.4 g。则Ca3N2的纯度为_________(用百分数表示,保留一位小数)(注:氨气能被灼热氧化铜氧化,生成一种对环境无污染气体)。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲烷、乙烯是重要的化工原料。下列叙述正确的是
A. 甲烷、乙烯是同分异构体
B. 可用酸性高锰酸钾溶液来区别甲烷和乙烯
C. 甲烷与氯气在光照条件下发生置换反应
D. 乙烯与水在一定条件下发生取代反应生成乙醇
查看答案和解析>>
科目: 来源: 题型:
【题目】现有如下各种说法:
①金属和非金属化合时一定形成离子键;
②离子键是阳离子、阴离子的相互吸引力;
③根据电离方程式HCl![]() H++Cl-,判断氯化氢分子里存在离子键;
H++Cl-,判断氯化氢分子里存在离子键;
④氢气和氯气的反应过程:H2、Cl2分子里共价键发生断裂生成H原子、Cl原子,而后H原子、Cl原子形成离子键的过程
上述各种说法正确的是
A. ①② B. 都不正确 C. ①②④ D. ①
查看答案和解析>>
科目: 来源: 题型:
【题目】氮及其化合物的转化过程如下图所示。

下列分析合理的是( )
A. N2与H2反应生成NH3的原子利用率为100%
B. 催化剂a、b能提高反应的平衡转化率
C. 催化剂a表面发生了极性共价键的断裂和形成
D. 在催化剂b表面形成氮氧键时,不涉及电子转移
查看答案和解析>>
科目: 来源: 题型:
【题目】由碳的氧化物直接合成乙醇燃料已进入大规模生产。下图是由二氧化碳合成乙醇的技术流程:

吸收池中盛有饱和碳酸钾溶液,把含有二氧化碳的空气吹入吸收池中,吸收池中反应液进入分解池后,向分解池中通入高温水蒸汽,把二氧化碳从溶液中提取出来,在合成塔中和氢气经化学反应使之变成可再生燃料乙醇。回答下列问题:
(1)写出吸收池中反应的离子方程式_______________________________________。
(2)除水之外,从分解池中循环使用的物质是_________________________________________。
(3)工业上还采用以CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g)写出该反应的化学平衡常数表达式 K=___________________。
CH3CH2OH(g)+H2O(g)写出该反应的化学平衡常数表达式 K=___________________。
(4)在相同条件下,由CO制取CH3CH2OH的平衡常数远远大于由CO2制取CH3CH2OH的平衡常数。则由CO制取CH3CH2OH的优点是原料有较大的转化率,由CO2制取CH3CH2OH的优点是_______________________________________________________。
(5)在一定压强下,测得由CO2制取CH3CH2OH的实验数据如下表:

根据表中数据分析:
①温度升高,该反应的平衡常数K值___________________(选填“增大”、“减小”或“不变”)
②提高氢碳n(H2)/n(CO2)比,对生成乙醇___________(选填“不利”、“有利”或“无影响”)
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A. 92 g甘油中含有羟基数为NA
B. 常温常压下,16 g O2和O3的混合气体中含有8NA个电子
C. 标准状况下,22.4 L苯中含有的碳碳双键数为3NA
D. 1 L 1 molL﹣1的NaClO溶液中含有ClO﹣的数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com