
科目: 来源: 题型:
【题目】下列属于水解反应且正确的是
A. H2O+H2O![]() H3O++OH﹣ B. Br﹣+H2O
H3O++OH﹣ B. Br﹣+H2O![]() HBr+OH﹣
HBr+OH﹣
C. HCO3-+H2O![]() CO32-+H3O+ D. CO32﹣+H2O
CO32-+H3O+ D. CO32﹣+H2O![]() HCO3﹣+OH﹣
HCO3﹣+OH﹣
查看答案和解析>>
科目: 来源: 题型:
【题目】用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶液于一洁净的锥形瓶中,然后用0.20mol·L -1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
NaOH起始读数 | NaOH终点读数 | |
第一次 | 0.10mL | 18.60mL |
第二次 | 0.30mL | 18.00mL |
(1)准确配制0.20mol·L-1的氢氧化钠溶液250mL,需要的主要仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有____________________
(2)根据以上数据可以计算出盐酸的物质的量浓度为_____________mol·L-1.
(3)用0.20mol·L-1标准氢氧化钠溶液滴定待测盐酸溶液,滴定时左手控制碱式滴定管的玻璃球,右手不停摇动锥形瓶,眼睛注视 _______________,直到滴定终点。
(4)达到滴定终点的标志是_______________________________________________________
(5)以下操作造成测定结果偏高的原因可能是__________________。
A. 未用标准液润洗碱式滴定管
B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K =__________________。
(2)该反应为__________反应(“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是_______________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c.υ正(H2)=υ逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________℃。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)常温时Cu(NO3)2的水溶液的pH _____7(填“>”、“=”、“<”),原因是(用离子方程式表示):________________________;
(2)氯化铝水溶液呈____性 ,原因是(用离子方程式表示):_________________。把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是________ 。
(3)在配制氯化铁溶液时,为了防止发生水解,可以加入少量的_______________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】在0.5mol·L-1的NaHCO3溶液中滴入酚酞,溶液变红。试回答有关问题:
(1)该溶液中HCO3-的电离程度__________(填“大于”、“小于”或“等于”)HCO3-的水解程度。溶液中Na+、HCO3-、CO32-、H+、OH-离子的浓度由大到小的顺序为______________。
(2)某温度下纯水中的c(H+)= 2×10-7mol/L,则此时溶液中的c(OH-)=_________;若温度不变,滴入稀盐酸,使c(H+)= 5×10-4mol/L,则溶液中c(OH-)=____________,此时溶液中由水电离产生的c(H+)= _________ 。
(3)物质的量浓度均为0.1 mol/L的下列溶液:①KNO3、②Na2CO3、③NaHCO3、④HCl 、⑤CH3COOH、⑥NaOH 、⑦Ba(OH)2、⑧NH4Cl, pH 由大到小的顺序为________________
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇: CO(g)+2H2(g) ![]() CH3OH(g),现在实验室模拟该反应并进行分析。
CH3OH(g),现在实验室模拟该反应并进行分析。
(1)下图是该反应在不同温度下CO的转化率随时间变化的曲线。

①该反应的焓变ΔH__________0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1_______K2 (填 “>”、“<”或“=”)。
③若容器容积不变,下列措施可增加甲醇产率的是______________。
A.升高温度 B.将CH3OH(g)从体系中分离
C.使用合适的催化剂 D.充入He,使体系总压强增大
(2)在容积为2 L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考察温度对反应的影响,如图所示
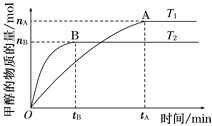
下列说法正确的是________(填序号);
①温度为T1时,从反应开始到平衡,生成甲醇的平均速率为v(CH3OH)=nA/tAmol·L-1·min-1
②该反应在T1时的平衡常数比T2时的小
③该反应为放热反应
④处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(3)在T1温度时,将1 mol CO2和3 mol H2充入一密闭恒容容器中,充分反应达到平衡后,若CO2的转化率为α,则容器内的压强与起始压强之比为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】草酸(H2C2O4)是一种二元弱酸。常温下,向H2C2O4溶液中逐滴加入NaOH溶液,混合溶液中lgX[X为c(HC2O4-)/c(H2C2O4)或c(C2O42-)/c(HC2O4-)]与pH的变化关系如图所示。下列说法一定正确的是( )

A. Ⅰ表示lgc(HC2O4-)/c(H2C2O4)与pH的变化关系
B. pH=1.22的溶液中:2c(C2O42﹣)+c(HC2O4﹣)>c(Na+)
C. 1.22<pH<4.19的溶液中:c(HC2O4﹣)>c(C2O42﹣)>c(H2C2O4)
D. pH=4.19的溶液中:c(Na+)=3c(HC2O4﹣)
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室可用浓盐酸与二氧化锰固体制备氯气。取0.2mol二氧化锰固体加入200g36%的浓盐酸(过量)中,完全反应。
(1)浓盐酸中溶质的物质的量为多少?_______________
(2)产生的氯气在标准状况下的体积为多少?(不考虑氯气溶于水)____________
(3)在反应后溶液中加入足量的AgNO3溶液,生成的AgCl沉淀的质量是多少克?_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下向10mL 0.1mol·L-1 NaOH溶液中加入0.1mol·L-1的一元酸HA溶液,pH变化曲线如图所示。下列说法正确的是

A. a点所示溶液中c(Na+)>c(A-)>c(H+)>c(HA)
B. a、b两点所示溶液中水的电离程度相同
C. b点所示溶液中c(A-)>c(HA)
D. pH=7时,c(Na+)=c(A-)+c(HA)
查看答案和解析>>
科目: 来源: 题型:
【题目】在一固定容积的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s) + 2NO(g) ![]() CO2(g) + N2(g),平衡时c (NO)与温度T的关系如下图所示,则下列说法正确的是
CO2(g) + N2(g),平衡时c (NO)与温度T的关系如下图所示,则下列说法正确的是

A. 该反应的△H>0
B. 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2
C. 若状态B、C、D的压强分别为PB、PC 、PD ,则PC=PD>PB
D. 在T2时,若反应体系处于状态D ,则此时v正>v逆
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com