
科目: 来源: 题型:
【题目】下列方程式书写正确的是
A. H2S在CuSO4溶液中反应的离子方程式:Cu2++S2- = CuS↓
B. H2SO3的电离方程式:H2SO3![]() 2H++SO32-
2H++SO32-
C. HCO3-的水解方程式:HCO3-+H2O![]() H2CO3+OH-
H2CO3+OH-
D. CaCO3的电离方程式:CaCO3 ![]() Ca2++CO32-
Ca2++CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】奈必洛尔是一种用于血管扩张的降血压药物,一种合成奈必洛尔中间体G的部分流程如下:

已知:乙酸酐的结构简式为![]() 。
。
请回答下列问题:
(1)A的名称是______;B中所含官能团的名称是______。
(2)反应⑤的化学方程式为______,该反应的反应类型是______。
(3)G的分子式为______。
(4)写出满足下列条件的E的同分异构体的结构简式:______、______。
Ⅰ.苯环上只有三个取代基
Ⅱ核磁共振氢谱图中只有4组吸收峰
Ⅲ.1mol该物质与足量NaHCO3溶液反应生成2molCO2
(5)根据已有知识并结合相关信息,写出以![]() 为原料制备
为原料制备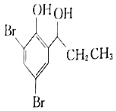 的合成路线流程图(无机试剂任选)______,合成路线流程图示例如下:CH3CH2Br
的合成路线流程图(无机试剂任选)______,合成路线流程图示例如下:CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目: 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g) + I2(g)![]() 2HI(g) ΔH=-a kJ·mol-1
2HI(g) ΔH=-a kJ·mol-1
已知: (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是( )
A. 反应物的总能量高于生成物的总能量
B. 断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量
C. 断开2 mol H-I键所需能量约为(c+b+a) kJ
D. 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】(以下各空用适当的化学用语或关系式填写)密闭容器中mA(g)+nB(g)pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如图所示.则:

(1)增大压强:A的转化率______,平衡向______ 移动,达到平衡后,混合物中C的质量分数______.
(2)上述化学方程式中的系数m、n、p的正确关系是______.
(3)当降低温度时,C的质量分数增大,则:平衡向______移动,A的转化率______,正反应是______ 热反应.
查看答案和解析>>
科目: 来源: 题型:
【题目】对于弱酸,在一定温度下达到电离平衡时,各粒子的浓度存在一种定量的关系.若25℃时有HA H++A-,则K=![]() 式中:K为电离平衡常数,只与温度有关,c为各粒子的平衡浓度.下表是几种常见弱酸的电离平衡常数(25℃).
式中:K为电离平衡常数,只与温度有关,c为各粒子的平衡浓度.下表是几种常见弱酸的电离平衡常数(25℃).

回答下列各题:
(1)K只与温度有关,当温度升高时,K值________(填“增大”、“减小”或“不变”).
(2)在温度相同时,各弱酸的K值不同,且K值越大酸性越________,某个酸的 K=6.4![]() 10-6,则0.1mol/L的上述各酸的H+离子浓度比该酸大的有________ 和 ________。
10-6,则0.1mol/L的上述各酸的H+离子浓度比该酸大的有________ 和 ________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、H2PO4-、HPO42-都看作是酸,其中酸性最强的是________,最弱的是________.
(4)多元弱酸是分步电离的,每一步都有相应的电离平衡常数,对于同一种多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是________,产生此规律的原因是__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】MoS2(辉钼矿的主要成分)可用于制取钼的化合物润滑添加剂氢化反应和异构化反应的催化剂等。回答下列问题:
(1)反应3MoS2+18HNO3+12HCl=3H2[MoO2Cl4]+18NO↑+6H2SO4+6H2O中,每溶解1mol MoS2,转移电子的物质的量为___________。
(2)已知:MoS2(s)= Mo(s)+S2(g) △H1
S2(g)+2O2(g)=2SO2(g) △H2
2MoS(s)+7O2(g)=2MoO3 (s)+4SO2(g) △H3
反应2Mo(s)+3O2(g)=2MoO3(s)的△H=___________(用含△H1、△H2、△H3的代数式表示)。
(3)利用电解法可浸取辉钼矿得到Na2MoO4和Na2SO4溶液(装置如图所示)。

①阴极的电极反应式为______________________。
②一段时间后,电解液的pH___________ (填“增大”“减小”或“不变”),MoO42-在电极___________(填“A”或“B”)附近生成。
③实际生产中,惰性电极A一般不选用石墨,而采用DSA惰性阳极(基层为TiO2,涂层为RuO2+IrO2),理由是_______________________。
(4)用辉钼矿冶炼Mo的反应为
MoS2(s)+4H2(g)+2Na2CO3(s)![]() Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) △H。
①该反应的△H___________(填“>”或“<”)0;p1、p2、p3按从小到大的顺序为___________。
②在某恒容密闭容器中加入0.1 mol MoS2、0.2mol Na2CO3、0.4mol H2,一定温度下发生上述反应,下列叙述说明反应已达到平衡状态的是____________ (填标号)。
a.v正(H2)=v逆(CO)
b.气体的密度不再随时间变化
c.气体的压强不再随时间变化
d单位时间内断裂H一H键与断裂H—O键的数目相等
③在2L的恒温恒容密闭容器中加入0.1 mol MoS2、0.2 mol Na2CO3、0.4molH2,在1100K时发生反应,达到平衡时恰好处于图中A点,则此温度下该反应的平衡常数为___________。

查看答案和解析>>
科目: 来源: 题型:
【题目】用化学原理和相应的方程式解释生活中的现象。
(1) 碳酸钙高温分解生成氧化钙和二氧化碳的化学反应中,![]() S______0;
S______0;
(2)明矾水溶液的pH_______7, 请用离子方程式说明原因______;
(3)盐碱地(含有氯化钠,碳酸钠)不利于作物生长。通过施加适量石膏可以降低土壤碱性。试用水解方程式分别表示盐碱地产生碱性的原因______________;以及用石膏降低其碱性的反应原理______________;
(4)请写出硫酸钡的溶解平衡方程式______________;并说明为什么在洗涤硫酸钡沉淀时,采用0.010mol/L的硫酸进行洗涤______________
查看答案和解析>>
科目: 来源: 题型:
【题目】TMB由碳氢氮三种元素组成,其相对分子质量为240,是一种新型指纹检测的色原试剂,已在逐步取代强致癌物联苯胺和其他致癌性的联苯胺衍生物应用于临床化验法医检验刑事侦破及环境监测等领域。某研究小组欲利用燃烧法测定TMB的分子式(氮元素转化为N2)实验装置如图所示。回答下列问题:
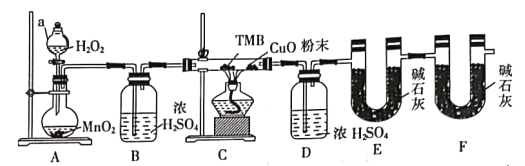
(1)实验装置两处用到装有碱石灰的干燥管,其中F处的目的是______________________。仪器a的名称是___________。
(2)将足量双氧水置于a中,圆底烧瓶中装入MnO2固体,按图连接好装置。
①A中发生反应的化学方程式为______________________。
②待B、D处导管口有均匀气泡时,再点燃C处酒精灯,原因是______________________。
(3)装置C中CuO粉末的作用为_________________________________。
(4)该实验___________(填“需要”或“不需要”)尾气处理,其原因是____________________。
(5)理想状态下,将4.80gTMB样品完全氧化,点燃C处酒精灯,实验结束时测得D增加3.60g,E增加14.08g,则TMB的分子式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中正确的是( )
A. 摩尔是国际单位制中七个基本物理量之一
B. 铁的摩尔质量就是铁原子的相对原子质量
C. 含有NA个氧原子的硫酸的物质的量是0.25mol
D. 40gNaOH溶于1L水,溶质的物质的量浓度为1mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值。下列说法正确的是
A. 1. 0mol·L-1 AlCl3的溶液中含Al3+的数目小于0. 1NA
B. 0. 5mol环己烷中含非极性键的数目为2. 5NA
C. 30g由葡萄糖和乳酸(C3H6O3)组成的混合物中含氢原子数目为2NA
D. 7. 1g Cl2完全反应转移的电子数一定为0. 2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com