
科目: 来源: 题型:
【题目】为了将混有Na2SO4、NaHCO3的NaCl固体提纯,制得纯净的氯化钠溶液,某学生设计了如下图所示的实验方案:

已知碳酸氢钠在加热条件下能分解成碳酸钠、二氧化碳和水,而NaCl和Na2SO4固体加热时不发生化学变化。请回答下列问题:
(1)操作①盛放药品可选用___________(填仪器名称)。
(2)操作②为什么不用Ba(NO3)2溶液,其理由是:___________________________。
(3)进行操作②后,判断SO42-已除尽的方法是:______________________________。
(4)操作③的目的是:____________________________________________________。
(5)此设计方案是否严密___________(填“是”或“否”)理由_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠晶体(![]() ,
,![]() )可用作还原剂。回答下列问题:
)可用作还原剂。回答下列问题:
(1)已知:![]() ,
,![]() 都是难溶于水的固体。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
都是难溶于水的固体。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
试剂:稀盐酸、稀![]() 、
、![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液
溶液
实验步骤 | 现象 |
①取少量样品,加入除氧蒸馏水 | ②固体完全溶解得无色澄清溶液 |
③取少量溶液溶于盐酸 | ④出现乳黄色浑浊,_____ |
⑤静置,________ | ⑥_______ |
(2)利用![]() 作为标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
作为标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制;称取1.270g纯净的![]() ,在盛有KI溶液的____(填仪器名称,下同)中溶解(反应为
,在盛有KI溶液的____(填仪器名称,下同)中溶解(反应为![]() ,
,![]() 能够充分反应),完全溶解后,全部转移至100 mL的____中,加蒸馏水至刻度线,此时
能够充分反应),完全溶解后,全部转移至100 mL的____中,加蒸馏水至刻度线,此时![]() 溶液的物质的量浓度为____
溶液的物质的量浓度为____![]() ;再取
;再取![]() 样品配制成溶液,备用。
样品配制成溶液,备用。
②滴定:利用发生反应:![]() ,对上述配制的
,对上述配制的![]() 溶液进行滴定,终点时消耗标准溶液20.00 mL,则样品纯度为___%(保留1位小数。
溶液进行滴定,终点时消耗标准溶液20.00 mL,则样品纯度为___%(保留1位小数。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学在能源开发与利用中起着十分关键的作用。能源分为一级能源和二级能源,将自然界中存在的能源称为一级能源,通过其它方式获得的能源称为二级能源。甲烷、氢气是重要的能源。回答下列问题:
(1)关于甲烷、氢气的说法正确的是___
A.甲烷和氢气都是一级能源 B.甲烷是一级能源,氢气是二级能源
C.甲烷和氢气都是二级能源 D.甲烷是二级能源,氢气是一级能源
(2)![]() 经催化重整可以获得合成气:
经催化重整可以获得合成气:![]()
①已知上述反应中相关的化学键键能数据如下:
化学键 | C—H |
| H—H |
|
键能/ | 413 | 745 | 436 | 1075 |
则该反应的![]() _____
_____![]() 。
。
②已知:![]()
![]()
![]()
![]()
而C(s)的燃烧热![]()
该催化重整反应的![]() ___
___![]() (用含a、b、c的式子表示)。
(用含a、b、c的式子表示)。
(3)氢气是氯碱工业的副产品,产生氢气的电极反应式为___。
(4)利用氢气可以合成氨,将![]() 通入NaClO的溶液中可以获得
通入NaClO的溶液中可以获得![]() 写出
写出![]() 的电子式__。该反应的化学方程式为____。
的电子式__。该反应的化学方程式为____。
(5)CO也是一种重要燃料,利用其燃烧可以设计成新型燃料电池,该电池利用熔融的碳酸盐为电解质,该燃料电池负极的电极反应式为____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示,相同温度下,在容器Ⅰ和Ⅱ中分别充入等物质的量的HI,发生反应2HI(g) ![]() H2(g)+I2(g)。下列关于反应起始时容器Ⅰ和Ⅱ中活化分子的说法不正确的是( )
H2(g)+I2(g)。下列关于反应起始时容器Ⅰ和Ⅱ中活化分子的说法不正确的是( )
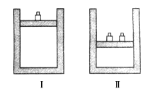
A. Ⅰ和Ⅱ中活化分子数相同
B. Ⅰ和Ⅱ中活化分子百分数相同
C. Ⅰ和Ⅱ中单位体积内活化分子数相等
D. Ⅰ中化学反应速率比Ⅱ中的小
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、W为四种短周期主族元素,且原子序数依次增大。已知X的最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,Y原子的最外层电子数是W原子最外层电子数的2倍,Z原子最外层只有1个电子。下列说法正确的是( )
A. 离子半径:![]() B. Z和Y形成的化合物可能含有非极性键
B. Z和Y形成的化合物可能含有非极性键
C. 氢化物的稳定性:![]() D. 最高价氧化物对应水化物的碱性:
D. 最高价氧化物对应水化物的碱性:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:![]() ,下列“水”电池在海水中放电时的有关说法正确的是( )
,下列“水”电池在海水中放电时的有关说法正确的是( )
A. 负极反应式:![]()
B. ![]() 不断向“水”电池的正极移动
不断向“水”电池的正极移动
C. 每生成![]() 转移5 mol电子
转移5 mol电子
D. 该电池工作时,电子由![]() 电极向Ag电极移动
电极向Ag电极移动
查看答案和解析>>
科目: 来源: 题型:
【题目】金属铜的提炼多从黄铜矿开始,黄铜矿在焙烧过程中主要反应之一的化学方程式为![]()
![]() 。下列说法正确的是( )
。下列说法正确的是( )
A. 每生成![]() ,有4mol硫被氧化
,有4mol硫被氧化
B. ![]() 只作还原剂,
只作还原剂,![]() 只作氧化剂
只作氧化剂
C. ![]() 既是氧化产物又是还原产物
既是氧化产物又是还原产物
D. 若有![]() 参加反应,则上述反应中共有
参加反应,则上述反应中共有![]() 转移
转移
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)按如图所示操作,充分反应后:
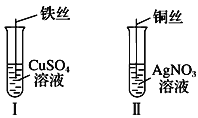
①Ⅰ中发生反应的离子方程式为______________;
②Ⅱ中铜丝上观察到的现象是_____________;
③结合Ⅰ、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为________。
(2)黑火药爆炸时发生反应:2KNO3+S+3C=K2S+N2↑+3CO2↑,其中被还原的元素是__,被氧化的元素是____,氧化剂是____,还原剂是__,氧化产物是____,还原产物是_____。
(3)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应物中氧化产物是_____;若反应中转移了0.3 mol电子,则还原产物的质量是____g。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上电解 Na2CO3的原理如图所示。下列说法不正确的是( )

A. 阴极产生的物质 A 是 H2
B. 电解一段时间后,阳极附近溶液的 PH 将增大
C. 该离子交换膜应为阳离子交换膜
D. 阳极电极反应为 4CO32-+2H2O-4e-=4HCO3-+O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,向一定体积 0.1mol/L 醋酸溶液中逐滴加入等浓度的 NaOH 溶液,溶液中pOH 与 pH 的变化关系如图所示,则正确的是( )
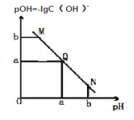
A. M 点所示溶液导电能力强于 Q 点
B. N 点所示溶液中 c(Na+)>c(CH3COO-)
C. Q 点所示的溶液 pH 一定等于 7
D. Q 点加入 NaOH 溶液的体积等于醋酸溶液的体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com