
科目: 来源: 题型:
【题目】(1)将a mol Cl2 通入含b mol FeBr2的溶液中,当0< a / b≤1/2 时,反应的离子方程式为:2Fe2+ + Cl2 = 2Fe3+ + 2Cl- ,写出另2个可能发生的离子方程式。
①当 a / b =1时___;②当a / b≥3/2时_______。
(2)观察反应①②,总结规律,并模仿反应①②方程式完成下列问题:①Al(OH)3 +H2O![]() Al(OH)4― + H+;②NH3+H2O
Al(OH)4― + H+;②NH3+H2O![]() NH4+ + OH―。
NH4+ + OH―。
(A)已知B(OH)3是一元弱酸,试写出其电离方程式: ___;
(B)N2H4是二元弱碱,其电离分步进行,第一步电离方程式N2H4+H2O![]() N2H5+ + OH―,试写出其第二步电离方程式_____。
N2H5+ + OH―,试写出其第二步电离方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如表中评价合理的是( )
选项 | 化学反应及其离子方程式 | 评价 |
A | NaHSO4溶液与Ba(OH)2溶液反应至SO42-沉淀完全:2H++ SO42-+Ba2++2OH==BaSO4↓+2H2O | 正确 |
B | 向碳酸镁浊液中加入足量稀盐酸:CO32- +2H+ | 错误,碳酸镁不应写成离子形式 |
C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色:Fe3++3H2O==Fe(OH)3↓+3H+ | 正确 |
D | 碳酸氢钠与足量澄清石灰水反应:2HCO3-+Ca2++2OH-==CaCO3↓+CO32-+2H2O | 正确 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素 X、Y、Z、W的原子序数依次增大,四种元素形成的单质依次为m、n、p、q;r、t、u 是这些元素组成的二元化合物,其中u为葡萄酒中的抑菌成分;25 ℃,0.01 mol/L的v溶液中:  = 1.0×10-10。上述物质的转化关系如图所示,下列说法不正确的是
= 1.0×10-10。上述物质的转化关系如图所示,下列说法不正确的是

A. 简单离子半径:W>Y>Z>X
B. W,Y分別与X元素形成的简单化合物的沸点: Y> W
C. Z2Y和ZX都只存在离子键
D. v能抑制水的电离,u能促进水的电离
查看答案和解析>>
科目: 来源: 题型:
【题目】36.5 g HCl溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,NA表示阿伏加德罗常数,则下列叙述中正确的是( )
A.所得溶液的质量分数:w=![]() B.所得溶液的物质的量浓度为1 mol·L-1
B.所得溶液的物质的量浓度为1 mol·L-1
C.36.5 g HCl气体占有的体积为22.4 LD.所得溶液中含有NA个HCl分子
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既不是氧化剂也不是还原剂.下列反应与Cl2+SO2+2H2O=H2SO4+2HCl相比较,水的作用完全相同的是( )
A.2H2O![]() 2H2↑+O2↑B.4Fe(OH)2+O2+2H2O=4Fe(OH)3
2H2↑+O2↑B.4Fe(OH)2+O2+2H2O=4Fe(OH)3
C.2Na+2H2O=2NaOH+H2↑D.C + H2O ![]() CO + H2
CO + H2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式书写正确的是 ( )
A. 氯化钙溶液中通入CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+
B. 以石墨作电极电解氯化铝溶液:2Cl-+ 2H2O![]() 2OH-+ H2↑+ Cl2↑
2OH-+ H2↑+ Cl2↑
C. Ca(C1O)2溶液中通人过量的SO2气体:ClO-+SO2+H2O=HSO3-+HClO
D. 向明矾溶液中加入氢氧化钡溶液至沉淀的质量最大:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】欲配制0.2mol/L 的NaOH溶液980mL,有以下仪器:
①烧杯②漏斗③托盘天平(带砝码)④玻璃棒⑤胶头滴管
(1)配制时,必须使用的仪器有____________(填代号),还缺少的玻璃仪器是____________________。该实验中两次用到玻璃棒,其作用分别是____________________,____________________。
(2)使用容量瓶前必须进行的一步操作是_____________________。
(3)根据计算应用托盘天平称量NaOH_______g。
(4)请你分析下列哪些操作会引起所配浓度偏大________(填写字母)。
A.将NaOH放在滤纸上称量
B.称取NaOH的砝码已生锈
C.容量瓶未干燥即用来配制溶液
D.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容;
E.往容量瓶转移时,有少量液体溅出
F.在容量瓶中定容时视线如图所示
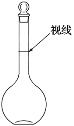
G.烧杯未进行洗涤
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
(5)若定容时不小心使液面超过了刻度线,应采取的措施是_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】关于NaHCO3溶液的表述正确的是
A. c (Na+)=c (HCO3-)+c (CO32-)+c (H2CO3)
B. c (Na+)+c (H+)=c (HCO3-)+c (CO32-)+c (OH-)
C. HCO3- 的电离程度大于HCO3-的水解程度
D. 其电离方程式为:NaHCO3![]() Na++H++CO32-
Na++H++CO32-
查看答案和解析>>
科目: 来源: 题型:
【题目】可用于分离或提纯物质的方法有:过滤、蒸发结晶、蒸馏、萃取、分液、洗气。根据需求填下列装置的序号:
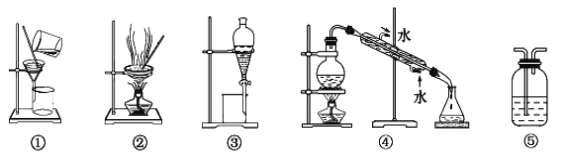
(1)分离Na2CO3溶液和CCl4,选_____(填序号),操作名称为________。
(2)用氢氧化钠溶液吸收O2中混有的杂质Cl2,选_______,操作名称为________。
(3)除去澄清石灰水中悬浮的CaCO3颗粒选______,操作名称为__________。
(4)制取蒸馏水,选________,操作名称为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应mA(s)+nB(g)![]() eC(g)+f D(g),当其它条件不变,平衡时C的百分含量(C%)和压强(P)的关系如图,下列叙述正确的是
eC(g)+f D(g),当其它条件不变,平衡时C的百分含量(C%)和压强(P)的关系如图,下列叙述正确的是
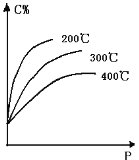
A. 化学方程式中n<e+f
B. 达到平衡后,加入催化剂,则C%增大
C. 达到平衡后,若升温,平衡逆向移动
D. 达到平衡后,增加A的量,平衡正向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com