
科目: 来源: 题型:
【题目】某溶液中可能含有OH-、CO32-、A1O2-、SiO32-、SO42-、HCO3-、Na+、Fe3+、Mg2+、Al3+等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如下图所示。下列说法正确的是

A. 原溶液中可能含有Na2SO4、可能不含有CO32-
B. 原溶液中一定含有的阴离子只有:OH-、A1O2-、CO32-
C. 原溶液中含CO32-与A1O2-的物质的量之比为3:4
D. a-d>3/4
查看答案和解析>>
科目: 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:
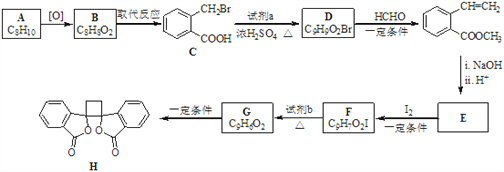
已知:i.RCH2Br ![]() R﹣HC═CH﹣R′
R﹣HC═CH﹣R′
ii.R﹣HC═CH﹣R′![]()
![]()
iii.R﹣HC═CH﹣R′![]()

(以上R、R'、R'代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是_______________________。
(2)D的结构简式是_______________________________。
(3)由F生成G的反应类型是________________________________________。
(4)由E与I2在一定条件下反应生成F的化学方程式是_____________________;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是_______________________________。
(5)下列说法正确的是___________(选填字母序号)。
A. G存在顺反异构体
B. 由G生成H的反应是加成反应
C. 1 mol G最多可以与1 mol H2发生加成反应
D. 1 mol F或1 mol H与足量NaOH溶液反应,均消耗2 molNaOH
(6)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成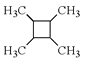 写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___________________
写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___________________
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答下列问题:
(1)画出氯离子的结构示意图_____。
(2)写出漂白粉有效成分的化学式_____。
(3)19g 某二价金属氯化物 ACl2 中含有 0.4 molCl-,则 ACl2 的摩尔质量为_____g/mol。
(4)写出一水合氨的电离方程式_________。
(5)表示“氯碱工业”的离子方程式_________。
(6)NH4HCO3 溶液中加入过量 NaOH 溶液的离子方程式为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】高锰酸钾是一种典型的强氧化剂。
(1)在用 KMnO4 酸性溶液处理固体 Cu2S 时,发生的反应如下:8MnO4-+5Cu2S+44H+=10Cu2++5SO2↑+8Mn2++22H2O
①还原产物为_____。
②被氧化的元素是_____
③氧化剂与还原剂的物质的量之比为_____
④每生成 2.24 L(标况下)SO2,转移电子数目是_____
(2)用 KMnO4 酸性溶液处理固体 CuS 时,也可将 CuS 反应成 Cu2+和 SO2。写出该离子反应方程式_____
(3)15.8g KMnO4,加热分解后剩余固体 15.0 g。该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体 A,产物中锰元素以 Mn2+存在,则气体 A 的物质的量为_____mol。
查看答案和解析>>
科目: 来源: 题型:
【题目】钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
(1)叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生 6.72 L(标准状况下)氮气,至少需要叠氮化钠_____g。
(2)为实现金属钠在隔绝空气条件下与水反应并收集生成的气体,某研究 性学习小组设计了如图发生装置.
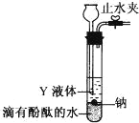
①写出 Na 与水反应的离子方程式_____。
②Y 液体可以选用_____
A.煤油 B.酒精 C.四氯化碳
③实验前检验该装置气密性的方法是:关闭止水夹,通过_________(填装置名称)向试管中加水至产生液面差,一段时间后,_____(填现象),则气密性良好。
(3)1mol 过氧化钠与 1.6mol 碳酸氢钠固体混合后,在密闭的容器中加热充分反应,排出气体物质后冷却,残留的固体物质及对应的物质的量(可不填满)。
物质 | 物质的量/mol |
__________ | __________ |
__________ | __________ |
查看答案和解析>>
科目: 来源: 题型:
【题目】为了探究硫酸亚铁的分解产物,进行了如下图装置所示的实验,打开K1和K2,缓缓通入N2,一段时间后加热,实验后反应管中残留固体为红色粉末,BaCl2溶液中有白色沉淀产生,品红溶液中红色褪去,检查氢氧化钠溶液出口处无氧气产生。下列说法错误的是

A. 氢氧化钠溶液的作用是吸收多余的SO2气体
B. 反应管内产生的红色粉末可能是Fe2O3
C. BaCl2溶液的目的是检验SO3的存在,此处用Ba(NO3)2溶液也可以检验SO3
D. 反应管内得到的氧化产物和还原产物物质的量之比为1:1
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是某位同学设计的实验装置,制取 Cl2 并以 Cl2 为原料制备纯净的无水 FeCl3粉末。已知:无水 FeCl3 遇水强烈反应。

(1)A 为氯气发生装置,写出反应的化学方程式:_____。
(2)装置 B 的作用是_____。
(3)实验时需要用到下列所有操作:a.点燃 A 处的酒精灯;b.打开分液漏斗旋塞,放入浓盐酸;c.点燃 D 处的酒精灯;d.检查装置气密性。
请给出上述操作的正确顺序_____(填字母)
(4)D 中实验现象为_________。
(5)装置 E 中倒置漏斗作用是_____。
(6)某同学设计的上述实验装置示意图有一处不合理,请提出改进方案__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】无机化合物 A 和 NaH 都是重要的还原剂,遇水都强烈反应。一定条件下,2.4g NaH 与气体 B 反应生成 3.9g 化合物 A 和 2.24L(已折算成标准状况)的 H2。已知气体 B 可使湿润红色石蕊试纸变蓝。请回答下列问题:
(1)B 的化学式是_____。
(2)NaH 与气体 B 反应生成化合物 A 的化学方程式_____。该反应中 A 是_____。
A.氧化产物 B.还原产物 C.既不是氧化产物也不是还原产物
(3)0.1molA 与足量盐酸发生非氧化还原反应最多消耗 HCl_____mol
(4)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,同时得到混合气体, 测得其平均摩尔质量为 25 g/mol,写出该反应的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某种胃药的有效成分为碳酸钙,测定其中碳酸钙含量的操作如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①配制1.60mol/L稀盐酸和1.60mol/LNaOH溶液;
②向一粒研碎后的药片(1.60g)中加入20.00mL蒸馏水;
③用1.60mol/LNaOH溶液中和过量的稀盐酸,记录所消耗的NaOH溶液的体积;
④加入25.00mL1.60mol/L稀盐酸。
请回答下列问题:
(1)正确的操作顺序是__________________________(填序号)
(2)测定过程中发生反应的离子方程式为___________________________________、___________________________。
(3)该测定实验共进行了4次。4次测定所消耗的NaOH溶液的体积如下:
测定次数 | 第1次 | 第2次 | 第3次 | 第4次 |
V(NaOH(aq))/mL | 13.00 | 12.90 | 13.10 | 13.00 |
实验室现有50mL、100mL、250mL、500mL4种规格的容量瓶,则配制NaOH溶液应选用的容量瓶的规格为___________。
(4)①配制上述NaOH溶液时需要的主要仪器有托盘天平、烧杯、________________。
②该实验的第一步是计算,称取_____gNaOH固体。
③用烧杯称取NaOH固体时,下列操作步骤的正确顺序是__________________(相同的操作可重复使用)。
a.调整天平零点 b.将砝码放回砝码盒 c.将游码拨回零刻度处
d.称取小烧杯的质量 e.称取小烧杯和NaOH的质量 f.记录称量的数据
④称取NaOH固体时,若将砝码放在天平左盘,将NaOH固体放在右盘,游码在1.4的刻度线处。则实际称得的NaOH固体为____________g。
⑤写出下列操作对所配制的溶液浓度造成的影响(填“偏大”“偏小”或“不变”)。
a.称量时砝码与NaOH固体在托盘中位置颠倒:______________。
b.未洗涤烧杯及玻璃棒:______________。
c.定容摇匀后,发现液面低于刻度线,重新加水至刻度线:______________。
⑥取50mL上述配制准确的NaOH溶液,加水稀释至100mL,所得NaOH溶液的物质的量浓度为________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组进行氯气性质的实验探究,设计了如图实验装置来制备并验证氯气的性质(部分夹持装置未画出)。请回答相关问题:
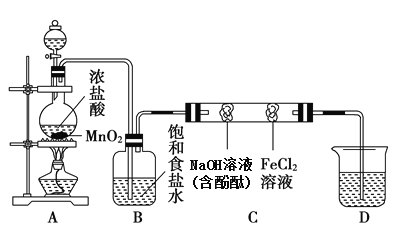
(1)A中放置固体二氧化锰的装置名称是_________。
(2)制备实验开始时,先检查装置气密性,如何检查整套装置的气密性?_____________________________________________________________。
(3)检查完装置的气密性后,接下来的操作依次是________(填序号)。
A.往烧瓶中加入MnO2粉末 B.加热 C.往烧瓶中加入浓盐酸
(4)写出A中反应的化学方程式________________________________。
(5)装置B的作用是______________________________________________。
(6)硬质玻璃管C中事先装有两个蘸有相关试剂的棉球,左侧棉球的实验现象为________________;产生该现象的原因可能是: _______________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com