
科目: 来源: 题型:
【题目】正硼酸(H3BO3)是一种片层状结构白色晶体,有与石墨相似的层状结构,受热易分解,层内的H3BO3分子通过氢键相连(如图所示),则下列有关说法中不正确的是

A. 正硼酸晶体属于分子晶体
B. 正硼酸分子的稳定性与氢键无关
C. 1molH3BO3晶体中含有3mol氢键
D. B原子杂化轨道的类型sp2,层间的H3BO3分子通过共价键相连
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关说法不正确的是( )
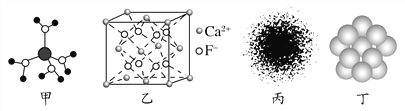
A. 水合铜离子的模型如图甲所示,1个水合铜离子中有4个配位键
B. CaF2晶体的晶胞如图乙所示,每个CaF2晶胞平均占有4个Ca2+
C. H原子的电子云图如图丙所示,H原子核外大多数电子在原子核附近运动
D. 金属Cu中Cu原子堆积模型如图丁所示,为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目: 来源: 题型:
【题目】通常情况下,NCl3是一种油状液体,其分子空间构型与NH3相似,下列对NCl3和NH3的有关叙述正确的是( )
A. 分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B. NCl3分子是非极性分子
C. NBr3比NCl3易挥发
D. 在氨水中,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式为![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】将64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为22.4 L。请计算(写出计算过程):
(1)NO标况下的体积________
(2)参加反应的HNO3的物质的量________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一个密闭容器中,A与B在一定条件下发生反应:A(s)+B(g)![]() C(g) △H<0,改变B的物质的量并使之达到平衡,得到如下图所示的平衡曲线,下列说法不正确的是
C(g) △H<0,改变B的物质的量并使之达到平衡,得到如下图所示的平衡曲线,下列说法不正确的是

A.增加少量A物质,平衡不移动
B.斜率为平衡常数,且随温度升高而减小
C.恒温恒容时,加入少量He气,容器内气体密度不变
D.缩小容器体积,气体平均相对分子质量不变
查看答案和解析>>
科目: 来源: 题型:
【题目】如图中A为电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,容器C为盛有500mL各0.1mol/L的CuSO4和K2SO4混合液的电解槽,e、f均为铂电极。接通电路后,发现B上的c点显红色,C中阳极产生1.12L(标况)气体,电解过程不考虑能量损失。

(1)电源A上的b为______极,滤纸B上d为______极。
(2)写出B上所发生的反应的化学反应方程式_________。
(3)写出C容器中阳极产生的气体是_______(填名称),另一极增重____克。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)分子式为C3H6O2的二元混合物,如果在核磁共振氢谱上观察到氢原子给出的峰有两种情况.第一种情况峰给出的强度为1:1;第二种情况峰给出的强度为3:2:1。由此推断混合物的组成可能是_______(写结构简式,写一种组合即可)。如图是一种分子式为C3H6O2的有机物的红外光谱图,则该有机物的结构简式为______。

(2)经测定,某有机物含碳77.8%、氢7.4%、氧14.8%;用质谱仪测定结果如下图。分析求此有机物的分子式为______。若此有机物能与烧碱反应,且苯环上的一溴代物只有四种,试写出它的结构简式_______。

查看答案和解析>>
科目: 来源: 题型:
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备:

请回答下列问题:
(1)环戊二烯分子中最多有____个原子共平面。
(2)金刚烷的分子式为_______,其分子中的-CH2-基团有____个。
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:

其中,反应①的产物名称是_______,反应②的反应试剂和反应条件是________。
(4)已知烯烃能发生如下反应:

![]()
![]() RCHO +
RCHO + ![]()
请写出下列反应产物的结构简式:
![]()
![]() _____
_____
查看答案和解析>>
科目: 来源: 题型:
【题目】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.Zn+H2SO4=ZnSO4+H2↑;B.NaOH+HCl=NaCl+H2O。能设计成原电池的反应是__________(填“A”或“B”)。
(2)将锌片和铜片按如图方式插入100 mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是__________。
A.甲、乙均为化学能转变为电能的装置
B.甲中铜片质量减少、乙中锌片质量减少
C.两烧杯中溶液的c(H+)均减小
②在相同时间内,两烧杯中产生气泡的速度:甲__________乙(填“>”、“<”或“=”)。
③请写出图中构成原电池的正极电极反应式:__________。
④当乙中产生2.24 L(标准状况)气体时,将锌铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.2 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】可燃冰是另一种CH4的重要来源,利用可燃冰制备的甲烷可以设计成如下燃料电池,可以作为“移动的发电厂”,源源不断的对外供电,下列说法错误的是

A.a电极通入甲烷气体,作负极
B.每通入1mol CH4,有8mol e-通过质子交换膜
C.b电极的电极反应式为:O2+4e-+4H+=2H2O
D.催化剂电极采用疏松多孔结构可提高电极反应效率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com