
科目: 来源: 题型:
【题目】某小组选用下列装置,利用反应![]() ,通过测量生成水的质量
,通过测量生成水的质量![]() 来测定Cu的相对原子质量。实验中先称取氧化铜的质量
来测定Cu的相对原子质量。实验中先称取氧化铜的质量![]() 为a g。
为a g。
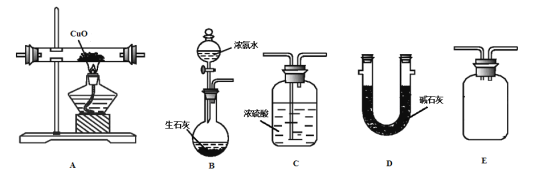
(1)浓氨水滴入生石灰中能制得NH3的原因是______________。
(2)甲同学按B-A-E-C-D的顺序连接装置,该方案是否可行__________,理由是_______________。
(3)乙同学按B-A-D-E-C的顺序连接装置,则装置C的作用是___________________________。
(4)丙同学认为乙同学测量的![]() 会偏高,理由是_____,你认为该如何改进?___
会偏高,理由是_____,你认为该如何改进?___
(5)若实验中测得![]() g,则Cu的相对原子质量为_______。(用含a,b的代数式表示)。
g,则Cu的相对原子质量为_______。(用含a,b的代数式表示)。
(6)若CuO中混有Cu,则该实验测定结果_________。(选填“偏大”、“偏小”或“不影响”)
查看答案和解析>>
科目: 来源: 题型:
【题目】活性炭、纯碱(Na2CO3)和小苏打(NaHCO3)在生产、生活中应用广泛。完成下列填空:
(1)活性炭可用于处理大气污染物NO:![]() ,已知NO的转化率随温度升高而降低。降低温度,重新达到平衡,判断下列各物理量的变化:(选填“增大”、“减小”或“不变”)
,已知NO的转化率随温度升高而降低。降低温度,重新达到平衡,判断下列各物理量的变化:(选填“增大”、“减小”或“不变”)![]() __________;N2的体积分数___________;平衡常数K____________。
__________;N2的体积分数___________;平衡常数K____________。
(2)将氨气和二氧化碳先后通入饱和食盐水中,可观察到的现象是_______;写出相关反应的化学方程式______________
(3)小苏打既能跟酸反应,又能跟碱反应,应用勒夏特列原理进行解释。_____________
(4)比较同温下浓度均为0.01mol/L的①H2CO3、②Na2CO3、③NaHCO3、④NH4HCO3四种溶液中![]() 的大小关系为_______(用编号表示)。
的大小关系为_______(用编号表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用催化技术可将汽车尾气中的 NO 和 CO 转变成 CO2 和 N2,化学方程式:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入 NO 和 CO,测得不同时间的 NO 和 CO 的浓度如表:
2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入 NO 和 CO,测得不同时间的 NO 和 CO 的浓度如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/×10-3mol/L | 1.00 | 0.45 | 0.25 | 0.15 | 0.10 | 0.10 |
c(CO)/×10-3mol/L | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
下列说法中不正确的是( )
A. 2 s 内的平均反应速率 v(N2)=1.875×10-4 mol·L-1·s-1
B. 在该温度下,反应的平衡常数 K=5
C. 若将容积缩小为原来的一半,NO 转化率大于 90%
D. 使用催化剂可以提高单位时间内 CO 和 NO 的处理量
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是利用二氧化硅制备硅及其化合物的流程,下列说法正确的是( )
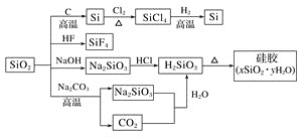
A.SiO2属于两性氧化物
B.盛放NaOH溶液的试剂瓶能用玻璃塞
C.硅胶吸水后可重复再生
D.图中所示转化反应都是氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),形成沉淀所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示。下列说法不正确的是

A. 若向沉淀剂Na2S溶液通入HC1气体至中性,存在关系: c(HS-)+2c(H2S)=c(Cl-)
B. 该温度下,Ksp(MnS)大于1.0×10-35
C. 若将MnS、FeS的饱和溶液等体积混合,再加入足量的浓 Na2S溶液,发生的反应为MnS沉淀少于FeS
D. 向l00mL浓度均为10-5mol·L-1Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol·L-1Na2S溶液,ZnS先沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】无机物可根据其组成和性质进行分类。现有Cl2、Na、CO2、Na2O、Na2O2、NH3六种物质,完成下列填空:
(1)由分子构成的单质是____________,属于极性分子的是____________。
(2)既有离子键又有共价键的物质的电子式为____________。
(3)上述化合物中组成元素的原子半径由大到小的顺序是____________。
(4)根据与水反应的不同,上述物质可分成A组(CO2、Na2O和NH3)和B组(Cl2、Na和Na2O2),分组的依据是________________________。
(5)在酸性高锰酸钾溶液中加入Na2O2,溶液褪色,发生反应![]() (未配平),配平该反应的离子方程式并标出电子转移方向与数目。____________
(未配平),配平该反应的离子方程式并标出电子转移方向与数目。____________
查看答案和解析>>
科目: 来源: 题型:
【题目】在一个2L的密闭容器中,发生反应: 2SO3 (g)![]() 2SO2 (g)+ O2 (g) — Q (Q>0),其中SO3的物质的量随时间变化如图所示,下列判断错误的是
2SO2 (g)+ O2 (g) — Q (Q>0),其中SO3的物质的量随时间变化如图所示,下列判断错误的是

A. 0~8min内v(SO3)=0.025mol/(L·min)
B. 8min时,v逆(SO2)=2v正(O2)
C. 8min时,容器内压强保持不变
D. 若8min时将容器压缩为1L,n(SO3)的变化如图中a
查看答案和解析>>
科目: 来源: 题型:
【题目】能证明SO2具有漂白性的是( )
A.酸性![]() 溶液中通入
溶液中通入![]() 气体后紫红色消失
气体后紫红色消失
B.滴有酚酞的NaOH溶液中通入![]() 气体后红色消失
气体后红色消失
C.品红溶液中通入![]() 气体后红色消失
气体后红色消失
D.溴水中通入![]() 气体后橙色消失
气体后橙色消失
查看答案和解析>>
科目: 来源: 题型:
【题目】兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示:
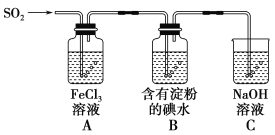
(1)SO2气体和Fe3+反应的氧化产物、还原产物分别是________、________
(2)下列实验方案适用于在实验室制取所需SO2的是________。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与浓H2SO4共热
(3)装置C的作用是__________________________________________________。
(4)装置B中反应的离子方程式_________________________________________________。
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入NaOH溶液,产生白色沉淀,并迅速转为灰绿,最后呈红褐色。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是方案_____,原因是__________________________________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列事实,不能用勒夏特列原理解释的是( )
A. 热纯碱溶液比冷的纯碱溶液洗涤油污的能力强
B. 向MgCO3沉淀中滴加NaOH溶液可以得到Mg(OH)2沉淀
C. 水的离子积随温度变化如表格所示: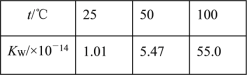
D. 对CO(g)+NO2(g) ![]() CO2(g)+NO(g)平衡体系增大压强可使颜色变深
CO2(g)+NO(g)平衡体系增大压强可使颜色变深
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com