
科目: 来源: 题型:
【题目】I.在①苯 ②苯酚 ③甲苯 ④氯乙烷 ⑤乙烯 ⑥乙醇中,(填编号)
(1)能和金属钠反应放出H2的有_______________
(2)能与NaOH溶液反应的有_______________
(3)常温下能与溴水反应的有_______________
(4)能使酸性KMnO4溶液褪色的烃有_______________
II.已知1-丁烯A发生如下反应,F的核磁共振氢谱有三种吸收峰,
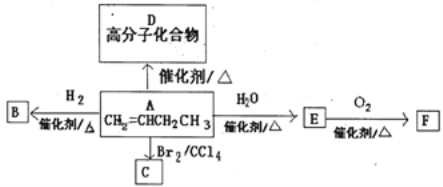
(1)A分子内所含官能团的名称____________。
(2)写出下列反应的化学方程式:
①A→D___________________。
②E→F___________________ 。
(3)由A的官能团位置异构的同分异构体G生成1,4-丁二醇需______步,请写出最后一步反应的化学方程式_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在室温下,下列五种溶液:①0.1 mol·L-1 NH4Cl溶液 ②0.1 mol·L-1 CH3COONH4溶液 ③0.1 mol·L-1 NH4HSO4溶液 ④0.1 mol·L-1氨水 ⑤0.1 mol·L-1 NH3·H2O和0.1 mol·L-1 NH4Cl混合液
请根据要求填写下列空白:
(1)溶液①呈_______(填“酸”、“碱”或“中”)性,其原因是___________(用离子方程式表示)。
(2)上述5中溶液中,其中水的电离程度最大的是_______(填序号)
(3)在上述①、②、③、④溶液中c(NH4+)浓度由大到小的顺序是_____________。(填序号)
(4) 室温下,测得溶液②的pH=7,则CH3COO-与NH4+浓度的大小关系是c(CH3COO-)______c(NH4+)(填“>”、“<”或“=”)。
(5)用标准盐酸溶液滴定未知浓度的氨水实验。滴定可选用的指示剂为_______(填“甲基橙”或 “酚酞”)。上述滴定开始时滴定管尖嘴处无气泡,完成时滴定管尖嘴处留有气泡,则会导致滴定结果______(填“偏高”或 “偏低”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在密闭容器中X2 (g)+2Y2 (g)![]() Z(g)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是( )
Z(g)的反应,X2、Y2、Z的起始浓度依次为0.2mol/L、0.3mol/L、0.3mol/L,当反应达到其最大限度(即化学平衡状态)时,各物质的浓度有可能的是( )
A.c(Z) ═0.45mol/LB.c(X2) ═0.3mol/L
C.c(X2) ═0.5mol/LD.c(Y2) ═0.5mol/L
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组研究亚硝酸钠,查阅下列资料,试根据信息回答下列问题。
药品 | NaNO2 (亚硝酸钠) |
性质 | 1.在酸性溶液中有较强氧化性,能将Fe2+ 氧化成Fe3+ ; 2.AgNO2是一种难溶于水、易溶于酸的盐。 |
(1)已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。请用双线桥表示电子转移的方向和数目:___。
(2)误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+ 而中毒,可服用维生素C 解毒。下列分析错误的是__(填序号)。
A.NaNO2被还原 B.维生素C具有还原性
C.还原性:维生素C>Fe2+ D.NaNO2是还原剂
(3)下列方法中,可用来区分NaNO2和NaCl的是___(填序号)。
A.焰色反应 B.分别滴加酸化FeSO4溶液和KSCN溶液
C.在酸性条件下加入KI 淀粉溶液 D.分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是( )
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中 减小
减小
B.将CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C.向氨水中加入盐酸至中性,溶液中![]() <1
<1
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中![]() 不变
不变
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,将3molA和1molB投入容积为2L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g)。2min末测得此时容器中C和D的浓度为0.2mol/L和0.4mol/L。下列叙述正确的是 ( )
xC(g)+2D(g)。2min末测得此时容器中C和D的浓度为0.2mol/L和0.4mol/L。下列叙述正确的是 ( )
A. x=2
B. 2min时,B的浓度为0.4mol/L
C. 0~2min内B的反应速率为0.2mol·L-·min-
D. 此时A的转化率为40%
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量的Na2CO3和NaHCO3的均匀混合物分成质量不等的三份,分别与50mL相同浓度的盐酸反应,得到气体的质量与固体混合物的质量关系如下表所示:
组 别 | 1 | 2 | 3 |
固体质量/g | 3.80 | 6.20 | 7.20 |
气体质量/g | 1.76 | 2.64 | 2.64 |
(1)上表中_______组数据表明盐酸参加反应后有剩余,理由是______________。
(2)上表中第2组数据中盐酸____________(填“过量”、“适量”、“不足量”)。
(3)通过计算求Na2CO3和NaHCO3的质量分数各为_________、____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。预计在未来20年里,不可能有替代钕铁硼磁铁的磁性材料岀现。生产钕铁硼磁铁的主要原材料有稀土金属钕、纯铁、铝、硼以及其他稀土原料。
(1) 钕(Nd)为60号元素,在周期表中第______周期;基态铁原子的外围电子排布式为______
(2) 实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如图所示。

① 已知Al2Cl6分子中正负电荷中心重合,则Al2Cl6属于_________分子(填“极性”或“非极性”),分子中A1原采取______杂化。
② Al2Cl6与过量NaOH溶液反应生成Na[Al(OH)4],[A1(OH)4]-中存在的化学键有_____ (填选项字母)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(3) B元素及与其同周期相邻的两种元素第一电离能由小到大的顺序为______(用元素符号表示)。B元素可在一定条件下生成H3O+ [B(OH)F3]- ,该化合物中电负性最大的元素的原子中,所有能层电子的电子云轮廓图形状有______种
(4) 因材料中含有大量的钕和铁,容易锈蚀是它的一大弱点。可电镀镍(Ni)、锌(Zn)等进行表面涂层处理。已知Ni可以形成[Ni(NH3)6]Cl2,该配合物中配体分子的空间构型为 _______ 。
(5) 已知立方BN晶体硬而脆,其晶胞结构如图所示,设晶胞中最近的B、N原子之间的距离为anm,晶体的密度为bg·cm-3,则阿伏加德罗常数为_________ mol-1(用含a、b的代数式表示)

查看答案和解析>>
科目: 来源: 题型:
【题目】对于2SO2(g)+O2(g) 2SO3(g),ΔH<0,根据下图,下列说法错误的是( )

A.t2时使用了催化剂B.t3时采取减小反应体系压强的措施
C.t5时采取升温的措施D.反应在t6时刻,SO3体积分数最大
查看答案和解析>>
科目: 来源: 题型:
【题目】室温下,某同学进行CO2与Na2O2反应的探究实验,回答下列问题。
(1)用如图装置制备纯净的CO2
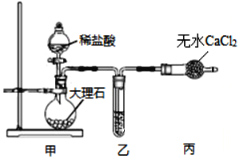
①甲装置中盛放稀盐酸的仪器名称是_____,乙装置中应加入的试剂是_______________。
②装置甲中反应的离子方程式为__________。
(2)按照下面的装置图进行实验(夹持装置略)。
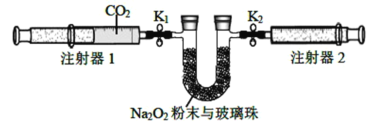
①先组装仪器,然后_______________,再用注射器1抽取100 mL纯净的CO2,将其连接在K1处,注射器2的活塞推到底后连接在K2处,具支U形管中装入足量的Na2O2粉末与玻璃珠。
②打开止水夹K1、K2,向右推动注射器1的活塞,可观察到的现象是_______________。
③实验过程中,需缓慢推入CO2,其目的是________________,反应的化学方程式为_______________。
(3)实验结束后,当注射器1的活塞推到底时,测得注射器2中气体体积为65 mL,则反应消耗CO2的体积是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com