
科目: 来源: 题型:
【题目】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
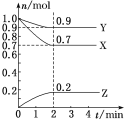
(1)由图中所给数据进行分析,该反应的化学方程式为____________________
(2)反应从开始至2min,用Z的浓度变化表示的平均反应速率为v(Z)=__________________。
(3)2min反应达平衡容器内混合气体的总压强比起始时________(填“增大”“减小”或“不变”);混合气体密度比起始时________(填“增大”“减小”或“不变”)。
(4)下列措施能加快反应速率的是________。
A.恒压时充入He B.恒容时充入He
C.恒容时充入X D.及时分离出Z
E.升高温度F.选择高效的催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、J、Q五种短周期主族元素的原子序数依次增大,元素Z在地壳中含量最高,J元素的焰色反应呈黄色,Q的最外层电子数与其电子总数比为3∶8,X能与J形成离子化合物,且J+的半径大于X-的半径,Y2是空气主要成分之一。请回答下列问题:
(1)Q元素在周期表中的位置是_______________________________________。
(2)这五种元素的原子半径从大到小的顺序为__________________(填元素符号)。
(3)元素的非金属性:Z________Q(填“>”或“<”),下列各项中,不能说明这一结论的事实有________(填字母)。
A.Q的氢化物的水溶液放置在空气中会变浑浊
B.Z与Q形成的化合物中元素的化合价
C.Z和Q的单质的状态
D.Z和Q在周期表中的位置
(4)Q的氢化物与它的+4价氧化物反应的化学方程式为________________________。
(5)X与Y可形成分子A,也可形成阳离子B,A与B都是10电子构型,写出阳离子B的电子式:__________,如何检验溶液中阳离子B的存在,请说出简要的实验方法:______,A的空间构型是______;实验室制备气体A的化学方程式:_______________________,
查看答案和解析>>
科目: 来源: 题型:
【题目】某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)
A. 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-="==" Cl-+ ClO-+ H2O
B. 该消毒液的pH约为12:ClO-+ H2O![]() HClO+ OH-
HClO+ OH-
C. 该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++ Cl-+ ClO-= Cl2↑+H2O
D. 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ ClO-= HClO+CH3COO—
查看答案和解析>>
科目: 来源: 题型:
【题目】请回答下列问题:
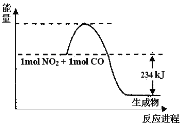
Ⅰ.如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图(图中涉及物质均为气态),请写出NO2和CO反应的热化学方程式:______
Ⅱ.现有①BaCl2②水晶③金属铝④Na2SO4⑤冰⑥碘片六种物质,按下列要求回答(填编号,下同):
(1)熔化时不需要破坏化学键的是_______,熔化时需要破坏共价键的是_______,能导电的是______。
(2)属于离子化合物的是________,只有离子键的物质是________,属于共价化合物的是______。
(3)①的电子式是________;⑤的结构式是________,⑤的空间构型是______,⑤中分子间作用力除了范德华力外,还含有______,因此而引起一些特殊的性质,请举出一种:______。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. 向稀HNO3中滴加NaHSO3溶液:H++HSO![]() ===SO2↑+H2O
===SO2↑+H2O
B. 硫酸铝溶液中加入过量氨水:Al3++3OH-===Al(OH)3↓
C. 向含有2 mol FeI2的溶液中通入2.5 mol Cl2:8I-+2Fe2++5Cl2===10Cl-+4I2+2Fe3+
D. 用酸性高锰酸钾标准溶液滴定草酸:2MnO![]() +16H++5C2O
+16H++5C2O![]() ===2Mn2++10CO2↑+8H2O
===2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验的反应原理用离子方程式表示正确的是( )
A. 室温下,测的氯化铵溶液pH<7,证明一水合氨的是弱碱:NH4++2H2O=NH3·H2O+H3O+
B. 用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑
C. 用碳酸氢钠溶液检验水杨酸中的羧基:
 +2HCO3-→
+2HCO3-→ +2H2O+2CO2↑
+2H2O+2CO2↑
D. 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 饱和Na2CO3溶液与CaSO4固体反应:CO32+CaSO4![]() CaCO3+SO42
CaCO3+SO42
B. 酸化NaIO3和NaI的混合溶液:I +IO3+6H+![]() I2+3H2O
I2+3H2O
C. KClO碱性溶液与Fe(OH)3反应:3ClO+2Fe(OH)3![]() 2FeO42+3Cl+4H++H2O
2FeO42+3Cl+4H++H2O
D. 电解饱和食盐水:2Cl+2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】将O2和NH3的混合气体448mL通过加热的三氧化二铬,充分反应后,再通过足量的水,最终收集到44.8mL气体。原混合气体中O2的体积可能是(假设氨全部被氧化;气体体积均已换算成标准状况)
A. 231.5mL B. 268.8mL C. 287.5mL D. 313.6mL
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,可逆反应2NO2![]() 2NO+O2在恒容密闭容器中进行,达到平衡状态的标志是
2NO+O2在恒容密闭容器中进行,达到平衡状态的标志是
①单位时间内生成nmolO2的同时生成2nmolNO2;
②单位时间内生成nmolO2的同时生成2nmolNO;
③混合气体的密度不再改变;
④混合气体的颜色不再改变;
⑤密闭容器中压强不再改变;
A.②③⑤B.①③⑤C.①④⑤D.全部
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2资源化利用的方法之一是合成二甲醚(CH3OCH3)。
(1)CO2 催化加氢合成二甲醚的过程中主要发生下列反应:反应I:CO2(g) + H2(g) ![]() CO(g) + H2O(g) H= +41.2 kJmol-1;反应II: 2CO2(g) + 6H2(g)
CO(g) + H2O(g) H= +41.2 kJmol-1;反应II: 2CO2(g) + 6H2(g) ![]() CH3OCH3(g) + 3H2O(g) H = - 122.5 kJmol-1;其中,反应II 分以下①②两步完成,请写出反应①的热化学方程式。
CH3OCH3(g) + 3H2O(g) H = - 122.5 kJmol-1;其中,反应II 分以下①②两步完成,请写出反应①的热化学方程式。
① _____
②2 CH3OH(g) ![]() CH3OCH3(g) + H2O(g) H = -23.5 kJmol-1
CH3OCH3(g) + H2O(g) H = -23.5 kJmol-1
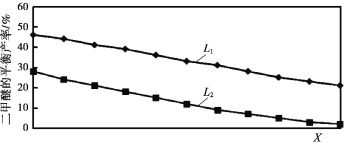
(2)L(L1、L2)、X分别代表压强或温度,如图表示L一定时,反应II中二甲醚的平衡产率随X变化的关系,其中X代表的物理量是_____。判断L1、L2的大小,并简述理由:_____。
(3)恒压时,在CO2和H2起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性![]() )随温度变化如图。
)随温度变化如图。
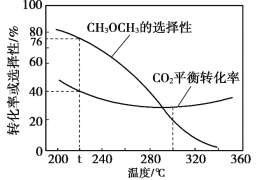
①t ℃ 时,起始投入a molCO2,b mol H2,达到平衡时反应II消耗的H2的物质的量为______mol。
②温度高于300℃,CO2平衡转化率随温度升高而增大的原因是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com