
科目: 来源: 题型:
【题目】下列有机反应不属于取代反应的是
A. C2H5OH + CH3COOH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
B. H﹣C≡C﹣H + HCl![]() H2C=CHCl
H2C=CHCl
C. ![]() + HNO3
+ HNO3![]()
![]() +H2O
+H2O
D. ![]() + Br2
+ Br2![]()
![]() +HBr
+HBr
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为________。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为______________。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为________。
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度________________
(2)该溶液的质量分数_________________________
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
溶质的质量分数 | 溶液的密度(g·cm-3) | |
第一份溶液 | w1 | ρ1 |
第二份溶液 | w2 | ρ2 |
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=________。(用以上字母表示)
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3___w4;若ρ1<ρ2,w3______w4(填“>”“<”或“=”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.某同学帮助水质检测站配制480mL0.5mol·L-1NaOH溶液以备使用。
(1)其操作步骤如乙图所示,则甲图操作应在乙图中的______之间。
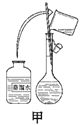
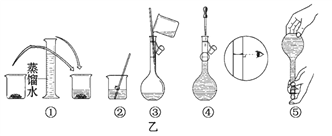
A.②与③ B.①与② C.③与④
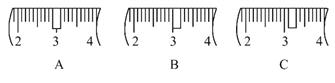
(2)该同学应称取NaOH固体________g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在在下图中选出能正确表示游码位置的选项________(填字母)。
Ⅱ.现有下列A、B、C三种常用化学仪器,请回答下列有关问题:
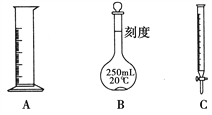
(1)三种化学仪器中标有“0”刻度的为________(填名称)。
(2)三种化学仪器在使用时首先需要检验是否漏液的为________(填字母代号)。
(3)用三种化学仪器中的一种对液体体积进行计量,正确的读数为n mL,仰视读数为x mL,俯视读数为y mL,若y>n>x,则所用量器是________(填名称)。
Ⅲ.化学课外活动小组设计了如下图所示的一套气体发生、收集和尾气吸收装置,以探究该装置的多功能性。
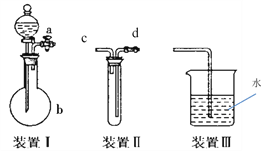
(1)实验前要检验装置Ⅰ的气密性,写出操作方法____________;
(2)利用装置Ⅱ可直接收集CO2,进气口为_____________。
(3)以上三个装置可组成实验室制取NH3,利用装置Ⅲ 吸收NH3时会发生倒吸,可向水中再加入一种液体可防止倒吸的发生,该液体为________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物G是一种药物合成中间体,其合成路线如下:

回答下列问题:
(1)B的名称为____;D中含有的无氧官能团结构简式为____。
(2)反应④的反应类型为____;反应⑥生成G和X两种有机物,其中X的结构简为_____。
(3)反应⑤的化学反应方程式为_____(C6H7BrS用结构简式表示)。
(4)满足下列条件的C的同分异构体共有 ___种,写出其中一种有机物的结构简式:____。
①苯环上连有碳碳三键;②核磁共振氢谱共有三组波峰。
(5)请设计由苯甲醇制备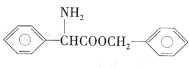 的合成路线(无机试剂任选)____:
的合成路线(无机试剂任选)____:
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:
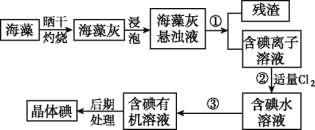
(1)实验室灼烧海藻,需要下列仪器中的____(填字母)。
a.试管 b.烧杯 c.坩埚 d.泥三角 e.铁三脚架 f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①_____________,③______。
(3)提取碘的过程中,可选择的有机试剂是_____。
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
(4)小组用CCl4萃取碘水中的碘,在分液漏斗中进行,下层液体呈____色;他们打开分液漏斗活塞,却未见液体流下,原因可能是____________________。
(5)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
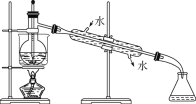
①________; ② _________; ③_________。
(6)进行上述蒸馏操作时,使用水浴加热的原因是___________,最后晶态碘在____里聚集。
Ⅱ.海水开发利用可以提取NaCl和Mg(OH)2。
(1)海水中提取的NaCl中若混有少量的KClO3固体(KClO3溶解度随温度变化大),可通过溶解、________、_________等操作净化。
(2)生成Mg(OH)2用的沉淀剂一般是生石灰或熟石灰,所以Mg(OH)2沉淀中会混有Ca(OH)2,可通过反复洗涤去除Ca(OH)2,检验沉淀是否洗净的操作方法_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】硒(Se)是一种非金属元素。可以用作光敏材料、电解锰行业催化剂、动物体必需的营养元素和植物有益的营养元素等。请回答下列问题:
(1) Se元素基态原子的电子排布式为____;第四周期中第一电离能比Se元素大的共有____种(氪元素除外)。
(2)气态SeO3分子的价层电子对互斥模型为____ ;SeO42-离子中Se原子的杂化方式为 ___ 。
(3)固态SeO2是以[SeO3]角锥体以角相连接的展平的聚合结构,每一锥体带有一悬垂的终端O原子(如下图1所示)。
①图1中Se-O键键长较短的是 ___(填“a"或“b"),其原因是______。
②SeO2熔点为350℃,固态SeO2属于___晶体,其熔点远高于SO2(-75.5℃)的原因是 ____。
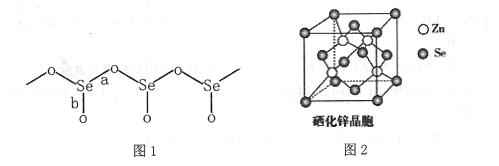
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如上图2所示,其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得ZnSe的晶胞参数a=0. 560nm,则Se2-的离子半径r(Se2-)= ____nm(计算结果保留3位有效数字,下同);硒化锌晶体的密度为________ g.cm-3。
查看答案和解析>>
科目: 来源: 题型:
【题目】以含1个碳原子物质(如CO、CO2、CH4、CH3OH等)为原料的“碳一化学”处于未来化学产业的核心,成为科学家研究的重要课题。请回答下列问题:
(1)已知CO、H2、CH3OH(g)的燃烧热分别为-283.0kJ·mol-1、-285.8kJ·mol-l、-764.5kJ·mol-l。则反应I:CO(g)+2H2(g)=CH3OH(g)△H=___
(2)在温度T时,向体积为2L恒容容器中充入3molCO和H2的混合气体,发生反应I,反应达到平衡时,CH3OH(g)的体积分数(φ)与n(H2)/n(CO)的关系如下图所示。
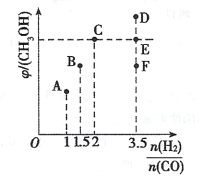
①当起始n(H2)/n(CO)=1时,从反应开始到平衡前,CO的体积分数将___(填“增大”、“减小”或“不变”)。
②当起始n(H2)/n(CO)=2时,反应经过l0min达到平衡,CO转化率为0.5,则0~l0min内平均反应速率v(H2)=___。
③当起始n(H2)/n(CO)=3.5时,达到平衡后,CH3OH的体积分数可能是图像中的__。(填“D”、“E”或“E”点)。
(3)在一容积可变的密闭容器中充有10molCO和20molH2,发生反应I。CO的平衡转化率(α)与温度(T)、压强(P)的关系如下图所示。
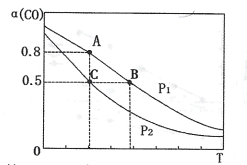
①压强P1=___(填“<”、“=”或“>”)P2;A、B、C三点的平衡常数KA、KB、KC的大小关系为___(用“<”、“=”或“>”表示)。
②若达到平衡状态C时,容器体积为10L,则在平衡状态A时容器体积为____L。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga______As,第一电离能Ga________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为_____________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是____________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGa g·mol-1 和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。
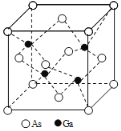
Ⅱ.醋酸铜可合成复合材料石墨烯Cu,其制备原料为CuSO4、NH3·H2O和醋酸等。
(1)写出一种与SO42-互为等电子体的分子__________。
(2)二聚醋酸铜的结构示意图如图所示,Cu2+的配位数为___________。
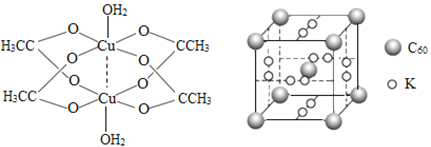
(3)石墨烯可转化为富勒烯(C60),C60和K能形成新型化合物,其晶胞如图所示,晶胞参数为a nm该化合物中K原子和C60分子的个数比为______,该晶体的密度ρ=______g/cm3(列出计算式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国某地粉煤灰中主要含有Al2O3,除此之外还含有Ga2O3及少量Fe2O3、CaO、MgO和SiO2等物质。已知从粉煤灰中回收铝并提取镓的工艺流程如下所示:
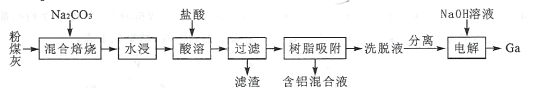
回答下列问题:
(1)焙烧前,应将粉煤灰与纯碱粉末充分混合,其原因是____;混合焙烧时,Al2O3、Ga2O3均发生类似于SiO2的反应,试写出Ga2O3在此过程中发生反应的化学方程式:____。
(2)滤渣的成分是____ ;含铝混合液中除了大量A13+之外,还有Fe3+和少量Mg2+,由混合液制取纯净Al(OH)3的实验方案是_____。
(3)洗脱液中往往还有少量Fe3+,需要进一步分离。若使Fe3+恰好完全沉淀[c(Fe3+)= l×l0-5mol·L-l]时,Ga3+浓度至少为_____mol·L-l才会开始沉淀。(已知:![]() 。)
。)
(4)电解过程中,Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电,则电解方程式为____;电解过程中需要保持溶液为pH=11以上的原因是 ___。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列变化属于①放热反应 ②吸热反应
A:分解反应 B:化合反应C:置换反应
(1)氯酸钾分解制氧气,既是_______(填①或②)又是______。(填A或B或C,下同)
(2)生石灰跟水反应生成熟石灰,既是_______又是______。
(3)锌粒与稀硫酸的反应,既是_______又是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com