
科目: 来源: 题型:
【题目】人体血液里Ca2+的浓度一般采用mg/cm3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
(配制KMnO4标准溶液)如图是配制50 mL KMnO4标准溶液的过程示意图。


(1)请你观察图示判断,其中不正确的操作有(填序号)________。
(2)其中确定50 mL溶液体积的容器是(填名称)________。
(3)如果用图示的操作配制溶液,所配制的溶液浓度将________(填“偏大”或“偏小”)。
(测定血液样品中Ca2+的浓度)抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol/L KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(4)已知草酸跟KMnO4溶液反应的离子方程式为:
2MnO4-+5H2C2O4+6H+===2Mnx++10CO2↑+8H2O则方程式中的x=________。
(5)经过计算,血液样品中Ca2+的浓度为________mg/cm3。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应条件是研究化学反应的重要方向。
(1)化工原料异丁烯(C4H8)可由异丁烷(C4H10)直接催化脱氢制备:C4H10(g) ![]() C4H8(g)+H2(g) △H=+139kJ·mol-1
C4H8(g)+H2(g) △H=+139kJ·mol-1
一定条件下,以异丁烷为原料生产异丁烯,在202kPa和808kPa下异丁烷平衡转化率随温度的变化如图所示。
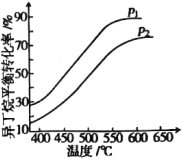
①p1=_______kPa,选择异丁烯制备的温度条件是550~600℃的理由是_________________。
②若平衡混合气中异丁烯的体积分数为25%,则异丁烷的平衡转化率为_______%(保留小数点后1位)。
(2)异丁烷催化脱氢制备异丁烯的研究热点是催化活性组分以及载体的选择。下表是以V-Fe-K-0为催化活性物质,反应时间相同时,测得的不同温度、不同载体条件下的数据。
温度/℃ | 570 | 580 | 590 | 600 | 610 | |
以r-Al2O3为载体 | 异丁烷转化率/% | 36.41 | 36.49 | 38.42 | 39.23 | 42.48 |
异丁烯收率/% | 26. 17 | 27. 11 | 27.51 | 26.56 | 26.22 | |
以TiO2为载体 | 异丁烷转化率/% | 30.23 | 30.87 | 32.23 | 33.63 | 33.92 |
异丁烯收率/% | 25.88 | 27.39 | 28.23 | 28.81 | 29.30 | |
说明:收率=(生产目标产物的原料量/原料的进料量)×100%
①由上表数据,可以得到的结论是____________(填字母序号)。
a 载体会影响催化剂的活性 b 载体会影响催化剂的选择性 c 载体会影响化学平衡常数
②分析以γ-Al2O3为载体时异丁烯收率随温度变化的可能原因:__________。
(3)工业上用复合氧化钴(组成为Co3O4)、碳酸锂以Li/Co(原子比)=1混合,在空气中900℃下加热5小时制备锂离子电池正极材料LiCo O2,写出制备LiCoO2的化学方程式__________。废旧的锂离子电池需要回收,“放电处理”废旧的锂离子电池有利于锂在正极回收的原因是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物) 为原料制备Mg CO3·3H2O。实验过程如下:

(1)酸溶过程中主要反应的热化学方程式为:
MgCO3(s)+2H+(aq)=Mg2+(aq)+CO2(g)+H2O H = -50.4kJ·mol-1
Mg2SiO4(s) +4 H+(aq)=2 Mg2+(aq) +H2SiO3(s) + H2O(l) H =-225.4kJ··mol-1
向Mg2SiO4悬浊液中通入CO2析出H2SiO3的热化学方程式为__________,该反应能正向进行的热力学原因是_________。该反应的平衡常数表达式为__________。
(2)对氧化后的溶液,加入萃取剂磷酸二异辛酯(C16H35O4P)的煤油溶液,并调节pH为1.4~4.3,萃取剂的体积约为水溶液的0.5倍,充分振荡、静止、分层(上层为含三价铁的有机层),分液。向分液得到的有机层加硫酸反萃取得到硫酸铁溶液,从而与有机层分离。萃取反应为:Fe2(SO4)3(水层)+6HA(有机层)=2FeA3(有机层)+3H2SO4(水层)
①提高萃取效率的措施有__________。
A 适当提高萃取剂的浓度 B 适当提高溶液酸度
C 充分振荡,多次萃取 D 不断地从下层排除出有机层
②在反萃取中加硫酸的作用是___________。
(3)萃取后的水溶液制备Mg CO3·3H2O的实验方案:滴加氨水调节溶液的pH在一定范围内,过滤。向滤液中滴加Na2 CO3溶液,搅拌、静置、过滤,用水洗涤固体2~3次,在50℃下干燥,得到Mg CO3·3H2O。[已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全]。
①调节溶液pH的范围____________。
②判断向滤液中滴加Na2CO3溶液过量的方法__________。
(4)从废渣制备Mg CO3·3H2O的整体实验方案看,酸溶时所加H2SO4不宜过量太多的原因是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室采用镁屑与液溴为原料制备无水MgBr2, 装置如图, 主要步骤如下:

步骤1组装好仪器,向三颈瓶中装入10g镁屑和150mL无水乙醚;装置B中加入15mL液溴。
步骤2 。
步骤3反应完毕后恢复至室温,过滤,滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4室温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁, 加热至160℃分解得无水Mg Br2产品。
已知:①Mg和Br2反应剧烈放热;Mg Br2具有强吸水性。
②MgBr2+3C2H5OC2H5=MgBr2·3C2H5OC2H5
③乙醚是重要有机溶剂,医用麻醉剂;易挥发储存于阴凉、通风处;易燃远离火源。
请回答下列问题:
(1)写出步骤2的操作是_________。
(2)仪器A的名称是__________。装置中碱石灰的作用__________。冰水浴的目的__________。
(3)该实验从安全角度考虑除了控制反应温度外,还需要注意:
①_________②_______。
(4)制备MgBr2装置中橡胶塞和用乳胶管连接的玻璃管口都要用锡箔纸包住的目的是_________。
(5)有关步骤4的说法,正确的是__________。
A 可用95%的乙醇代替苯溶解粗品 B 洗涤晶体可选用0℃的苯
C 加热至160℃的主要目的是除去苯 D 该步骤的目的是除去乙醚和可能残留的溴
(6)为测定产品的纯度,可用EDTA(简写为Y4-) 标准溶液滴定,反应的离子方程式:Mg2+ +Y4-═MgY2-
①先称取0.7500g无水MgBr2产品,溶解后,等体积分装在3只锥形瓶中, 用0.0500mol·L-1的EDTA标准溶液滴定至终点,三次消耗EDTA标准溶液的体积平均为26.50mL, 则测得无水MgBr2产品的纯度是_______(保留4位有效数字)。
②滴定前未用标准溶液润洗滴定管,则测得产品纯度___________(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】回答下列问题:
(1)写出实验室制NH3的化学方程式_________________;
(2)写出铅蓄电池的负极电极反应式__________________;
(3)写出Ba(OH)2·8H2O与NH4Cl晶体搅拌反应的化学方程式_______________;
(4)画出稀有气体氪的原子结构示意图__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气是未来最理想的能源,最近科学家研制出利用太阳能产生激光,在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O![]() 2H2↑+O2↑。制得的氢气可用于燃料电池。请回答下列问题:
2H2↑+O2↑。制得的氢气可用于燃料电池。请回答下列问题:
(1)太阳光分解海水时,实现了_____能转变为_______能,二氧化钛作_______。生成的氢气用于燃料电池时,实现了_______能转变为_______能。太阳光分解海水的反应属于_______(填“放热”或“吸热”)反应。
(2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2--4e-=2H2O;B极:O2+4e-=2O2-,则A极是电池的________极;电子从该极________(填“流入”或“流出”)。
(3)请根据下列信息,写出H2燃烧热的热化学方程式________。
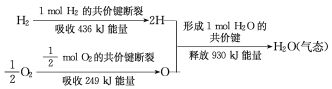
H2O(l) = H2O(g) ΔH = +44kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2 O42-) =0.100mol·L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列说法错误的是

A.由图可知:Ka2(H2C2O4)的数量级为10-4
B.若将0.05mol NaHC2O4和0.05mol Na2C2O4固体完全溶于水配成1L溶液,所得混合液的pH为4
C.c(Na+)=0.100mol·L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-)
D.用标准的氢氧化钠溶液滴定H2C2O4溶液,可用酚酞做指示剂
查看答案和解析>>
科目: 来源: 题型:
【题目】让生态环境更秀美、人民生活更幸福!为此,天津冬季取暖许多家庭用上了清洁能源天然气。实际生产中天然气需要脱硫,在1200℃时,工艺中会发生下列反应:
①H2S(g)+![]() O2(g)=SO2(g)+H2O(g) ΔH1
O2(g)=SO2(g)+H2O(g) ΔH1
②2H2S(g)+SO2(g)=![]() S2(g)+2H2O(g) ΔH2
S2(g)+2H2O(g) ΔH2
③H2S(g)+![]() O2(g)=S(g)+H2O(g) ΔH3
O2(g)=S(g)+H2O(g) ΔH3
④2S(g)=S2(g) ΔH4
则ΔH4的正确表达式为( )
A.ΔH4=![]() (ΔH1 +ΔH2-3ΔH3)
(ΔH1 +ΔH2-3ΔH3)
B.ΔH4=![]() (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C.ΔH4=![]() (ΔH1-ΔH2+3ΔH3)
(ΔH1-ΔH2+3ΔH3)
D.ΔH4=![]() (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
科目: 来源: 题型:
【题目】在100mL混合酸的溶液中,硝酸的物质的量浓度为0.4mol/L,硫酸的物质的量浓度为0.2mol/L,向其中加入6.4g铜粉,微热,使其充分反应,生成NO的物质的量( )
A.0.02molB.0.03molC.0.04molD.0.1mol
查看答案和解析>>
科目: 来源: 题型:
【题目】最近科学家利用下列装置图成功地实现了CO2和H2O合成CH4。下列叙述错误的是( )

A.电池工作时,实现了将太阳能转化为电能
B.电池内 H+ 透过质子交换膜从左向右移动
C.铜电极为正极,电极反应式为CO2+8H+-8e-=CH4+2H2O
D.为提高该人工光合系统的工作效率,可向装置中加入少量稀硫酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com