
科目: 来源: 题型:
【题目】一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是( )
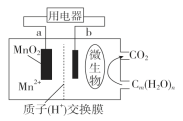
A. 电池工作时,电子由a流向b
B. 微生物所在电极区放电时发生还原反应
C. 放电过程中,H+从正极区移向负极区
D. 正极反应式为:MnO2+4H++2e-===Mn2++2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:
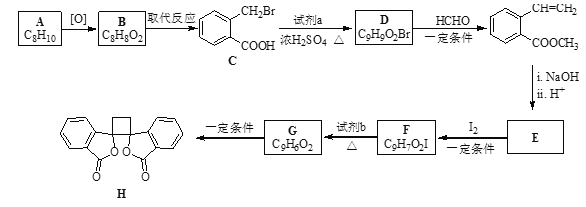
已知:i.RCH2Br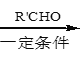 R-HC=CH-R’
R-HC=CH-R’
ii. R-HC=CH-R’ 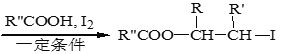
iii. R-HC=CH-R’ 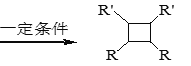
(以上R、R’、R’’代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是_________
(2)B的结构简式是__________。
(3)由C生成D的化学方程式是__________。
(4)由E与I2在一定条件下反应生成F的化学方程式是___________。
(5)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成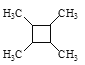 ,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。______
,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。______
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组以烯烃D和芳香烃A为原料合成医药中间体J的路线如下(部分产物和条件省略):
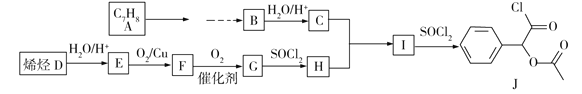
已知:RCN![]() RCOOH
RCOOH![]() RCOCl
RCOCl![]() RCOOR1
RCOOR1
回答下列问题:
(1)标准状况下,烯烃D的密度为1.25 g·L1。则D的结构简式为________。A的名称是____________。
(2)G所含官能团名称是____________;D→E的反应类型是____________。
(3)写出C+H→I的化学方程式:________________________。
(4)J的分子式为____________。
(5)B的同分异构体中,同时符合下列条件的结构有____________种。
①有4个碳原子在同一条直线上;
②含有—NH2和—OH且都与苯环直接相连。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知热化学方程式:
① C2H2(g) +![]() O2(g) = 2CO2(g)+H2O(l) ΔH1=-1301.0 kJmol-1
O2(g) = 2CO2(g)+H2O(l) ΔH1=-1301.0 kJmol-1
② C(s)+ O2(g) = CO2(g) △H2=-393.5 kJmol-1
③ H2(g)+![]() O2(g) = H2O(l) △H3 = -285.8 kJ·mol-1
O2(g) = H2O(l) △H3 = -285.8 kJ·mol-1
则反应④ 2C(s)+ H2(g) = C2H2(g)的△H为( )
A.+228.2 kJ·mol-1B.-228.2 kJ·mol-1
C.+1301.0 kJ·mol-1D.+621.7 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年为“国际化学元素周期表年”。下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W与X的最高化合价之和为8。下列说法不正确的是( )
![]()
A.原子半径:W<X
B.X的最高价氧化物的水化物是强碱
C.Y单质可用做半导体材料
D.气态氢化物热稳定性:Z<W
查看答案和解析>>
科目: 来源: 题型:
【题目】(12)烷烃A只可能有三种一氯取代产物B、C和D。C的结构简式是 。B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。以上反应及B的进一步反应如下所示。
。B和D分别与强碱的醇溶液共热,都只能得到有机化合物E。以上反应及B的进一步反应如下所示。

请回答下列问题:
(1)A的结构简式是_______________H的结构简式是________________
(2)B转化为F属于________反应,B转化为E的反应属于________反应(填反应类型名称)。
(3)写出F转化为G的化学方程式_____________ 。
(4)1.16 g H与足量NaHCO3作用,标准状况下可得CO2的体积是______mL。
(5)写出反应①的方程式______________
查看答案和解析>>
科目: 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如下:
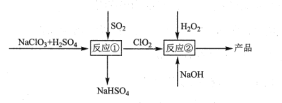
下列说法错误的是( )
A. 反应①阶段,参加反应的NaClO3和SO2的物质的量之比为2:1
B. 若反应①通过原电池来实现,则ClO2是正极产物
C. 反应②中的H2O2可用NaClO2代替
D. 反应②条件下,ClO2的氧化性大于H2O2
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室制备1,2-二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
CH2=CH2+Br2 → BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140 ℃脱水生成乙醚
用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
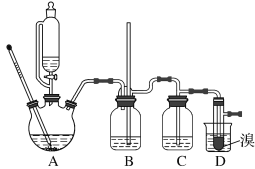
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/(g·cm-3) | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132. | 34.6 |
熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是________(填正确选项前的字母)。
a .引发反应 b. 加快反应速度 c. 防止乙醇挥发 d. 减少副产物乙醚生成
(2)在装置C中应加入________(填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体。
a .水 b .浓硫酸 c .氢氧化钠溶液 d .饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是_______________________。
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在________层(填“上”或“下”)。
(5)若产物中有少量未反应的Br2,最好用________(填正确选项前的字母)洗涤除去。
a 水 b 氢氧化钠溶液 c 碘化钠溶液 d 乙醇
(6)若产物中有少量副产物乙醚,可用________的方法除去。
(7)反应过程中应用冷水冷却装置D,其主要目的是_______________________;但又不能过度冷却(如用冰水),其原因是_______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应。实验记录如下:
序号 | I | II | III |
实验 步骤 |
充分振荡,加2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验 现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀 |
下列说法不正确的是( )
A.实验I、II、III中均发生了反应2Fe3++Cu===2Fe2++Cu2+
B.对比实验I、II、III说明白色沉淀的产生可能与铜粉的量及溶液的阴离子种类有关
C.实验II、III中加入蒸馏水后c(Cu2+)相同
D.向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于反应能量的说法正确的是( )
A.若反应A=B △H<0,说明A物质比B物质稳定,分子内共价键键能 A比B大
B.Zn(s)+CuSO4 (aq)==ZnSO4 (aq) +Cu(s) △H= -216 kJ·mol-1。则反应物总能量>生成物总能量
C.101kPa时,2H2(g)+O2(g)==2H2O(g) △H= -Q kJ·mol-1,则H2的燃烧热为1/2Q kJ·mol-l
D.H+(aq) +OH- (aq)=H2O(l) △H= -57.3 kJ·mol-1,含1mol NaOH的氢氧化钠溶液与含0.5mol CH3COOH的醋酸溶液混合后会放出57.3 kJ的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com