
科目: 来源: 题型:
【题目】以有机物A为原料通过一步反应即可制得重要有机化工产品P(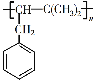 )。下列说法错误的是
)。下列说法错误的是
A.A的分子式为C11H14,可发生取代、氧化、加成等反应
B.由A生成P的反应类型为加成聚合反应,反应过程没有小分子生成
C.A的结构简式为![]() ,分子中所有碳原子不可能共面
,分子中所有碳原子不可能共面
D.1 mol A最多能与4 mol H2发生加成反应
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物F是一种重要的有机合成中间体,它的合成路线如下:
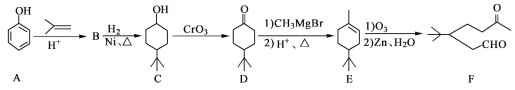
(1)化合物F中含氧官能团的名称是_________和_________。
(2)由B生成C的化学反应类型是________。
(3)写出化合物B的结构简式:__________。
(4)某化合物是D的同分异构体,且分子中只有三种不同化学环境的氢。写出该化合物的结构简式:__________(任写一种)。
(5)请根据已有知识并结合相关信息,写出以苯酚(![]() )和CH2=CH2为原料制备有机物
)和CH2=CH2为原料制备有机物![]() 的合成路线流程图_____________________________(无机试剂任用)。
的合成路线流程图_____________________________(无机试剂任用)。
合成路线流程图示例如下:
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图)
(1)经过一段时间后,两个实验中,首先观察到溶液变红的区域是_____(填代号)。
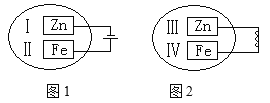
A.Ⅰ和Ⅲ附近 B.Ⅰ和Ⅳ附近 C.Ⅱ和Ⅲ附近 D.Ⅱ和Ⅳ附近
(2)试用化学用语(电极反应或离子方程式)和简练的语言说明相应区域溶液变红的原因:
图1:_____________________
图2:_____________________
(3)从金属腐蚀的角度看,铁片受到防腐保护的是_____(填“图1”或“图2”),这种防护方法的名称为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物W是一种医药化工合成中间体,其合成路线如下:
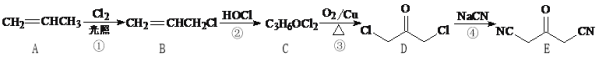
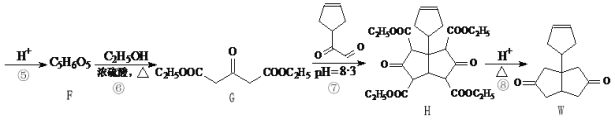
(1)B中官能团的名称是________和_________。
(2)反应④的反应类型是________。
(3)F的结构简式是_________。
(4)芳香化合物X是W的同分异构体,X能够发生银镜反应,核磁共振氢谱有五组峰,峰面积之比为6:4:3:2:1,写出X的一种结构简式:________。
(5)写出以1,2-二氯乙烷和![]() 为原料合成
为原料合成![]() 的合成路线流程图(无机试剂可任选)_________________。合成路线流程图示例如下:
的合成路线流程图(无机试剂可任选)_________________。合成路线流程图示例如下:![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】[化学——选修3:物质结构与性质](15分)
人体必需的元素包括常量元素与微量元素,常量元素包括碳、氢、氧、氮、钙、镁等,微量元素包括铁、铜、锌、氟、碘等,这些元素形成的化合物种类繁多,应用广泛。
(1)锌、铜、铁、钙四种元素与少儿生长发育息息相关,请写出Fe2+的核外电子排布式__________。
(2)1个Cu2+与2个H2N—CH2—COO形成含两个五元环结构的内配盐(化合物),其结构简式为_______________(用→标出配位键),在H2N—CH2—COO中,属于第二周期的元素的第一电离能由大到小的顺序是__________(用元素符号表示),N、C原子存在的相同杂化方式是_________杂化。
(3)碳酸盐中的阳离子不同,热分解温度就不同,查阅文献资料可知,离子半径r(Mg2+)=66 pm,r(Ca2+)=99 pm,r(Sr2+)=112 pm,r(Ba2+)=135 pm;碳酸盐分解温度T(MgCO3)=402℃,T(CaCO3)=825℃,T(SrCO3)=1172℃,T(BaCO3)=1360℃。分析数据得出的规律是_____________,解释出现此规律的原因是____________________________________。
(4)自然界的氟化钙矿物为萤石或氟石,CaF2的晶体结构呈立方体形,其结构如下:
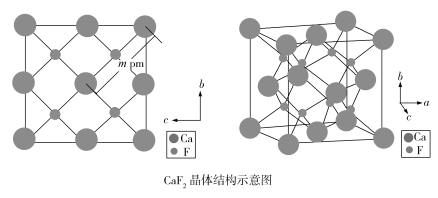
①两个最近的F之间的距离是___________pm(用含m的代数式表示)。
②CaF2晶胞体积与8个F形成的立方体的体积比为___________。
③CaF2晶胞的密度是___________g·cm3(化简至带根号的最简式,NA表示阿伏加德罗常数的值)。
[化学——选修5:有机化学基础](15分)
药物H在人体内具有抑制白色念球菌的作用,H可经下图所示合成路线进行制备。
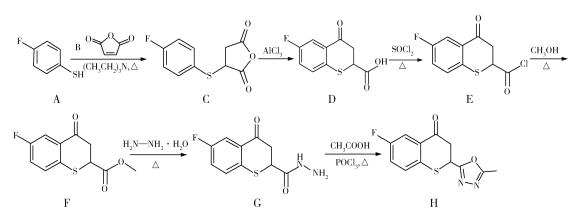
已知:硫醚键易被浓硫酸氧化。
回答下列问题:
(1)官能团SH的名称为巯(qiú)基,SH直接连在苯环上形成的物质属于硫酚,则A的名称为________________。D分子中含氧官能团的名称为________________。
(2)写出下列反应类型:A→C_____________,E→F_____________。
(3)F生成G的化学方程式为_______________________________________。
(4)下列关于D的说法正确的是_____________(填标号)。(已知:同时连接四个各不相同的原子或原子团的碳原子称为手性碳原子)
A.分子式为C10H7O3FS
B.分子中有2个手性碳原子
C.能与NaHCO3溶液、AgNO3溶液发生反应
D.能发生取代、氧化、加成、还原等反应
(5)M与A互为同系物,分子组成比A多1个CH2,M分子的可能结构有_______种;其中核磁共振氢谱有4组峰,且峰面积比为2∶2∶2∶1的物质的结构简式为_____________。
(6)有机化合物K(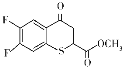 )是合成广谱抗念球菌药物的重要中间体,参考上述流程,设计以
)是合成广谱抗念球菌药物的重要中间体,参考上述流程,设计以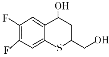 为原料的合成K的路线。_____________
为原料的合成K的路线。_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物E是一种药物中间体,合成路线如下:

(1)该路线中设计第Ⅰ、Ⅲ步的目的是________。
(2)步骤Ⅳ中X的结构简式为________。
(3)1 mol E与足量的H2反应,最多消耗H2_________mol。
(4)F是C的一种同分异构体,能与新制的氢氧化铜反应生成红色沉淀,遇FeCl3溶液显紫色,分子中含有4种不同环境的氢。F的结构简式为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(15分)含碳物质的价值型转化,有利于“减碳”和可持续性发展,有着重要的研究价值。请回答下列问题:
(1)已知CO分子中化学键为C≡O。相关的化学键键能数据如下:
化学键 | H—O | C≡O | C=O | H—H |
E/(kJ·mol1) | 463 | 1075 | 803 | 436 |
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=___________kJ·mol1。下列有利于提高CO平衡转化率的措施有_______________(填标号)。
CO2(g)+H2(g) ΔH=___________kJ·mol1。下列有利于提高CO平衡转化率的措施有_______________(填标号)。
a.增大压强 b.降低温度
c.提高原料气中H2O的比例 d.使用高效催化剂
(2)用惰性电极电解KHCO3溶液,可将空气中的CO2转化为甲酸根(HCOO),然后进一步可以制得重要有机化工原料甲酸。CO2发生反应的电极反应式为________________,若电解过程中转移1 mol电子,阳极生成气体的体积(标准状况)为_________L。
(3)乙苯催化脱氢制取苯乙烯的反应为:![]() (g)+CO2(g)
(g)+CO2(g)![]()
![]() (g)+CO(g)+H2O(g),其反应历程如下:
(g)+CO(g)+H2O(g),其反应历程如下:
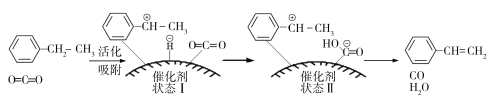
①由原料到状态Ⅰ____________能量(填“放出”或“吸收”)。
②一定温度下,向恒容密闭容器中充入2 mol乙苯和2 mol CO2,起始压强为p0,平衡时容器内气体总物质的量为5 mol,乙苯的转化率为_______,用平衡分压代替平衡浓度表示的化学平衡常数Kp=_______。[气体分压(p分)=气体总压(p总)×气体体积分数]
③乙苯平衡转化率与p(CO2)的关系如下图所示,请解释乙苯平衡转化率随着p(CO2)变化而变化的原因________________________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】借助于李比希法、现代科学仪器及化学实验可以测定有机物的组成和结构。实验兴趣小组用如下图所示的装置测定某有机物X(含元素C、H、O中的两种或三种)的组成。实验测得样品X消耗的质量为1.50g,高氯酸镁质量增加0.90g,碱石棉质量增加2.20g。
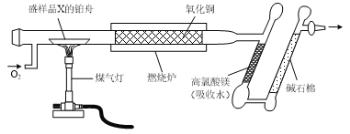
(1)由实验数据分析计算可得X的实验式为_____。
(2)若红外光谱测得X中含有“C=O”和“C-O-C”的结构,质谱法测得X的相对分子质量是60,则X的名称为_______。
(3)若实验测得相同状况下,X蒸汽的密度是H2密度的45倍(已知相同状况下,气体的密度比等于摩尔质量之比),X能发生银镜反应,1mol X最多能与2mol Na发生反应。则X的结构简式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】SO2、NO是大气污染物。吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):
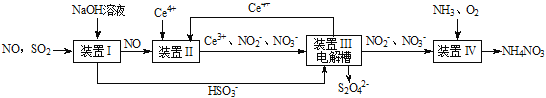
(1)装置Ⅰ中生成HSO3-的离子方程式为_____ 。
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图所示。
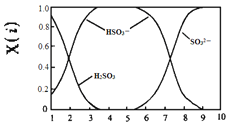
①下列说法正确的是_____(填字母序号)。
A.pH=8时,溶液中c(HSO3-) <c(SO32-)
B.pH=7时,溶液中c(Na+)=c(HSO3-)+c(SO32-)
C.为获得尽可能纯的NaHSO3,可将溶液的pH控制在4~5左右
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:_____。
(3)装置Ⅱ中,酸性条件下,NO被Ce4+氧化的产物主要是NO3-、NO2-,写出生成NO3-的离子方程式____。
(4)装置Ⅲ的作用之一是再生Ce4+,其原理如图所示。

①生成Ce4+的电极反应式为_________。
②生成Ce4+从电解槽的_____(填字母序号)口流出。
(5)已知进入装置Ⅳ的溶液中,NO2-的浓度为a g/L,要使1m3该溶液中的NO2-完全转化为NH4NO3,需至少向装置Ⅳ中通入标准状况下的O2___L。(用含a代数式表示,计算结果保留整数)
查看答案和解析>>
科目: 来源: 题型:
【题目】(14分)硫酸铜晶体(CuSO4·5H2O)是铜盐中重要的无机化工原料,广泛应用于农业、电镀、饲料添加剂、催化剂、石油、选矿、油漆等行业。
Ⅰ.采用孔雀石[主要成分CuCO3·Cu(OH)2]、硫酸(70%)、氨水为原料制取硫酸铜晶体。其工艺流程如下:
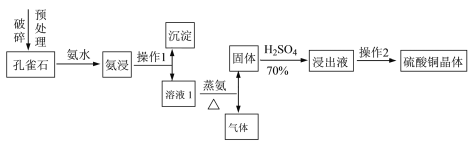
(1)预处理时要用破碎机将孔雀石破碎成粒子直径<1 mm,破碎的目的是____________________。
(2)已知氨浸时发生的反应为CuCO3·Cu(OH)2+8NH3·H2O![]() [Cu(NH3)4]2(OH)2CO3+8H2O,蒸氨时得到的固体呈黑色,请写出蒸氨时的反应方程式:______________________。
[Cu(NH3)4]2(OH)2CO3+8H2O,蒸氨时得到的固体呈黑色,请写出蒸氨时的反应方程式:______________________。
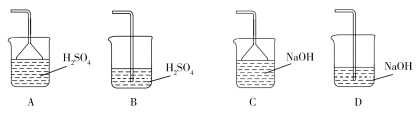
(3)蒸氨出来的气体有污染,需要净化处理,下图装置中合适的为___________(填标号);经吸收净化所得的溶液用途是_______________(任写一条)。
(4)操作2为一系列的操作,通过加热浓缩、冷却结晶、___________、洗涤、___________等操作得到硫酸铜晶体。
Ⅱ.采用金属铜单质制备硫酸铜晶体
(5)教材中用金属铜单质与浓硫酸反应制备硫酸铜,虽然生产工艺简洁,但在实际生产过程中不采用,其原因是______________________(任写两条)。
(6)某兴趣小组查阅资料得知:Cu+CuCl2![]() 2CuCl,4CuCl+O2+2H2O
2CuCl,4CuCl+O2+2H2O![]() 2[Cu(OH)2·CuCl2],[Cu(OH)2·CuCl2]+H2SO4
2[Cu(OH)2·CuCl2],[Cu(OH)2·CuCl2]+H2SO4![]() CuSO4+CuCl2+2H2O。现设计如下实验来制备硫酸铜晶体,装置如图:
CuSO4+CuCl2+2H2O。现设计如下实验来制备硫酸铜晶体,装置如图:
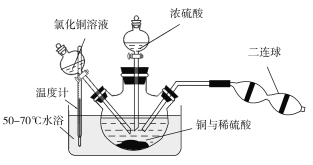
向铜和稀硫酸的混合物中加入氯化铜溶液,利用二连球鼓入空气,将铜溶解,当三颈烧瓶中呈乳状浑浊液时,滴加浓硫酸。
①盛装浓硫酸的仪器名称为___________。
②装置中加入CuCl2的作用是______________;最后可以利用重结晶的方法纯化硫酸铜晶体的原因为______________________。
③若开始时加入a g铜粉,含b g氯化铜溶质的氯化铜溶液,最后制得c g CuSO4·5H2O,假设整个过程中杂质不参与反应且不结晶,每步反应都进行得比较完全,则原铜粉的纯度为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com