
科目: 来源: 题型:
【题目】实验室用下述装置制取氯气,并用氯气进行下列实验。看图回答下列问题:
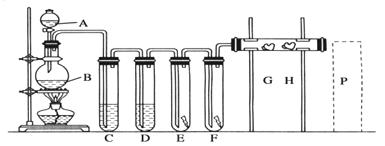
![]() 仪器的名称: ________。B中发生反应的化学方程式为____________。
仪器的名称: ________。B中发生反应的化学方程式为____________。
![]() 为了获得纯净干燥的氯气, C、D中应分别放入的试剂C为_________,作用是________________________;D中为___________。
为了获得纯净干燥的氯气, C、D中应分别放入的试剂C为_________,作用是________________________;D中为___________。
![]() 中为红色干布条,F中为红色湿布条,可观察到有色布条褪色的是______
中为红色干布条,F中为红色湿布条,可观察到有色布条褪色的是______![]() 填E或
填E或![]()
![]() 是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成__________,H是浸有NaBr溶液的棉花球,H处发生的离子方程式为_________________。
是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成__________,H是浸有NaBr溶液的棉花球,H处发生的离子方程式为_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于物质工业制备的说法中正确的是
A.接触法制硫酸时,在吸收塔中用水来吸收三氧化硫获得硫酸产品
B.工业上制备硝酸时产生的NOx,一般可以用NaOH溶液吸收
C.从海水中提取镁的过程涉及化合、分解、置换、复分解等反应类型
D.工业炼铁时,常用焦炭做还原剂在高温条件下还原铁矿石
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于氧化还原反应的说法正确的是
A.1mol Na2O2参与氧化还原反应,电子转移数一定为NA (NA为阿伏加德罗常数的值)
B.浓HCl和MnO2制氯气的反应中,参与反应的HCl中体现酸性和氧化性各占一半
C.VC可以防止亚铁离子转化成三价铁离子,主要原因是VC具有较强的还原性
D.NO2与水反应,氧化剂和还原剂的物质的量之比为2: 1
查看答案和解析>>
科目: 来源: 题型:
【题目】我国女药学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖。青蒿素的一种化学合成方法的部分工艺流程如图所示:
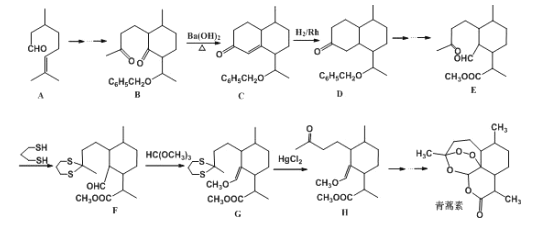
己知:①C6H5-表示苯基;②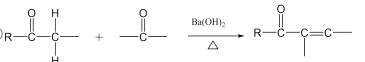
(1)化合物E中含有的含氧官能团有__、__和羰基(写名称)。
(2)合成路线中设计E→F、G→H的目的是__。
(3)B→C实际上是分两步反应进行的,先进行加成反应,再进行__反应。
(4)A在Sn-p沸石作用下,可生成同分异构体异蒲勒醇,己知异蒲勒醇分子中有3个手性碳原子(连有四个不同基团的碳原子称为手性碳原子),异蒲勒醇分子内脱水后再与H21:1发生1,4-加成可生成![]() ,则异蒲勒醇的结构简式为:__。
,则异蒲勒醇的结构简式为:__。
(5)A的同分异构体Y含有醛基和六元碳环,且环上只有一个支链,满足上述条件的Y有__种,其中核磁共振氢谱峰数最少的物质的结构简式为__。
(6)如图是以乙烯为原料制备苄基乙醛![]() 的合成路线流程图。
的合成路线流程图。
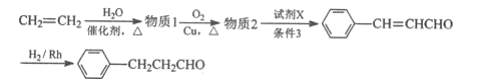
请填写下列空白(有机物写结构简式):
物质1为__;物质2为__;试剂X为__;条件3为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。填写下列空白:
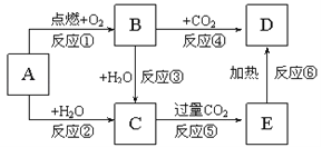
![]() 写出化学式:B__________,C______________,D __________________
写出化学式:B__________,C______________,D __________________
![]() 写出反应
写出反应![]() 的离子方程式:_______________________________________
的离子方程式:_______________________________________
![]() 写出反应
写出反应![]() 的化学反应方程式:_________________________________
的化学反应方程式:_________________________________
![]() 写出反应
写出反应![]() 的化学反应方程式,______________,若产生
的化学反应方程式,______________,若产生![]() 氧化产物,被还原的物质是__________,其物质的量是____mol,转移的电子数目______
氧化产物,被还原的物质是__________,其物质的量是____mol,转移的电子数目______
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家通过测量SiO2中的26Al和10Be两种元素的比例确定“北京人”年龄,这种测量方法叫“铝铍测年法”。完成下列填空:
(1)写出Be的核外电子排布式_______________。Be所在的周期中,最外层有2个未成对电子的元素的符号是_______、_________。
(2)写出Al的最外层电子轨道表示式__________________。铝原子核外有_______种运动状态不同的电子;铝原子核外有_______中能量不同的电子。
(3)比较Al3+、S2-和Cl-半径由大到小的顺序_________________________;这3种元素最高价氧化物对应的水化物中酸性最强的是___________(写化学式)。
(4)铝元素最高价氧化物与氢氧化钠溶液反应的化学方程式______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。汽车尾气中含有害的一氧化碳和一氧化氮,利用钯(Pd)等金属作催化剂可以迅速将二者转化为无害的二氧化碳和氮气。
(1)钯与镍位于同列,且在镍的下一周期,钯在元素周期表的位置是__,基态镍原子的价电子的电子排布图为__。
(2)C、N、O的第一电离能由大到小的顺序为__。
(3)SO2分子的VSEPR构型为__;SO3分子中心原子的杂化形式为__;N2O与CO2互为等电子体,且N2O分子中O只与一个N相连,N2O的空间构型为_,分子中的σ键和π键数目之比是__。
(4)大π键是3个或3个以上原子彼此平行的p轨道从侧面相互重叠形成的π键。一氧化氮分子中,氮与氧之间形成一个σ键、一个2电子π键与一个3电子π键,则3电子π键__(填“是”或“不是”)大π键;一氧化氮可与Fe2+生成棕色[Fe(H2O)5NO]2+离子,为检验亚铁离子的反应之一,[Fe(H2O)5NO]2+离子中配位体是__。
(5)CO可形成熔点为-20℃,沸点为103℃的配合物Fe(CO)5,Fe(CO)5分子中铁元素的化合价为___,属于__晶体。
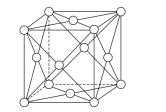
(6)钯晶体的晶胞如图,晶胞的边长为apm,NA表示阿伏加德罗常数的值,则钯单质的密度为___g/cm3(列出计算式)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素![]() 在表中的位置,用 化 学 用 语回答下列问题:
在表中的位置,用 化 学 用 语回答下列问题:
族 周期 | IA | 0 | ||||||
1 |
| ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 |
|
|
| |||||
3 |
|
|
|
| ||||
![]() 的原子结构示意图为_________。
的原子结构示意图为_________。
![]() 的气态氢化物分子的结构式为_____________。
的气态氢化物分子的结构式为_____________。
![]() 、
、![]() 的最高价含氧酸的酸性由强到弱的顺序是________________。
的最高价含氧酸的酸性由强到弱的顺序是________________。![]() 填化学式
填化学式![]()
![]() 、
、![]() 元素的金属性强弱依次为___________。
元素的金属性强弱依次为___________。![]() 填“增大”“减小”或“不变”
填“增大”“减小”或“不变”![]()
![]() 、
、![]() 、
、![]() 的形成的简单离子半径依次_______。
的形成的简单离子半径依次_______。![]() 填“增大”“减小”或“不变”
填“增大”“减小”或“不变”![]()
![]() 、
、![]() 元素可形成既含离子键又含共价键的化合物,写出它的电子式:_______。
元素可形成既含离子键又含共价键的化合物,写出它的电子式:_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】合成气(CO、H2)是一种重要的化工原料气。合成气制取有多种方法,如煤的气化、天然气部分氧化等。回答下列问题:
I.合成气的制取
(1)煤的气化制取合成气。
已知:①H2O(g)=H2O(l) △H=-44kJ/mol;
②部分物质的燃烧热:
![]()
则反应C(s)+H2O(g)![]() CO(g)+H2(g)的△H=___kJ/mol。
CO(g)+H2(g)的△H=___kJ/mol。
(2)天然气部分氧化制取合成气。
如果用O2(g)、H2O(g)、CO2(g)混合物氧化CH4(g),欲使制得的合成气中CO和H2的物质的量之比为1︰2,则原混合物中H2O(g)与CO2(g)的物质的量之比为__。
Ⅱ.利用合成气合成乙醇
在一定条件下,向容积为2L的恒容密闭容器中投入2molCO和4molH2,发生反应:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g)。
CH3CH2OH(g)+H2O(g)。
(1)写出该反应的平衡常数表达式__。
(2)下列情况能作为判断反应体系达到平衡的标志是__(填序号)。
A.压强不再变化 B.平均摩尔质量不再变化 C.密度不再变化
(3)反应起始压强记为p1、平衡后记为p2,平衡时H2的转化率为__。(用含p1、p2的代数式表示)
Ⅲ.合成乙醇的条件选择
为探究合成气制取乙醇的适宜条件,某科研团队对不同温度、不同Rh质量分数的催化剂对CO的吸附强度进行了研究,实验数据如图。CO的非离解吸附是指CO尚未乙醇化,离解吸附是指CO已经乙醇化。
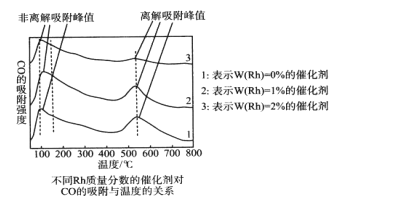
(1)结合图像从低温区、高温区分析温度对CO吸附强度的影响__;以及催化剂对CO吸附强度的影响__。
(2)用Rh作催化剂,合成气制取乙醇的适宜温度是__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com