
科目: 来源: 题型:
【题目】下列实验操作不能达到实验目的的是
选项 | 实验目的 | 实验操作 |
A | 比较金属镁和铝的活泼性 | 分別向两只盛有等体积等浓度的稀硫酸烧杯中加入打磨过的同样大小的镁片和铝片,比较反应现象 |
B | 除去Mg粉中混有的Al 粉 | 加入足量的NaOH 溶液,过滤、洗涤、干燥 |
C | 探究维生素C的还原性 | 向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
D | 配制0.4000mol·L1的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,直接向烧杯中加入250mL水 |
A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化亚铜常用作有机合成催化剂,难溶于水,不溶于稀硝酸和乙醇,但可溶于Cl-浓度较大的体系生成配离子[CuCl2]-,在潮湿空气中易水解氧化为碱式氯化铜。一种制备CuCl的流程如图,下列说法不正确的是

A.X试剂可选用乙醇
B.操作④可在真空中进行
C.流程中可循环利用的物质有两种
D.用去氧水稀释目的是使[CuCl2]-转化为CuCl,同时防止CuCl 被氧化
查看答案和解析>>
科目: 来源: 题型:
【题目】氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
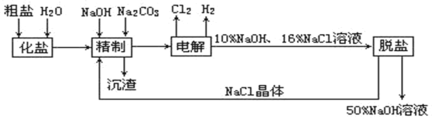
依据上图,完成下列填空:
(1)用惰性电极电解饱和食盐水时,与电源正极相连的电极上所发生的电极反应式为_____________;与电源负极相连的电极附近,溶液pH______(选填:不变、升高或下降)。
(2)如果粗盐中SO42-含量较高,必须加钡剂除去,该钡试剂可以是_________;
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为_______________、_______________;
(4)氯碱工业所用的隔膜电解装置,广泛应用于多种化工产品生产,如工业上用惰性电极电解Na2CO3溶液得到含NaHCO3,原理如下图所示。
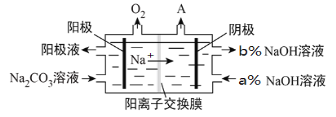
阴极产生的物质A的化学式为__________,a%_____b%(填“<、>、=”),NaHCO3产生在_______室(填“阴极”或“阳极”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】相同金属在其不同浓度盐溶液中可形成浓差电池。如下图所示装置是利用浓差电池电解Na2SO4溶液(a、b电极均为石墨电极),可以制得O2、H2、H2SO4和NaOH。下列说法不正确的是
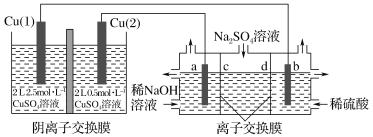
A.a电极的电极反应为4H2O+4e-=2H2↑+4OH-
B.c、d离子交换膜依次为阳离子交换膜和阴离子交换膜
C.电池放电过程中,Cu(1)电极上的电极反应为Cu2++2e-=Cu
D.电池从开始工作到停止放电,电解池理论上可制得320gNaOH
查看答案和解析>>
科目: 来源: 题型:
【题目】CH4-CO2的催化重整不仅可以得到合成气(CO和H2)。还对温室气体的减排具有重要意义。
CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g)。
已知:C(s)+2H2(g)= CH4(g) △H=-75 kJ/mol
C(s)+O2(g)=CO2(g) △H=-394 kJ/mol
C(s)+![]() O2(g)= CO(g) △H=-111 kJ/mol
O2(g)= CO(g) △H=-111 kJ/mol
该催化重整的热化学反应方程式是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用如图所示装置测定中和热的实验步骤如下:
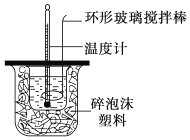
①用量筒量取50mL0.50mol/L盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL0.55mol/LNaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)为什么所用NaOH溶液要稍过量____________________。
(2)倒入NaOH溶液的正确操作是________(填序号)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是________(填序号)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1L1mol·L-1的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3的大小关系为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A 是一种分子量为28的气态烃,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
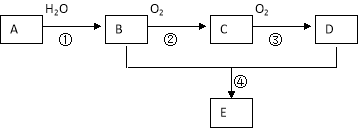
请回答下列问题:
(1)写出A的结构简式 。
(2)B、D分子中的官能团名称分别是 , 。
(3)物质B可以被直接氧化为D,需要加入的试剂是 。
(4)写出下列反应的化学方程式:
① ;反应类型: 。
④ ;反应类型: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于苯的叙述正确的是
A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃
B.从苯的结构简式 看,苯分子中含有碳碳双键,应属于烯烃
看,苯分子中含有碳碳双键,应属于烯烃
C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应
D.苯分子为平面正六边形结构,6个碳原子之间的化学键完全相同
查看答案和解析>>
科目: 来源: 题型:
【题目】已知由氢气和氧气反应生成1 mol水蒸气,放出241.8 kJ热量。
(1)写出该反应的热化学方程式_________。
(2)若1g水蒸气转化成液态水放热2.494kJ,则反应H2(g)+![]() O2(g)=H2O(l)的ΔH=_____kJ/mol。
O2(g)=H2O(l)的ΔH=_____kJ/mol。
(3)HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和NaOH反应的中和热的热化学方程式为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应3X(g)+Y(g)![]() Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
(1)升高温度:____________; (2)增大压强:____________;
(3)增大容器容积:____________; (4)加入X:______________;
(5)加入Y:______________; (6)压缩体积:______________;
(7)加入催化剂_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com