
科目: 来源: 题型:
【题目】一定条件下,在密闭容器中进行反应:3SiCl4(g)+2N2(g)+6H2(g)![]() Si3N4(s)+12HCl(g)。不能表示上述反应达到化学平衡状态的是( )
Si3N4(s)+12HCl(g)。不能表示上述反应达到化学平衡状态的是( )
A.单位时间消耗2molN2,同时生成6molH2
B.c(HCl)保持不变
C.混合气体密度保持不变
D.c(N2):c(H2):c(HCl)=1:3:6
查看答案和解析>>
科目: 来源: 题型:
【题目】大气环境中![]() 的减量化排放受到国内外广泛关注。利用碳还原NO的反应为:
的减量化排放受到国内外广泛关注。利用碳还原NO的反应为:![]() 。回答下列问题:
。回答下列问题:
(1)该反应在常温下可以自发进行,则反应的![]() ________0(填“
________0(填“![]() ”“
”“![]() ”或“
”或“![]() ”),有利于提高NO平衡转化率的条件是________(任写一条)。
”),有利于提高NO平衡转化率的条件是________(任写一条)。
(2)以上反应可分为如下四步反应历程,写出其中第三步的反应:
第一步:![]()
第二步:![]()
第三步:________
第四步:![]()
(3)对比研究活性炭负载钙、镧氧化物的反应活性。在三个反应器中分别加入C、![]() 、
、![]() ,通入
,通入![]() 使其浓度达到
使其浓度达到![]() 。不同温度下,测得第2小时NO去除率如图所示:
。不同温度下,测得第2小时NO去除率如图所示:
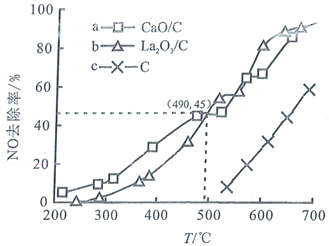
①据图分析,490℃以下,三种情况下反应的活化能最小的是________(用a、b、c表示);![]() 、
、![]() 去除NO效果比C更好,其依据是________(写一条)。
去除NO效果比C更好,其依据是________(写一条)。
②上述实验中,490℃时,若测得![]() 对NO的去除率为60%,则可能采取的措施是________。
对NO的去除率为60%,则可能采取的措施是________。
A.及时分离出![]() B.压缩体积
B.压缩体积
C.恒容下,向体系中通入氮气 D.寻找更好的催化剂
③490℃时的反应速率![]() ________
________![]() ,该温度下此反应的平衡常数为121,则反应达平衡时NO的去除率为________(保留二位有效数字)。
,该温度下此反应的平衡常数为121,则反应达平衡时NO的去除率为________(保留二位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】电动汽车已逐渐走入人们的生活,一些电动汽车动力使用的是钴酸锂(LiCoO2)电池,其工作原理如图,A极材料是金属锂和石墨的复合材料(石墨作为金属锂的载体),电解质为一种能传导Li+的高分子材料。隔膜只允许特定的离子通过,电池反应式为LixC6+Li1xCoO2![]() C6+LiCoO2,下列说法不正确的是
C6+LiCoO2,下列说法不正确的是
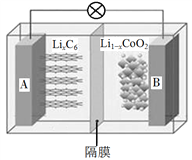
A. 该隔膜只允许Li+通过,放电时Li+从左边移向右边
B. 充电时,B电极与电源正极相连
C. 电池放电时,负极的电极反应式为LixC6xe![]() xLi++C6
xLi++C6
D. 废旧钴酸锂电池进行“放电处理”让Li+进入石墨中而有利于回收
查看答案和解析>>
科目: 来源: 题型:
【题目】德国化学家F.Haber利用N2和H2在催化剂表面合成氨气而获得诺贝尔奖,该反应的微观历程及能量变化的示意图如下,用![]() 、
、![]() 、
、![]() 分别表示N2、H2、NH3,下列说法正确的是( )
分别表示N2、H2、NH3,下列说法正确的是( )
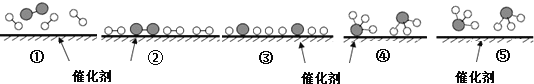
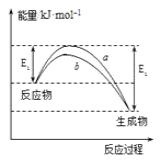
A. 合成氨反应中,反应物断键吸收能量大于生成物形成新键释放的能量
B. 催化剂在吸附N2、H2时,催化剂与气体之间的作用力为化学键
C. 在该过程中,N2、H2断键形成N原子和H原子
D. 使用催化剂,合成氨反应放出的热量减少
查看答案和解析>>
科目: 来源: 题型:
【题目】将等物质的量的A、B混合于2L的密闭容器中,发生下列反应:3A(g)+B(g)![]() xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.25mol·L1·min1,下列说法正确的是
xC(g)+2D(g),经2min后测得D的浓度为0.5mol/L,c(A):c(B)=3:5,以C表示的平均速率v(C)=0.25mol·L1·min1,下列说法正确的是
A. 反应速率v(B)=0.25 mol·L-1·min-1
B. 该反应方程式中x=1
C. 2min时,A的物质的量为1.5mol
D. 2min时,A的转化率为60%
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组为研究电化学原理,设计如图装置.下列叙述不正确的是

A. a和b不连接时,铁片上会有金属铜析出
B. a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu
C. 无论a和b是否连接,铁片均会溶解
D. a和b用导线连接后,Fe片上发生还原反应,溶液中的Cu2+向铜电极移动
查看答案和解析>>
科目: 来源: 题型:
【题目】对于可逆反应4 NH3(g)+5O2(g)![]() 4NO(g)+6 H2O(g),下列叙述正确的是
4NO(g)+6 H2O(g),下列叙述正确的是
A.NH3和H2O化学反应速率关系是2v正(NH3)= 3v正(H2O)
B.达到化学平衡时,4v正(O2)= 5v逆(NO )
C.达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大
D.若单位时间内生成x mol NO的同时,消耗x mol NH3 ,则反应达到平衡状态
查看答案和解析>>
科目: 来源: 题型:
【题目】钻钼系催化剂主要用于石油炼制等工艺,从废钴钼催化剂(主要含有![]() 、CoS和
、CoS和![]() )中回收钴和钼的工艺流程如图:
)中回收钴和钼的工艺流程如图:
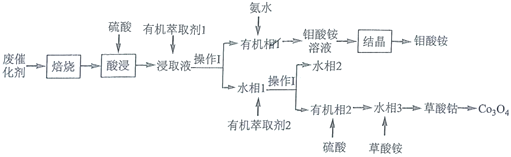
已知:浸取液中的金属离子主要为![]() 、
、![]() 、
、![]() 。
。
(1)钼酸铵![]() 中
中![]() 的化合价为________,
的化合价为________,![]() 在空气中高温焙烧产生两种氧化物:
在空气中高温焙烧产生两种氧化物:![]() 和________(填化学式)。
和________(填化学式)。
(2)为了加快酸浸速率,可采取的措施为________(任写一条)。
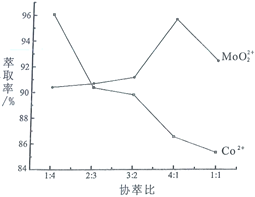
(3)若选择两种不同萃取剂按一定比例(协萃比)协同萃取![]() 和
和![]() ,萃取情况如图所示,当协萃比
,萃取情况如图所示,当协萃比![]() ________,更有利于
________,更有利于![]() 的萃取。
的萃取。
(4)操作Ⅰ的名称为________。
(5)向有机相1中滴加氨水,发生的离子方程式为________。
(6)![]() 萃取的反应原理为
萃取的反应原理为![]() ,向有机相2中加入
,向有机相2中加入![]() 能进行反萃取的原因是________(结合平衡移动原理解释)。
能进行反萃取的原因是________(结合平衡移动原理解释)。
(7)水相2中的主要溶质除了![]() ,还有________(填化学式)。
,还有________(填化学式)。
(8)![]() 可用作电极,若选用
可用作电极,若选用![]() 电解质溶液,通电时可转化为
电解质溶液,通电时可转化为![]() ,其电极反应式为________。
,其电极反应式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期元素X、Y、Z、W、Q原子序数依次增大。已知:X的最外层电子数是次外层的2倍,在地壳中Z的含量最大,W是短周期元素中原子半径最大的主族元素,Q的最外层比次外层少2个电子。请回答下列问题:
(1)X的价层电子排布式是___,Q的原子结构示意图是____。
(2)Y、Z两种元素中,第一电离能较大的是(填元素符号)_____,原因是______。
(3)Z、W、Q三种元素的简单离子的半径从小到大排列的是________。
(4)关于Y、Z、Q三种元素的下列有关说法,正确有是_______;
A.Y的轨道表示式是:
B.Z、Q两种元素的简单氢化物的稳定性较强的是Z
C. Z、Q两种元素简单氢化物的沸点较高的是Q
D.Y常见单质中σ键与π键的数目之比是1:2
(5)Q与Z形成的化合物QZ2,中心原子Q的杂化类型是_____,QZ2易溶于水的原因是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知海水中的溴含量约为65mg·L-1,从海水中提取溴的工业流程如图:
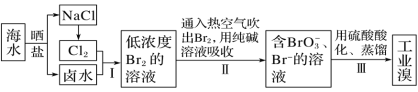
(1)上述步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将其转化成化合态的溴,目的是_____。
(2)步骤Ⅱ通入热空气吹出Br2,利用了溴的______(填字母)。
A.氧化性 B.还原性 C.挥发性 D.腐蚀性
(3)步骤Ⅱ中涉及的离子反应如下,请在方框内填入正确的化学计量数,并将配平后的反应写在答题纸相应位置。_____
![]()
(4)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为_____。
(5)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有______(填字母)。
A.乙醇 B.四氯化碳 C.裂化汽油 D.苯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com