
科目: 来源: 题型:
【题目】ClO2与Cl2的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。
Ⅰ.实验室制备Cl2的离子方程式____________________________。
Ⅱ.某兴趣小组通过下图装置(夹持装置略)ClO2对制备、吸收、释放和应用进行了研究。
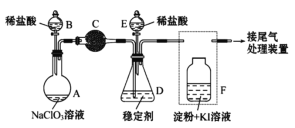
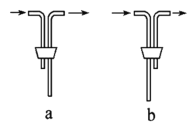
(1)仪器B的名称是___________。安装F中导管时,应选用上图中的_________。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2 在D中被稳定剂充分吸收,滴加稀盐酸的速度宜___________ (填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是___________ 。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为__________________,装置F中的现象是________________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学课外活动小组通过实验探究NO2的性质。已知:2NO2+2NaOH=NaNO3+NaNO2+H2O。任务1:利用如图所示装置探究NO2能否被NH3还原(夹持固定装置已略去)。
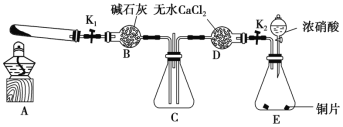
请回答下列问题:
(1)E装置中制取NO2的化学方程式是_____________________________。
(2)此实验装置存在的一个明显缺陷是_______________________________________。
任务2:探究NO2能否与Na2O2发生氧化还原反应。
(3)实验前,该小组同学提出三种假设。
假设1:二者不反应;假设2:NO2能被Na2O2氧化;
假设3:________________________________________________。
(4)为了验证假设2,该小组同学选用任务1中的B、D、E装置,将B中的药品更换为Na2O2,另选F装置(如图所示),重新组装,进行实验。

①装置的合理连接顺序是(某些装置可以重复使用)_________________。
②实验过程中,B装置中淡黄色粉末逐渐变成白色。经检验,该白色物质为纯净物,且无其他物质生成。推测B装置中发生反应的化学方程式为______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】印刷电路板(PCB)是用腐蚀液将覆铜板上的部分铜腐蚀掉而制得。一种用FeCl3溶液制作PCB并将腐蚀后废液回收再生的流程如图:
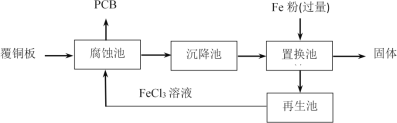
下列说法不正确的是( )
A.腐蚀池中发生反应的化学方程式是:Cu+2FeCl3=CuCl2+2FeCl2
B.腐蚀后的废液中,主要的金属阳离子有Fe3+、Cu2+、Fe2+
C.置换池中发生的主要反应为:Fe+Cu2+=Cu+Fe2+和Fe+2Fe3+=3Fe2+
D.再生池中加入酸化的H2O2,反应过程中pH降低
查看答案和解析>>
科目: 来源: 题型:
【题目】多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇与水在铜基催化剂上的反应机理和能量图如图:
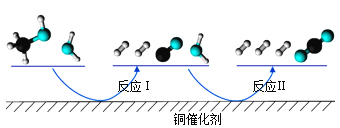

下列说法正确的是( )
A.反应Ⅱ的热化学方程式为:CO(g)+H2O(g)=H2(g)+CO2(g) △H=+akJ/mol(a>0)
B.1molCH3OH(g)和1molH2O(g)的总能量大于1molCO2(g)和3molH2(g)的总能量
C.选择优良的催化剂降低反应Ⅰ和Ⅱ的活化能,有利于减少过程中的能耗
D.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】NaNO2可用作食品添加剂。NaNO2能发生以下反应:3NO2-+2H+=NO3-+2NO↑+H2O
NO2-+Ag+=AgNO2↓(淡黄色)
某化学兴趣小组进行以下探究。回答有关问题:
(l)制取NaNO2反应原理:Na2CO3+2NO2=NaNO2+NaNO3+CO2 Na2CO3+NO+NO2=2NaNO2+CO2
用下图所示装置进行实验。
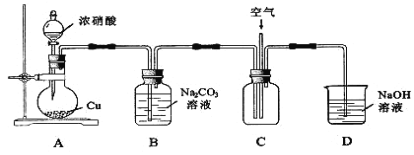
①铜与浓硝酸反应的化学方程式为______________________________。
②实验过程中,需控制B中溶液的pH>7,否则产率会下降,理由是_________。
③往C中通入空气的目的是____________________(用化学方程式表示)。
④反应结束后,B中溶液经蒸发浓缩、冷却结品、___________ 等操作,可得到粗产品晶体和母液。
(2)测定粗产品中NaNO2的含量
称取5.000g粗产品,溶解后稀释至250mL。取出25.00 mL溶液,用0.1000 mol·L-1KMNO4酸性溶液平行滴定三次,平均消耗的体积为20.00mL。已知:2MnO4-+6H++5NO2-=5NO3-+2Mn2++3H2O
①稀释溶液时,需使用的玻璃仪器除烧杯、玻璃棒外,还有 _________(填标号)。
A.容量瓶 B.量筒 C.胶头滴管 D.锥形瓶
②当观察到_________________时,滴定达到终点。
③粗产品中NaNO2的质量分数为____________ (用代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫和氮及其化合物在生产生活中应用广泛。请回答:
(1)蔗糖炭化的过程中,会发生反应:C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是______mol,蔗糖炭化过程体现了浓H2SO4的____(选填:脱水性、吸水性、氧化性、酸性)。
CO2↑+2SO2↑+2H2O,若生成0.5 mol CO2,则转移电子的物质的量是______mol,蔗糖炭化过程体现了浓H2SO4的____(选填:脱水性、吸水性、氧化性、酸性)。
(2)实验室有一瓶放置很久的Na2SO3固体药品,小明同学想设计一个实验验证这瓶药品有没有变质?请你帮助他设计一个实验______________________________________。
(3)Cl2和SO2均可以使品红溶液褪色,将二者等体积混合通入品红,发现红色不褪去,用化学方程式解释其原因__________________________________________________。
(4)工业上可以通过氮气和氢气在一定条件下合成氨气。下列关于氨气的性质和用途描述正确的是____________。
A.氨气易液化,液氨可作制冷剂 B.可用排水法收集氨气
C.氨气是一种无色无味的气体 D.向氨水中滴加酚酞,溶液变红
(5)氨气在一定条件下还可以被氧气所氧化,请写出化学方程式_____________________
(6)实验室检验试管里氨气是否收集满的方法是___________________(写出一种即可)。
(7)25.6 g Cu与含2 mol/L的HNO3和1mol/LH2SO4的200mL混合酸充分反应,反应后收集到的气体在标准状况下的体积为___________________(假设HNO3还原产物为NO)。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酰氯(SO2Cl2)熔点-54.1℃、沸点69.2℃,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。
(1)SO2Cl2中S的化合价为_______,SO2Cl2在潮湿空气中因水解“发烟”的化学方程式为________________。
(2)现拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯,实验装置如图所示(夹持装置未画出)。
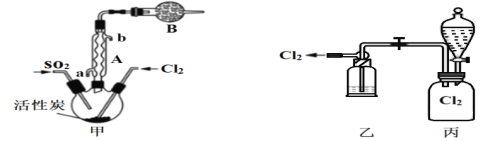
①仪器A的名称为___________,装置乙中装入的试剂_____________,装置B的作用是_______________________。
②装置丙分液漏斗中盛装的最佳试剂是________(选填字母)。
A.蒸馏水 B.10.0 mol/L浓盐酸
C.浓氢氧化钠溶液 D.饱和食盐水
(3)探究硫酰氯在催化剂作用下加热分解的产物,实验装置如图所示(部分夹持装置未画出)。
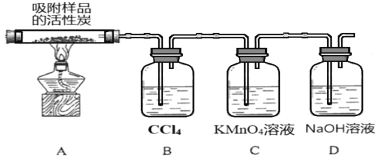
①加热时A中试管出现黄绿色,装置B的作用是 ____________。
②装置C中的现象是___________,反应的离子方程式为___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】脲醛树脂的合成与酚醛树脂类似,生成线型脲甲醛树脂的方程式为:n![]() +nHCHO
+nHCHO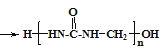 +xH2O,下列说法不正确的是( )
+xH2O,下列说法不正确的是( )
A.网状的脲甲醛树脂以如图所示结构单元为主
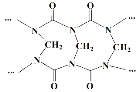
B.方程式中的化学计量数x=n-1
C.脲甲醛树脂合成过程中可能存在中间体![]()
D.通过质谱法测定线型脲甲醛树脂的平均相对分子质量,可得其聚合度
查看答案和解析>>
科目: 来源: 题型:
【题目】一定量的锌与100 mL 18.5 mol·L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6 L(标准状况)。将反应后的溶液稀释至1 L,测得溶液的c(H+)=0.1 mol·L-1。下列叙述不正确的是( )
A. 反应中共消耗1.8 mol H2SO4B. 气体甲中SO2与H2的体积比为4∶1
C. 反应中共消耗97.5 g ZnD. 反应中共转移3 mol电子
查看答案和解析>>
科目: 来源: 题型:
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com