
科目: 来源: 题型:
【题目】下列对氧化还原反应的分析中合理的是
A.Mg变为MgO时化合价升高,因此,Mg在该反应中作还原剂
B.KMnO4受热分解时,Mn元素化合价一方面升高一方面降低,因此,在该反应中Mn元 素既被氧化又被还原
C.凡是氧化还原反应都能造福人类
D.在反应2H2O![]() 2H2↑+ O2↑中H2O是还原剂
2H2↑+ O2↑中H2O是还原剂
查看答案和解析>>
科目: 来源: 题型:
【题目】若气态烃A的相对分子质量为26,根据下列转化关系推断:
A![]() B
B![]() C;A
C;A![]() D
D![]() E。
E。
(1)写出A~E的结构简式:
A_____B________C_________D_________E___________
(2)写出下列反应的化学方程式:
B ![]() C:_________。
C:_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是 ( )
A. 2 mol H2O的摩尔质量和1 mol H2O的摩尔质量
B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-)
C. 64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D. 20% NaOH溶液中NaOH的物质的量浓度和10% NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目: 来源: 题型:
【题目】某固体混合物中,可能含有下列离子中的几种:K+、NH4+、Mg2+、Ba2+、Cl-、SO42-、CO32-,将该混合物溶于水后得澄清溶液,现取三份各100mL该溶液分别进行如下实验:
(1)在一份溶液中加入AgNO3溶液,有白色沉淀生成;
(2)在另一份溶液中加入足量的NaOH溶液并加热,收集到1.12L气体(标准状况下);
(3)在第三份溶液中加入足量的BaCl2溶液有沉淀生成,经称量其质量为6.27g,在该沉淀中 加入足量的盐酸,沉淀部分溶解,剩余固体质量为2.33g。
根据上述实验回答下列问题:
①溶液中一定不存在的离子是:_______________________________;
②溶液中一定存在的阴离子有:_______________;其物质的量浓度分别为:_____________;
③推断K+是否存在:(填“是 ”或“否”)________________,其物质的量浓度为:___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各物质中只有A、B、C三种单质,A的焰色反应为黄色,主要以G形式存在于海水中,F是一种淡黄色的固体,H是一种常见的无色液体,I是造成温室效应的“元凶”,各物质间的转化关系图如下:
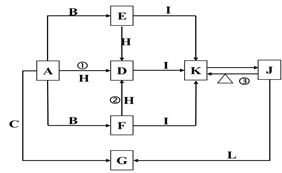
回答下列问题:
(1)A是:____________, I是:____________(填化学式);
(2)按要求写出下列反应的方程式:
Ⅰ.①的化学方程式:______________________________;
Ⅱ.②的化学方程式(同时用双线桥法表示该反应的电子转移情况):________________;
Ⅲ. J与过量的澄清石灰水反应的离子方程式:______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填些对应的化学符号
(1)质量数为37的氯原子符号为________。
(2)S2-的结构示意图________。
(3) N2的电子式________
(4)磷原子的核外电子排布式__________铬原子价电子排布图_____________
(5)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为__________。
(6)B元素的正三价离子的3d能级为半充满,其基态原子的电子排布式为___________
(7)O、N、F 3种元素的第一电离能由大到小的顺序为________(用元素符号表示)
(8)前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子数相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。四种元素中,D元素在周期表中的位置____第一电离能最小的是_____(填元素符号,下同),电负性最大的是______
(9)已知和碳元素同主族的X元素位于周期表中的第1个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们形成的化学式为XY4的物质。试回答:
X元素原子的基态电子排布式为__________
Y元素原子最外层电子的轨道表示式为________
若X、Y两元素电负性分别为2.1和2.85,则XY4中X与Y之间的化学键为_______(填“共价键”或“离子键”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某纯碱试样中含有 NaCl 杂质,为测定试样中纯碱的质量分数,可用下图中的装置进行实验。
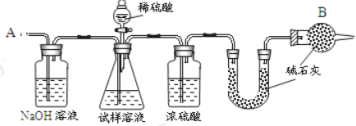
主要实验步骤如下:
①按图组装仪器,并检查装置的气密性;
②将 a g 试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
③称量盛有碱石灰的 U 形管的质量,得到 b g;
④从分液漏斗滴入 6 molL-1的硫酸,直到不再产生气体时为止;
⑤从导管 A 处缓缓鼓入一定量的空气;
⑥再次称量盛有碱石灰的 U 型管的质量,得到 c g;
⑦重复步骤⑤和⑥的操作,直到 U 型管的质量基本不变,为 d g;
请填空和回答问题:
(1)第一个洗气瓶中氢氧化钠溶液的作用是____________________
(2)装置中干燥管 B 的作用是_______________________________
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的结果_________(填偏高、偏低或不变)。
(4)步骤⑤的目的是_______________________________________
(5)步骤⑦的目的是_________________________________________
(6)该试样中纯碱的质量分数的计算式为________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空:
(1)还原铁粉与高温水蒸气反应的化学方程式:_____________________________________;
(2)除去Mg粉中的Al粉的试剂是__________ ,反应的离子方程式为:____________;
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
____Fe(OH)3 +____ClO-+____OH- =__FeO42-+___Cl-+__(_______)
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是________________;还原剂是_______________;当有11molP参加反应,转移的电子的物质的量为________;1molCuSO4能氧化的P原子的数目为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】四氢呋喃是常用的有机溶剂,可由有机物A(分子式:C4H8O)通过下列路线制得
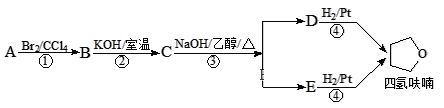
已知:R1X + R2OH![]() R1OR2 + HX
R1OR2 + HX
下列说法不正确的是
A. C中含氧官能团为醚键
B. A的结构简式是CH3CH=CHCH2OH
C. D和E均能使酸性高锰酸钾溶液褪色
D. ①③的反应类型分别为加成反应、消去反应
查看答案和解析>>
科目: 来源: 题型:
【题目】过氧化钙(![]() )在室温下稳定,加热至350℃左右迅速分解。实验室制备反应:
)在室温下稳定,加热至350℃左右迅速分解。实验室制备反应:![]() ,装置如图所示。下列说法错误的是( )
,装置如图所示。下列说法错误的是( )
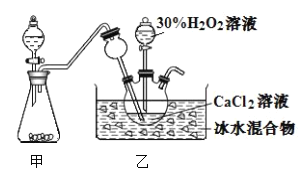
A.长颈漏斗可以起到防倒吸的作用
B.甲装置可以用浓氨水和碱石灰来制备氨气
C.冰水混合物的主要作用是防止生成的过氧化钙受热分解
D.反应过程中![]() 不断中和
不断中和![]() 和过氧化氢生成的
和过氧化氢生成的![]() ,促进反应进行
,促进反应进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com